2019届初三下册中考二模化学考题(浙江省宁波市四明中学)
| 1. | 详细信息 |
|
2018年12月9日,联合国气候大会在波兰举行,对“中国减排和应对气候变化的举措”给予高度肯定。下列说法不符合“减排”措施的是( ) A. 公交优先低碳出行 B. 开发和利用新能源 C. 大量开采化石能源 D. 倡导绿色化学理念 |
|
| 2. | 详细信息 |
在粗盐提纯的实验中,下列操作不规范的是 A. 称量 B. 溶解 C. 过滤 D. 蒸发 |
|
| 3. | 详细信息 |
|
三氧化二碳(化学式C2O3)通常情况下是一种无色无味的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其他的化学性质与一氧化碳相似。下列有关三氧化二碳说法错误的是 A. C2O3中碳元素的化合价为+4价 B. 三氧化二碳具有还原性 C. 在空气中燃烧的产物为二氧化碳 D. 与氢氧化钠溶液反应可生成盐 |
|
| 4. | 详细信息 |
|
下列有关溶液、饱和溶液、不饱和溶液的有关说法正确的是( ) A. 均一稳定的液体一定是溶液 B. 20℃时KNO3的饱和溶液可以继续溶解NaCl,但不能溶解KNO3 C. 不饱和溶液降低温度后一定会变成饱和溶液 D. 饱和溶液的浓度一定比不饱和溶液的浓度大 |
|
| 5. | 详细信息 |
|
人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色. (1)西汉时期中国古老的冶铜方法是“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,写出反应的化学方程式_____. (2)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图. 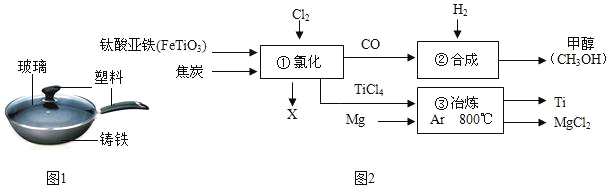 ①铁锅含有的有机合成材料是_____.(填写名称). ②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是_____. ③铜也易生锈,铜锈的主要成分是碱式碳酸铜(Cu(OH)2CO3),是铜与空气中的氧气、水和_____共同作用的结果. (3)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、航天飞机、船舶等,如图为某化工企业生产钛流程示意图: 请回答下列问题: ①FeTiO3中钛元素的化合价为_____; ②氯化中化学方程式为2FeTiO3+6C+7Cl2 ③合成中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是_____. ④冶炼中氩气的作用是_____,该步反应的化学方程式为_____. |
|
| 6. | 详细信息 |
如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,若E是生活中常用的调味剂、防腐剂,(部分反应条件略去),试回答下列问题: (1)写出物质的化学式为:C_____、D_____、G_____. (2)反应①的化学方程式为:_____. (3)图中标出的九种物质按单质、氧化物、酸、碱、盐进行分类,一定没有的物质类别是_____. (4)反应①~⑤中没有涉及的基本反应类型是_____. |
|
| 7. | 详细信息 |
|
某化学学习小组的同学在学习了《常见的酸》以后,对蚊虫分泌的让人痛痒不止的蚁酸产生了兴趣。他们在老师指导下对蚁酸进行探究。 (查阅资料)蚁酸的主要成分是甲酸,甲酸的化学式为HCOOH;甲酸溶于水,在一定条件下发生分解反应生成两种氧化物。 (提出问题)甲酸溶液是否具有酸性? (实验与结论)向盛有甲酸溶液的试管中滴加紫色石蕊溶液,观察到溶液颜色变成红色,说明甲酸溶液显____性。 (提出问题)甲酸分解生成的两种氧化物是什么? (推断与猜想) ⑴小组同学根据甲酸中含有氢元素,推测出生成物中含有水。 ⑵他们对另一种氧化物提出两种猜想:猜想①:二氧化碳;猜想②:一氧化碳。 (实验与结论) 为了证明自己的猜想,他们将甲酸分解产生的气体通过如下图所示的装置(铁架台已略去)。 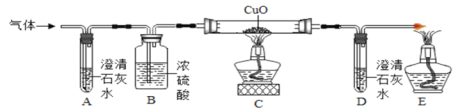 观察到的实验现象如下: Ⅰ.装置A中澄清石灰水无明显变化。 Ⅱ.装置C中的黑色粉末变红色。 Ⅲ. 装置D中澄清石灰水变浑浊。 (实验结论)甲酸具有酸性,在一定条件下分解生成水和_______。 (拓展延伸)人被蚊虫叮咬后,在其叮咬处涂抹______________可减轻痛痒。 |
|
| 8. | 详细信息 |
|
通过分析、计算回答下列问题: (1)相同质量的钠、镁、铝、钾中所含原子个数最多的是_____。 (2)N(NO2)3是科学家发现的一种新型火箭燃料,试计算: ①N(NO2)3的相对分子质量是_____。 ②N(NO2)3中氮元素和氧元素的最简质量比是_____。 ③N(NO2)3中氮元素的质量分数是_____精确到0.1%)。 (3)取一种可燃物3.2克充分燃烧,测得生成二氧化碳4.4克,水3.6克,试求: ①该可燃物中含有的元素各占多少克_____?(写出完整的计算过程) ②该可燃物的分子中各原子的个数比是_____。 |
|
| 9. | 详细信息 |
同学们从山上采集到一种石灰石样品,为了测定石灰石样品中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应,也不溶于水),取45g石灰石样品,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示,请计算: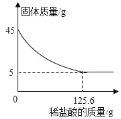 (1)45g这种石灰石样品中碳酸钙的质量是_____g (2)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。 (3)列式计算45g石灰石与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数?_____。 |
|
最近更新



