山东省肥城市2022届高考适应性训练(二)化学试题
山东省肥城市2022届高考适应性训练(二)化学试题
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-04-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
2021年我国取得让世界瞩目的科技成果,化学功不可没,下列说法错误的是( )
A . 我国成功研制出多款新冠疫苗,采用冷链运输疫苗,以防止蛋白质变性
B . “海牛II号”刷新世界钻探深度,钻头采用硬质合金材料,其硬度高于组分金属
C . “天和核心舱”电推进系统中的腔体采用氮化硼陶瓷属于新型无机非金属材料
D . 二氧化碳到淀粉的人工全合成技术,可减少向空气中排放CO2形成酸雨
|
|
| 2. 单选题 | |
|
下列关于物质的性质与用途不具有对应关系的是( )
A . CO具有还原性,可用于冶炼铁
B . 明矾溶液显酸性,可以用于清洗铜镜表面的铜锈
C . SO2具有氧化性,可用于漂白纸浆
D . NaNO3具有氧化性,可用于使铁器表面产生Fe3O4
|
|
| 3. 单选题 | |
|
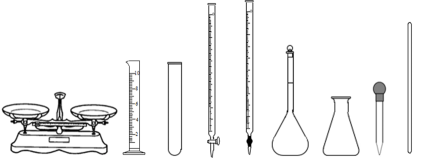
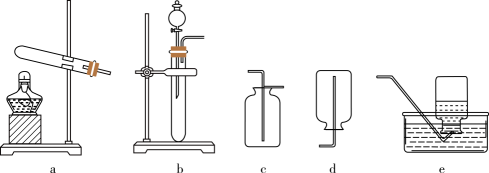
浓盐酸易挥发,无法直接配制具有准确浓度的标准溶液,因此配制HCl标准溶液的具体流程如下:
按上述流程进行操作,下列仪器中不需要用到的有( )
A . 1种
B . 2种
C . 3种
D . 4种
|
|
| 4. 单选题 | |
|
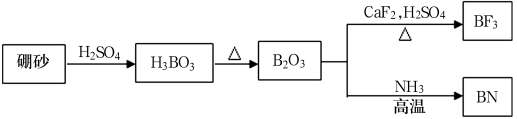
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示。下列叙述正确的是( )
A . NH3与BF3都是由极性键构成的极性分子
B . 六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C . NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1molNH4BF4含有配位键的数目为NA
D . 立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝
|
|
| 5. 单选题 | |||||||||||||||||||||||||||||||
|
实验室制备下列气体所选试剂、制备装置、收集方法及操作均正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||||||||||||
| 6. 单选题 | |
|
据文献报道,氨催化还原法可用来消除某些污染气体,其反应历程如图所示:
下列说法错误的是( )
A . V的价电子排布式为3d34s2
B . V5+—OH在该反应过程中作催化剂
C . 总反应化学方程式:4NH3+3O2
 2N2+6H2O
D . 当消耗标准状况下11.2LO2时,整个过程转移6mole- 2N2+6H2O
D . 当消耗标准状况下11.2LO2时,整个过程转移6mole-
|
|
| 7. 单选题 | |
|
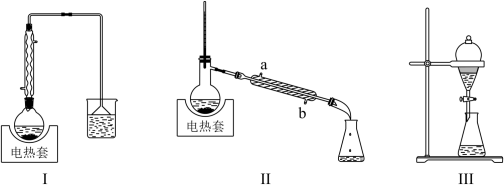
1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴丁烷粗产品,装置如图所示:
已知: 下列说法正确的是( )
A . 装置I中回流的目的是为了提高产率
B . 装置II中a为进水口,b为出水口
C . 用装置III萃取分液时,将分层的液体依次从下放出
D . 蒸馏完毕后,应先停止通冷凝水,再停止加热
|
|
| 8. 单选题 | |
|
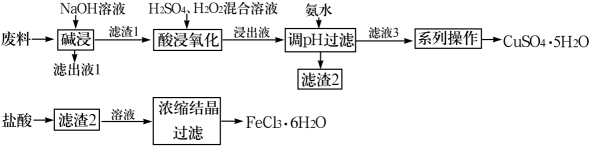
FeCl3·6H2O是城市污水及工业废水处理的高效廉价絮凝剂,具有显著的沉淀重金属及硫化物、脱色、脱臭除油、杀菌等功效。利用废料(主要成分为Fe2O3、Cu2O及少量Ga2O3)制备FeCl3·6H2O和CuSO4·5H2O的流程如下。下列说法错误的是( )
已知:①镓(Ga)和铝同主族,具有相似的化学性质。 ②25℃时,
A . 浸出液1中溶质除了NaOH,还主要含有NaGeO2
B . “酸浸氧化”中H2O2参与反应的离子方程式为Cu2O+H2O2+4H+=2Cu2++3H2O
C . 当金属阳离子浓度为1.0×10-5mol·L-1时恰好沉淀完全,用氨水调pH后滤液3的pH为3
D . 在实验室中进行“浓缩结晶”操作所需的硅酸盐仪器有酒精灯、坩埚、玻璃棒
|
|
| 9. 单选题 | |
|
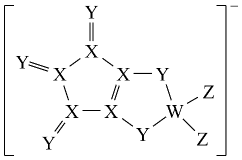
LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成,结构如图,Y的最外层电子数等于X的核外电子总数,下列说法正确的是( )
A . 同周期元素第一电离能小于Y的有5种
B . 简单氢化物的还原性:X<Y
C . 四种元素中原子半径最大的是W
D . 四种元素形成的单质中Y的氧化性最强
|
|
| 10. 单选题 | |
|
某钠离子电池结构如图所示,电极A为含钠过渡金属氧化物(NaxTMO2),电极B为硬碳,充电时Na+得电子成为Na嵌入硬碳中。下列说法错误的是( )
A . 充电时,电极B与外接直流电源的负极相连
B . 放电时,外电路通过a mol电子时,A电极电解质损失a mol Na+
C . 放电时,电极A为正极,反应可表示为Na1-xTMO2+ xNa+ + xe-= NaTMO2
D . 电池总反应可表示为Na1-xTMO2+ NaxC = NaTMO2+ C
|
|
高中化学 试卷推荐
- 高中化学鲁科版(2019)必修第二册 第3章测试卷
- 河北省邯郸市2016-2017学年高一上学期化学期末考试试卷
- 2016-2017学年江西省抚州市崇仁二中高一上学期期中化学试卷
- 江苏省淮安市2019-2020学年高一下学期化学期末考试试卷
- 备考2019年高考化学二轮专题 06 化学反应中的能量变化
- 广东省佛山市顺德区2019-2020学年高一下学期化学期末考试试卷
- 2016年江西省新余市分宜一中高考化学五模试卷
- 黑龙江哈尔滨第三中学2020年高考理综-化学二模试卷
- 北京市朝阳区2020年高考化学模拟试卷
- 重庆市开州区2017-2018学年高二下学期化学期末考试试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 四川省攀枝花市2017-2018学年高二上学期化学期末考试试卷
最近更新


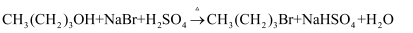
 。
。