制取气体的反应原理的探究 知识点题库
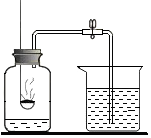
为测定气球内的气体成分,有学生用超薄材料制成的气球按如图装置进行实验.开始时气球沉于烧杯底部,打开开关后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口.气球内可能的气体是( )
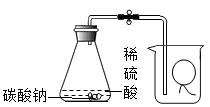
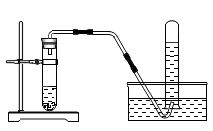
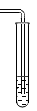
人通过肺与外界进行气体交换,吸入空气,排出CO2等气体.但人体排出的CO2究竟是空气中原有的,还是人体代谢的最终产物.为了证实这个问题,某同学采用了如图装置进行实验.实验过程是:一同学反复慢慢从呼吸口呼吸,能证明人呼出的气体中所含有CO2不是来自空气,而是人体的代谢最终产物,请回答:
(1)呼气时,乙瓶中的现象是 。
(2)甲瓶中所装试剂的作用是 ;丙瓶中所装试剂的作用是 。
(3)请写出甲瓶中反应的化学方程式 。
(4)能验证实验目的的现象是 。
 高锰酸钾+二氧化锰+氧气
B . 氧化汞
高锰酸钾+二氧化锰+氧气
B . 氧化汞 汞+氧气
C . 水
汞+氧气
C . 水 氧气+氢气
D . 过氧化钠+二氧化碳→碳酸钠+氧气
氧气+氢气
D . 过氧化钠+二氧化碳→碳酸钠+氧气
 锰酸钾+二氧化锰+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢
锰酸钾+二氧化锰+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢 水+氧气
水+氧气
①利用该反应获得氧气时不要加热,可以节约能源;②该反应可将废气二氧化碳进行利用;
③反应物和生成物都属于氧化物;④实验室利用这一原理制取的氧气中可能混有二氧化碳;
⑤该反应是化合反应.
 锰酸钾+二氧化碳+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢
锰酸钾+二氧化碳+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢  水+氧气
水+氧气
-
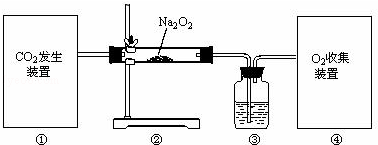
(1) 装置①中CO2的制取方法有多种:若用稀盐酸和石灰石制取CO2 , 该反应的化学方程式为若用加热分解NaHCO3固体制取CO2 , 应该选用的发生装置为(选填如图字)
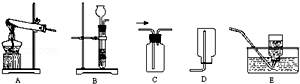
-
(2) 装置③中盛装的试剂为,作用是.
-
(3) ④为O2的收集装置,可选用装置C,如何验满:.

-
(1) 图中仪器a的名称 ,
-
(2) 用高锰酸钾制取氧气时,装置A还需要做的一点改动是。其化学方程式为。
-
(3) 实验室用锌粒和稀硫酸制取氢气可选用的发生装置和收集装置是。(填字母,下同),
-
(4) 用大理石和稀盐酸制取二氧化碳时,可选用的发生装置和收集装置是。
-
(5) (二)水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少量的二氧化碳和水蒸气。某课题组同学为验证水煤气的成分,设计如下实验装置:
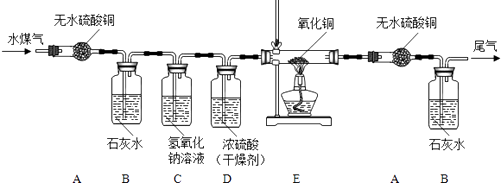
请分析上面信息后回答:
①利用上述装置验证水煤气中四种成分的依次顺序是 (填气体的化学式);
②装置C的目的是 ,装置E内观察到的现象是 ;
③实验中两次用到装置A,其目的分别是 、 。
-
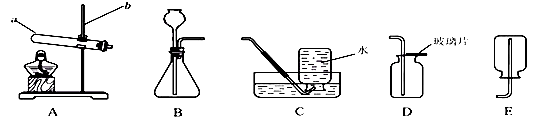
(1) 写出仪器a和b的名称:a,b。
-
(2) 加热氯酸钾和二氧化锰的混合物制取氧气,该反应的化学方程式为。
-
(3) 用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为(填字母)。
-
(4) 与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的盖好集气瓶(填“光滑面”或“磨砂面”)。
-
(5) 检验氧气是否收集满的正确操作是
-
(6) 某同学用上述A中的方法制取氧气,实验过程中试管发生了炸裂,请你帮他分析试管炸裂可能的原因是。(写一条即可)
【资料查阅】①浓盐酸具有挥发性,能挥发出氯化氢气体
②HCl与AgNO3溶液发生反应,生成白色沉淀(白色沉淀为不溶于水也不溶于酸的AgCl)。
③盐酸可与石灰水反应:Ca(OH)2+2HCl═CaCl2+2H2O
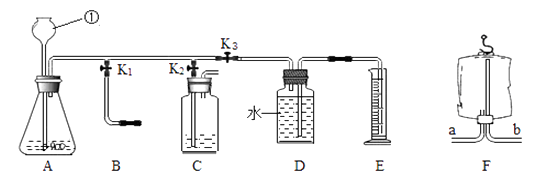
探究一 气体的制取
-
(1) 写出图中①的仪器名称:。
-
(2) 用装置A制取二氧化碳的反应化学方程式是。若装置A用于实验室制取氧气,则反应化学方程式是。
-
(3) 生活中有许多物品可以代替实验仪器。关闭K2和K3 , 打开K1 , 若用装置F所示的医用塑料袋排空气法收集CO2 , 则F装置(填“a”或“b”)端与B装置相连。
探究二 气体的性质检验
打开K2、关闭K1和K3 , 用于检验制取的二氧化碳性质。
-
(4) 若装置C中是紫色石蕊试剂,可观察到(填现象),证明二氧化碳与水发生了反应。若装置C中试剂是澄清石灰水,则该反应的化学方程式是。
-
(5) 小强将制取的二氧化碳通入澄清石灰水中,未见浑浊,小强认为是使用的盐酸浓度过高,挥发进入石灰水中。要验证是否是上述原因,设计实验方案为:。
-
(6) 探究三 测定气体生成的反应速率
关闭K1、K2 , 打开K3 , 可测一段时间内生成二氧化碳气体的速率。所测得数据如下:
稀盐酸的体积(mL)
(反应前)
大理石质量(g)(反应前)
E装置收集的液体量(mL)
反应时间(s)
50
5.0
37.8
100
由实验数据可知,生成CO2的体积为 mL。
-
(7) 若生成气体的反应速率用公式v =△V/△t表示(△V表示生成气体的体积、△t表示反应所用的时间),则生成的二氧化碳的速率为 mL/s。
-
(8) 有同学认为,图中的测量方法容易带来误差,请指出造成误差的原因(写一点)。
-
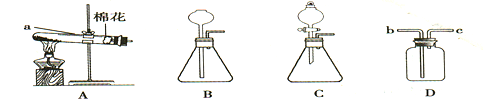
(1) 请写出图A中仪器a的名称;
-
(2) 实验室选用B装置制取氧气时,反应的化学方程式为;用此方法制取的氧气中通常含有水蒸气,若用D装置除去水蒸气,则D中盛放的试剂为
-
(3) 某同学用碳酸钠粉末和稀盐酸反应来制取二氧化碳,为了较好地控制反应速率,可选用的发生装置是(填字母序号);若用D装置收集二氧化碳,气体应从(填“b”或“c”)端进入。
-
(4) 用A装置制取氧气时,试管中棉花的作用为;棉花没有燃烧的主要原因是
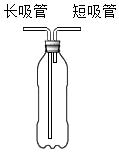
(探究一)用如图所示自制装置进行“人体吸入和呼出气体成分”的探究。
(提出假设)人体呼出气体中二氧化碳的含量高于吸入气体。
(进行实验)实验1
|
步骤 |
操作 |
现象 |
|
① |
在饮料瓶中装水至浸没过长吸管底端,对着短吸管缓慢吹气 | 水从长吸管端快速流出 |
| ② | 将饮料瓶中装满水,对着短管吹气,水排空后,将燃着的木条快速伸入饮料瓶中 | 饮料瓶中木条熄灭 |
| ③ | 将水倒掉,向饮料瓶中加入澄清石灰水至没过长吸管底,从短吸管端吸气30秒,观察石灰水的变化;再从长吸管端吹气30秒,观察石灰水的变化 |
-
(1) 步骤①说明,自制装置的气密性(填“良好”或“不良”)。
-
(2) 步骤②中的现象(填“能”或“不能”)证明呼出气体中含二氧化碳。
-
(3) 若假设成立,步骤③中,预期会观察到的现象是。
-
(4) 实验2
实验1中有同学发现,吹气一段时间后发现,浑浊的石灰水重新变得澄清。他用上述装置加入与实验1等体积的石灰水,做下列实验来研究这一问题。
实验编号
石灰水浓度
持续吹气时间
瓶底现象
2-1
0.16%
30秒
澄清石灰水变浑浊
2-2
0.16%
2分钟
澄清石灰水先变浑浊,后又变得澄清
2-3
0.08%
30秒
澄清石灰水先变浑浊,后又变得澄清
2-4
0.08%
2分钟
澄清石灰水先变浑浊,后又变得澄清
(反思与评价)
石灰水变浑浊发生反应文字或符号表达式为,能说明石灰水重新变澄清与石灰水浓度有关的实验是(填实验编号)。
-
(5) 实验1中,吹气时间均为30秒,有同学观察到石灰水变澄清,而有的学生未观察到,产生现象差异的可能原因是。
-
(6) (探究二)实验室制取二氧化碳药品的选择
某硏究小组在实验室制取CO2发现,通常不选用大理石与稀硫酸反应制取CO2 , 原因是反应生成硫酸钙微溶物覆盖在固体表面,阻碍了大理石与稀硫酸接触,反应速率逐渐减慢甚至停止。该小组猜测,硫酸的浓度是否会对实验效果造成影响?他们试图选择出合适浓度的硫酸。(实验所用硫酸浓度均为反应速率合理范围内)
操作:在28℃时,分别向五支各盛有等量大理石的试管中加入等体积硫酸,15分钟内生成气体的体积见右表:
试管编号
1
2
3
4
5
硫酸浓度(%)
15
20
25
30
35
气体体积(mL)
35
47
55
51
42
请回答:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为%。
②除选用合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加操作,更有利于气体的制备。
③大理石和稀硫酸反应生成硫酸钙、水和二氧化碳,试写出反应的文字表达式。
④提出猜想:请写出另一种你认为可能影响反应速率的因素。
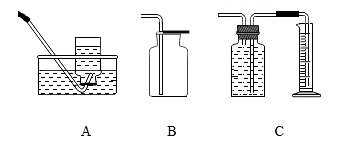
⑤在该实验中,你认为可以用下列装置收集气体的是(填编号)。(假设液体不与二氧化碳反应,也不溶解二氧化碳)
-
(1) 实验室制取气体时,确定发生装置需要考虑的两种因素有(填序号)。
A 反应物的状态 B 气体的密度
C 反应的条件 D 气体的溶解性
-
(2) 实验室部分装置如图(A﹣F)所示,请回答:
(提示:装置C的多孔隔板,可以放置颗粒大小比孔径大的固体)
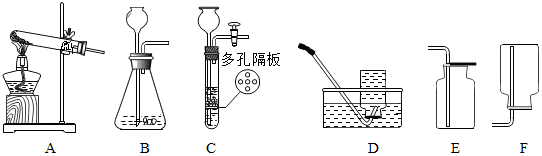
下表是初中几种常见气体的实验室制法,请你在横线上的空白处填上答案。
反应物
制取气体
发生装置(填字母)
收集装置(填字母)
大理石和稀盐酸
CO2
B或
锌粒和稀硫酸
H2
B
D或
高锰酸钾
O2
E或D
-
(3) 实验室常用高锰酸钾来制取氧气,其化学方程式为 ;
-
(4) 小颖同学在探究二氧化碳性质时,将二氧化碳气体通入紫色石蕊溶液中,石蕊溶液很快变红色,原因是。
-
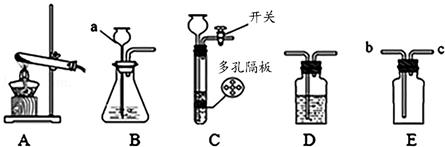
(5) 若使用图1装置收集氧气,气体应从(填“a”或“b”)端通入。若通过连接图1和图2装置来测量氧气的体积,应将图2装置的c端与图1装置的(填“a”或“b”)端相连。一段时间后量筒内的凹液面如图3所示,则集得氧气的体积是mL。
-
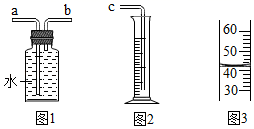
(1) 实验室用装置A制备氧气,反应的化学方程式为。
-
(2) 实验室制取氢气的药品是(填名称),实验室可选用C装置(孔隔板用来放块状固体)制取氢气,该装置的优点是。
-
(3) E装置可用于气体的收集、检验、除杂等,该装置能完成的实验是 (填序号,可多选)。A . 收集氧气,气体从b端通入,将带火星木条放在c端管口进行验满。 B . 瓶内装有澄清石灰水,气体从b端通入,检验氧气中是否混有二氧化碳。 C . 瓶内装有水,气体从b端通入,除去一氧化碳中混有的二氧化碳。 D . 瓶内装满水,在c端接量筒,气体从b端通入,测量氧气的体积。
-
(1) 如图是实验室气体制取常用装置图,请根据所给装置图回答问题:
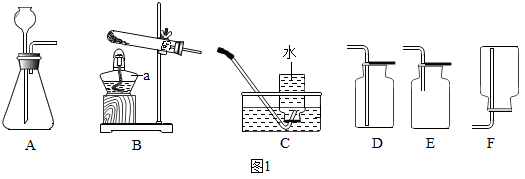
①请写出图1中标号a仪器的名称: 。
②小丽同学在实验室制取氧气,选取了B这一发生装置,请你根据小丽选取的装置写出实验室制取氧气的药品的化学式, 若要收集二氧化碳你选择的装置(填字母序号),用该装置验满二氧化碳的方法 。
-
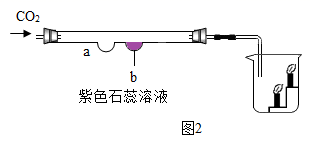
(2) 检验二氧化碳的性质实验如图2所示。
①实验过程中,b处的实验现象是。若要证明二氧化碳与水反应,应在a处放;
②根据烧杯中的实验现象,得出的结论是。
-
(3) 石灰石高温煅烧获得的生石灰(主要成分CaO)是炼钢生产中的主要造渣材料,煅烧温度1050℃时,加NaCl和不加NaCl,如图是比较煅烧石灰石的分解率。
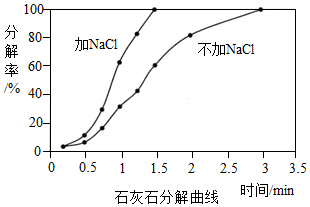
由图像你能得出实验(3)的结论是。
-
(1) 实验时药品选择不当,可能会导致无法达到实验目的,也可能影响实验效果。请将A与①分为一类,分类标准是②。

A.用硫黄代替红磷测定空气中氧气含量
B.用铝片代替锌粒与稀硫酸反应制取氢气
C.用氢氧化钠溶液代替澄清石灰水检验二氧化碳
D.用食醋代替稀盐酸与石灰石反应制取二氧化碳
-
(2) 相同的反应物可能会发生不同的反应,生成不同的物质。
①碳与氧气充分燃烧时生成二氧化碳,不充分燃烧时却生成一氧化碳,由此得出当反应物不同,生成物可能不同的结论。
②反应条件不同时,生成物也可能不同,例如:
 , 请写出与其反应条件不同的反应的化学方程式。
, 请写出与其反应条件不同的反应的化学方程式。
-
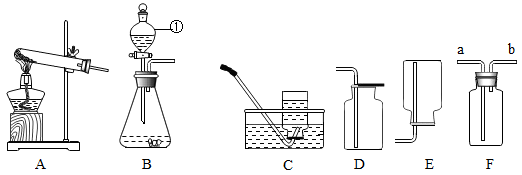
(1) 装置B中标号仪器①的名称是。
-
(2) 实验室制取二氧化碳的化学方程式为。
-
(3) 用双氧水和二氧化锰制取氧气的化学方程式为,反应后过滤,干燥,所得到的二氧化锰(填“能”或“不能”)继续作为双氧水分解的催化剂。
-
(4) 用C收集气体,收集满的现象是。若用F装置收集二氧化碳,气体应从(选填“a”或“b”,下同)端通入。若用F排水法收集气体,气体应从端通入。
-
(5) 二氧化硫是有毒气体,密度比空气大,易溶于水。实验中常用氢氧化钠溶液吸收二氧化硫尾气。用如图所示装置收集一瓶干燥的二氧化硫,装置中导管按气流方向连接顺序是①→②→→⑤(填序号)。烧杯中发生反应的化学方程式为。

 , 已知漂白粉的有效成分为Ca(ClO)2。该兴趣小组用图所示装置进行实验。
, 已知漂白粉的有效成分为Ca(ClO)2。该兴趣小组用图所示装置进行实验。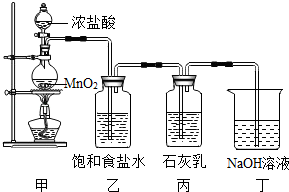
-
(1) 甲装置中二氧化锰和浓盐酸在加热条件下发生反应制备氯气,同时生成MnCl2和一种氧化物,该反应的化学方程式为。
-
(2) 乙装置的作用是。
-
(3) 小组成员发现,实际上产物中Ca(ClO)2的质量明显小于理论值。小组成员为探究原因,查阅资料发现:氯气和碱反应时会放热,温度较高时。氯气和碱还能发生反应
 。为提高Ca(ClO)2的产率,可对丙装置作适当改进,改进方法可以是(填一种即可)。
。为提高Ca(ClO)2的产率,可对丙装置作适当改进,改进方法可以是(填一种即可)。
-
(4) 该兴趣小组用浓盐酸与MnO2制备得到氯气7.1g,并将所得氯气与过量的石灰乳反应,则理论上最多可制得多少克Ca(ClO)2?(写出具体计算过程)
-
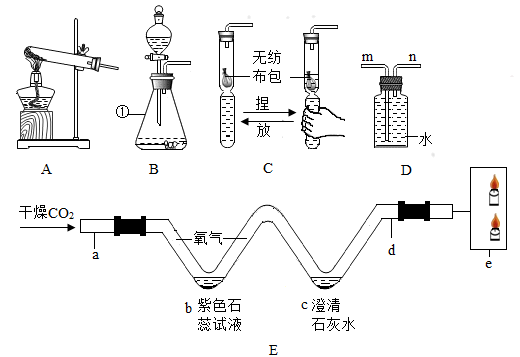
(1) 写出标有①的仪器名称。
-
(2) 写出实验室用装置A制取氧气的化学方程式。
-
(3) 图C装置是小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密),与装置B对比,装置C不仅能控制反应速度,还能。
-
(4) 用D装置收集氧气,氧气应该从(选填m或n)端通入。
-
(5) 用装置E进行CO2的部分性质实验,下列有关说法正确的是____。A . 通入的CO2可用浓硫酸干燥 B . 将干燥的紫色石蕊试纸放在d处,并与b处现象对比,可说明CO2能与水反应 C . e处容器中的高低两支燃着的蜡烛会同时熄灭 D . 用装置E可以节约药品并提高实验效率