探究二氧化碳的性质 知识点题库
|
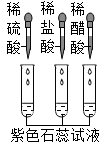
实验操作 |
| | | |
| 实验现象 | 紫色石蕊溶液变成红色 | 紫色干燥小纸花不变化 | 紫色石蕊溶液变成红色 | 红色溶液又变成紫色 |
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
-
(1) 由实验Ⅰ可得出的结论是;
-
(2) 小明认为不必做“向石蕊溶液中滴加蒸馏水”的实验,理由是;
-
(3) 综合实验I、Ⅱ、Ⅲ能得出的结论是;
-
(4) 写出实验Ⅳ中反应的化学方程式。

-
(1)
-
(2)
-
(3)
-
(4)
-
(5)
-
(6)
-
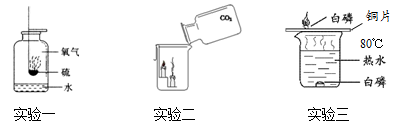
(1) 在实验一中,水的作用是;
-
(2) 由实验二可知,CO2具有的物理性质是;
-
(3) 在实验三中,铜片上的白磷燃烧,红磷不燃烧,由此能够得出燃烧的条件之一是。
-
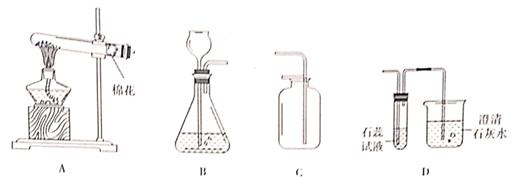
(1) 某实验室的仪器柜里有如图1所示的仪器:
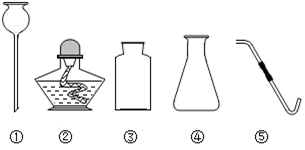
图1
仪器①的名称是,④的名称是,实验室用大理石和稀盐酸制备并收集二氧化碳时,不可能选择的仪器名称是。
-
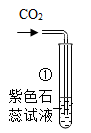
(2) 如图2是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图,请回答下列问题:
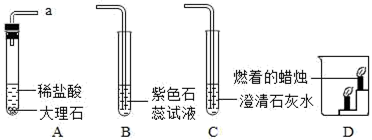
图2
①将A、B装置连接,观察到B的现象是,可验证二氧化碳的性质是(用方程式表示)。
②将A、C装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为:。
③用集气瓶集满一瓶二氧化碳气体,移开玻璃片,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象是,这些现象说明二氧化碳具有的物理性质是,化学性质是,。
-
(1) 加热高锰酸钾的方法制取氧气,所选择的发生装置是 (填字母序号);用C装置收集氧气,检验氧气收集满的方法是。
-
(2) 制取二氧化碳气体并验证其化学性质,把生成的二氧化碳通入D装置中,在试管里可观察到的现象是,烧杯中发生的化学反应方程式是。
-
(1) (实验记录与分析)
实验一
实验二
实验三
实验操作


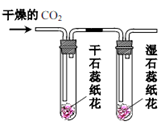
实验现象
蜡烛火焰
软塑料瓶变瘪程度较大的是(选填“甲”或“乙”)
干石蕊纸花不变色,湿石蕊纸花变红色
实验结论
①二氧化碳的密度比空气大;
②二氧化碳既不能燃烧,也不能支持燃烧
二氧化碳能与氢氧化钠发生反应
-
(2) (反思与拓展)
依据实验一的结论,写出二氧化碳的一条重要用途。
-
(3) 由实验二的结论分析得出:实验室中保存氢氧化钠要注意。
-
(4) 在设计上述三组对比实验时,都只改变一个影响因素,保持其他因素不变,这是运用了科学探究中的方法。
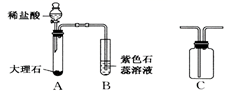
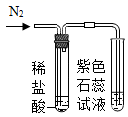
乙同学在实验时闻到制得的CO2有些刺激性气味,于是乙同学对气味的来源以及能使紫色石蕊试液变红的酸性物质产生了疑问。针对疑问,探究过程如下:
(查阅资料)大理石与稀盐酸反应产生热量;大理石无气味,稀盐酸有刺激性气味。
(猜想与假设)实验时制得的CO2中混有的刺激性气味来源于稀盐酸,刺激性气味气体的混入与温度、气流的速率有关。
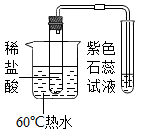
(进行实验)实验装置如下(两个实验中所用稀盐酸及紫色石蕊试液的体积、浓度均相同;夹持装置已略去)。
| 实验一 | 实验二 |
| | |
(解释与结论)
-
(1) 乙同学进行猜想与假设的依据是。
-
(2) 实验一、实验二均观察到紫色石蕊试液变红,由此说明猜想与假设正确。但是老师提示乙同学上述实验设计仍有不足,还应该补充一个实验,实验方案是。
-
(3) (反思与评价)
需在装置A、B之间增加装置C。装置C的作用是,装置C中药品应具有的性质是。
 B . 探究分子运动现象
B . 探究分子运动现象  D . 探究水的组成
D . 探究水的组成 
![]()
-
(1) 向澄清石灰水中通入CO2 , 观察到澄清石灰水变浑浊,产生该现象的原因是(用化学方程式表示)。
-
(2) 向紫色石蕊稀溶液(由紫色石蕊和水配制而成)中通入CO2 , 观察到紫色溶液变红。
①上述实验(填“能”或“不能”)得出“CO2可以和H2O发生反应”的结论,理由是。
②加热该红色溶液,可观察到的现象是。
-
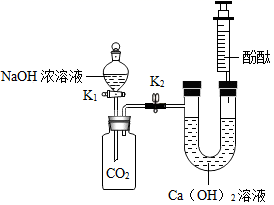
(1) 将足量的氢氧化钠浓溶液装入分液漏斗中,先打开阀门K1 , 广口瓶中发生反应的化学方程式为,待氢氧化钠溶液完全进入广口瓶之后立即关闭K1 , 充分反应后,打开止水夹K2 , 观察到的现象是。
-
(2) 同学们将实验后的废液倒入烧杯中并过滤,取滤液于试管中加入足量的稀盐酸,无气泡产生,说明废液中的溶质为(写出所有可能)。
-
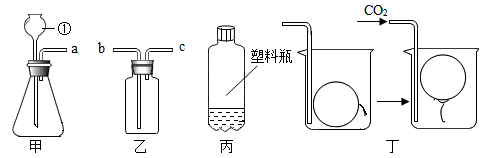
(1) 写出图中仪器①的名称:;
-
(2) 装置甲中应添加固体试剂的主要成分的化学式是;若用甲装置制氧气,发生反应的化学方程式为:。
-
(3) 用装置乙收集CO2时,导管口a应与(填“b”或“c”)相连;
-
(4) 用图丙所示的质地较软的塑料瓶收集满CO2 , 再倒入约1/3体积的紫色石蕊试液,立即旋紧瓶盖,振荡,观察到的现象是。
-
(5) 往图丁的烧杯内缓缓通入CO2 , 超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是。
A 测定空气中氧气的含量 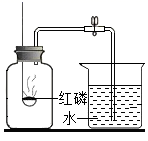 B 倾倒二氧化碳
B 倾倒二氧化碳 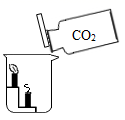 C 浓硫酸的稀释
C 浓硫酸的稀释 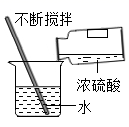
-
(1) A 实验中,导致实验结果偏小的原因可能是(写一点)。
-
(2) B 实验中,下层的蜡烛先熄灭上层的蜡烛后熄灭。说明 CO2的化学性质是。
-
(3) C 实验中,用玻璃棒搅拌的目的。
-
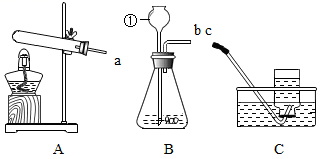
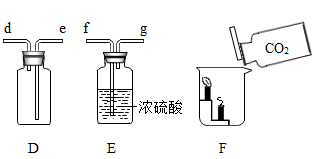
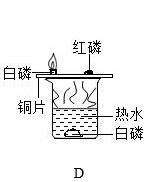
(1) 仪器①的名称为。
-
(2) 实验室选A装置用KMnO4制氧气,应进行的改进措施是,该反应的化学方程式为。
-
(3) 实验室制取干燥的二氧化碳气体,应选择的发生、干燥、收集装置的导管口正确连接顺序为(填小写字母)。
-
(4) 用F装置探究二氧化碳的性质,观察到蜡烛从下到上依次熄灭,说明二氧化碳具有的化学性质是。

-
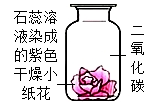
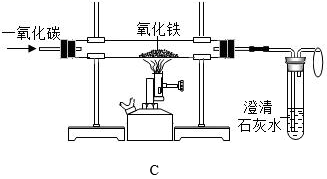
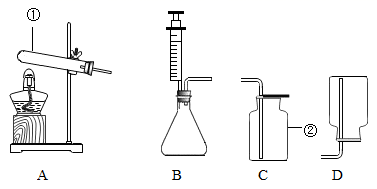
(1) A图烧杯中的下面蜡烛先熄灭,体现二氧化碳的物理性质是;
-
(2) B图中装满生石灰的塑料试剂瓶已经膨胀破裂,请用化学方程式解释这一现象;
-
(3) C图玻璃管中的现象是,反应的化学方程式是;
-
(4) D图能验证可燃物燃烧需要氧气的现象是;热水的作用、。
-
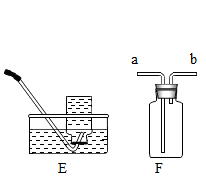
(1) 仪器的名称:①,②。
-
(2) 实验室利用H2O2制备并收集一瓶较纯净的氧气应选用的装置是(填字母);用高锰酸钾制O2则装置A需要改进的地方是。
-
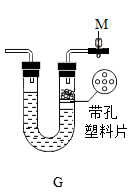
(3) 实验室现用G装置制取CO2气体,多孔塑料片上面放置石灰石,打开止水夹M,取下左侧的橡胶塞,向U型管内加入稀盐酸,U型管内发生反应的方程式是;一段时间后,关闭M后,观察到的现象是;该装置的优点是;若用F装置收集该气体,气体应从(填“a”或“b”)端通入。
-
(4) 用纯净的二氧化碳气体按如图装置进行实验,H中观察到的现象是;I中出现浑浊的反应原理是。
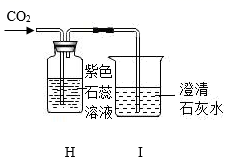
-
(1) 基础实验一:验证微粒不断运动
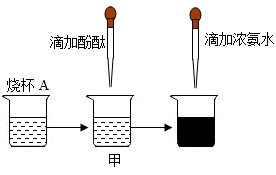
(实验1)向烧杯A中加入20mL蒸馏水,滴入2~3滴酚酞试液,得到溶液甲。向溶液甲中滴加1~2滴浓氨水,观察现象。这一实验现象说明了。
-
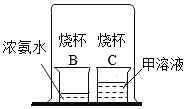
(2) (实验2)在烧杯C中重新配制甲溶液。在烧杯B中加入3~5mL浓氨水,用一个大烧杯把两个烧杯罩在一起,观察到,说明微粒是不断运动的。
-
(3) 基础实验二:验证质量守恒定律
(实验3)该实验观察到的现象是。


天平保持平衡。请从具体的反应物和生成物的角度分析天平平衡的原因是。
-
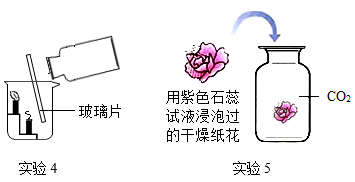
(4) 基础实验三:认识二氧化碳的性质
(实验4)根据实验4中的现象可以得出CO2具有的物理性质是。
-
(5) (实验5)实验5中干燥的紫色石蕊纸花(填“变”或“不变”)红。要证明CO2能与水反应,还需要进行的操作是。
 , 两个注射器内各装有85m1的水及40%的氢氧化钠溶液。连接好装置和压强传感器,同时迅速将注射器内的液体注入各自烧瓶并关闭活塞。实验过程中实时测得烧瓶内气压变化情况如图2所示。下列说法不正确的是( )
, 两个注射器内各装有85m1的水及40%的氢氧化钠溶液。连接好装置和压强传感器,同时迅速将注射器内的液体注入各自烧瓶并关闭活塞。实验过程中实时测得烧瓶内气压变化情况如图2所示。下列说法不正确的是( )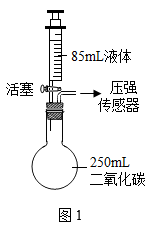

 能与水发生反应
B . 实验证明
能与水发生反应
B . 实验证明 能与
能与 溶液发生反应
C . 不改变装置药品的情况下,降低温度可以降低E点的位置
D . 振荡了烧瓶可能是导致曲线1中CD段气压“急速”减小的原因
溶液发生反应
C . 不改变装置药品的情况下,降低温度可以降低E点的位置
D . 振荡了烧瓶可能是导致曲线1中CD段气压“急速”减小的原因

已知:通常状况下,1体积的水约能溶解1体积二氧化碳。
-
(1) CO2与NaOH反应的化学方程式为。
-
(2) 步骤2中注射器活塞缓缓向左移动,最终停留在5mL刻度处。产生上述现象的原因是。
-
(1) 酸、碱、盐之间发生复分解反应的条件是。
-
(2) 在探究氢氧化钠的性质时,某化学小组设计了如图所示实验。
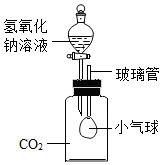
①当把分液漏斗中的氢氧化钠溶液滴入装有CO2的密闭瓶中后,可观察到的现象是,则证明CO2与氢氧化钠溶液发生了反应,写出该反应的化学方程式。
②反应后溶液中的溶质可能只含有碳酸钠。也可能还含有氢氧化钠,请设计实验检验溶质的成分,简要写出实验步骤现象和结论。(提示:碳酸钠溶液呈碱性)
-
(3) 除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作顺序为:i.加过量的NaOH溶液;ii.加过量的BaCl2溶液;iii.加过量的Na2CO3溶液;ⅳ.过滤;v.加适量的稀盐液。
①为什么加过量的NaOH溶液后。镁离子被彻底除去而钙离子不能被彻底除去。
②加入适量稀盐酸的目的是。
③最终得到的氯化钠固体质量比粗盐中含有的氯化钠质量大,原因是。
-
(4) 取20g部分变质的氢氧化钠样品,加水配制成溶液,然后向其中加入足量的氯化钡溶液,生成沉淀的质为19.7g。计算该样品中所含杂质的质量分数。
-
(1) 项目一 CO2气体的制取及净化
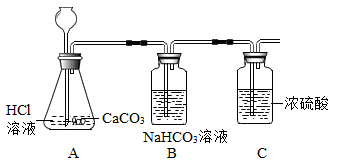
C装置中浓硫酸的作用是。
-
(2) B装置的作用是除去CO2气体中混有的少量HCl,该反应的化学方程式为。
-
(3) 项目二 不同收集方法所得CO2气体纯度的比较
取相同规格的集气瓶,先用向上排空气法收集两瓶CO2 , 并用燃着的木条验满后,倒扣在题39图所示的水槽中、再用排水集气法收集两瓶CO2 , 也倒扣在水槽中,依次编号为1、2、3、4。
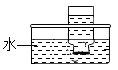
气体样本
1
2
3
4
收集方法
向上排空气法
排水法
2小时后进入的水量
13.7%
14%
15.3%
15.1%
24小时后进入的水量
54.7%
55.3%
94.2%
93.6%
通常情况下,1体积的水约能溶解1体积的CO2。能用排水法收集CO2的主要原因是。
-
(4) 与向上排空气法相比,用排水法收集CO2的优点是。
-
(5) 项目三 探究CO2与NaOH的可视化反应
实验操作
现象
①将少量水与Na2CO3粉末加入50mL乙醇中,搅拌
粉末基本没有溶解
②将少量水与NaOH粉末加入50mL乙醇中,搅拌
粉末消失
③向50mL乙醇中加入NaOH固体至其溶解达到饱和
/
④将CO2通入操作3中所得的NaOH乙醇饱和溶液中
?
预测实验操作4可能的实验现象:。