气体发生装置 知识点题库
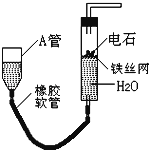
如图的实验装置可用于实验室中制取乙炔.请回答下列问题:
(1)图中,A管的作用是 ,制取乙炔的化学方程式为 .
(2)将制得的乙炔通入酸性KMnO4溶液中可观察到的现象是 ,这是由于乙炔发生了 反应.
(3)将制得的乙炔通入溴的四氯化碳溶液中可观察到的现象是 ,这是由于乙炔发生了 反应,写出该反应的化学方程式 .
(4) 为了安全,乙炔气体在点燃前应 ,乙炔燃烧时的现象是 .
A、水 B、过氧化氢溶液
C、高锰酸钾 D、.

-
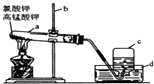
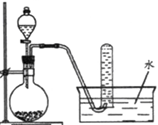
(1) 指出图中有标号的仪器名称:
a: b: c: d:
-
(2) 实验时应注意:①实验前要检查装置的性,其方法是.
②试管口要,其目的是.
③给试管加热时.④停止加热时,先要,然后.
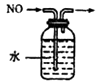 排水集气法收集NO
B .
排水集气法收集NO
B .  实验室制取氨气
C .
实验室制取氨气
C .  检查装置气密性
D .
检查装置气密性
D . 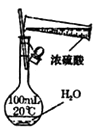 配制稀硫酸
配制稀硫酸
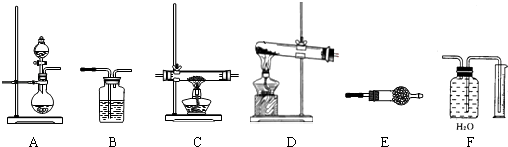
请回答下列问题:
-
(1) 按该方法制氨气时,应选用上述装置中的(填装置代码,下同)做氨气发生装置。写出Li3N和水反应制取氨气的化学方程式。
-
(2) 为检验氨气还原氧化铜反应后生成Cu、H2O、N2 , 氨气发生装置后应依次连接→C→→。(给出的装置可重复使用)
-
(3) 有资料提出:CuO被还原时,当黑色固体完全变为红时,不一定完全转化为Cu,可能还含有Cu2O.已知查阅到一离子反应方程式:Cu2O+2H+=Cu2++Cu+H2O.依据该信息,若要证明C处的红色固体中是否含有Cu2O,请设计实验: 。
-
(4) 甲同学认为利用上述实验设计改进后的装置还可测定Cu的相对原子质量,他是通过测定反应物CuO的质量和生成物H2O的质量来完成的。若实验测得完全反应的CuO和生成的H2O的质量分别为m(CuO)、m(H2O),则据此计算Cu的相对原子为。
 2CaSO4 +2Cl2↑+2H2O。该实验的发生装置为( )
2CaSO4 +2Cl2↑+2H2O。该实验的发生装置为( )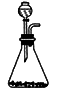 B .
B . 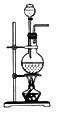 C .
C . 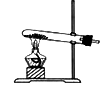 D .
D . 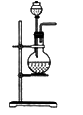
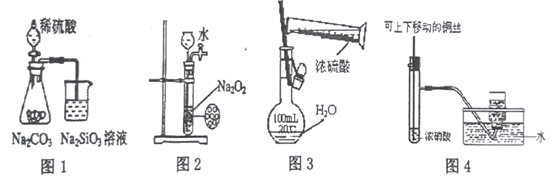
查阅资料得:实验室制取甲烷常用的方法为无水醋酸钠 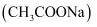 与氢氧化钠在二氧化锰作催化剂的条件下共热,产物中有少量的副产物丙酮
与氢氧化钠在二氧化锰作催化剂的条件下共热,产物中有少量的副产物丙酮 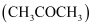 ,丙酮可与水混溶。
,丙酮可与水混溶。
-
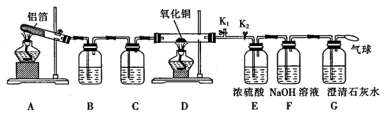
(1) 组装好仪器后,首先进行的操作是,实验中先点燃(填“A”或“D”)处酒精灯,此时
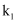 、
、  的状态为(填标号)。
的状态为(填标号)。 A.
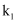 关闭、
关闭、  关闭 B.
关闭 B. 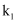 关闭、
关闭、  打开
打开C.
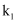 打开、
打开、  打开 D.
打开 D. 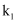 打开、
打开、  关闭
关闭 -
(2) 装置A中主要发生反应的化学方程式为,试管内壁加一层铝箔不仅能使药品受热均匀,还能。
-
(3) 装置B中盛装的试剂为。
-
(4) 实验过程中记录的实验数据如下:
实验前装置总质量/g
D
E
F
G
实验后装置总质量/g
180.0
277.8
311.5
301.0
实验前装置总质量/g
177.2
279.6
312.6
301.0
若装置D中的氧化铜全部被还原成铜,则气球中收集到的由D中反应产生的气体在标准状况下的体积为L,此条件下,装置D中发生反应的化学方程式为。
| A | B | C | D |
| | | | |
| 制取 CO2气体 | 过滤获得碳酸氢钠晶体 | 灼烧碳酸氢钠制取碳酸钠 | 蒸发浓缩氯化钠溶液 |
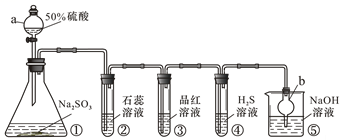
-
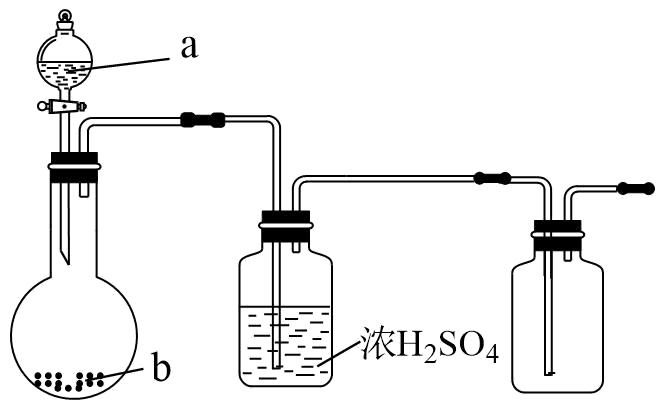
(1) 仪器a的名称是,仪器b的作用是,装置⑤中NaOH溶液的作用是。
-
(2) 装置②中的实验现象是。反应结束后,对装置③的试管加热,可观察到的现象是。
-
(3) 装置④中发生反应的化学方程式为,在该反应中SO2作剂。
-
(4) 已知本实验所用50%硫酸的密度约为1.39g/cm3 , 则其物质的量浓度为(计算结果保留两位有效数字)。用18.4mol/L的浓硫酸配制100mL50%的硫酸,需要用量筒量取mL浓硫酸;配制该溶液用到的基本仪器除容量瓶、量筒、烧杯、玻璃棒外,还有。下列操作会导致所配硫酸浓度偏高的是(填标号)。
A.稀释浓硫酸时,未冷却至室温即转入容量瓶进行定容
B.用量筒量取浓硫酸时俯视刻度线
C.定容时俯视容量瓶刻度线
D.转移溶液时未洗涤烧杯
-
(5) 若使用装置①并选用KMnO4和浓盐酸来制取Cl2 , 则装置①中发生反应的离子方程式为;将制得的Cl2依次通入装置②、③、④,其中实验现象与通入SO2不同的是装置。
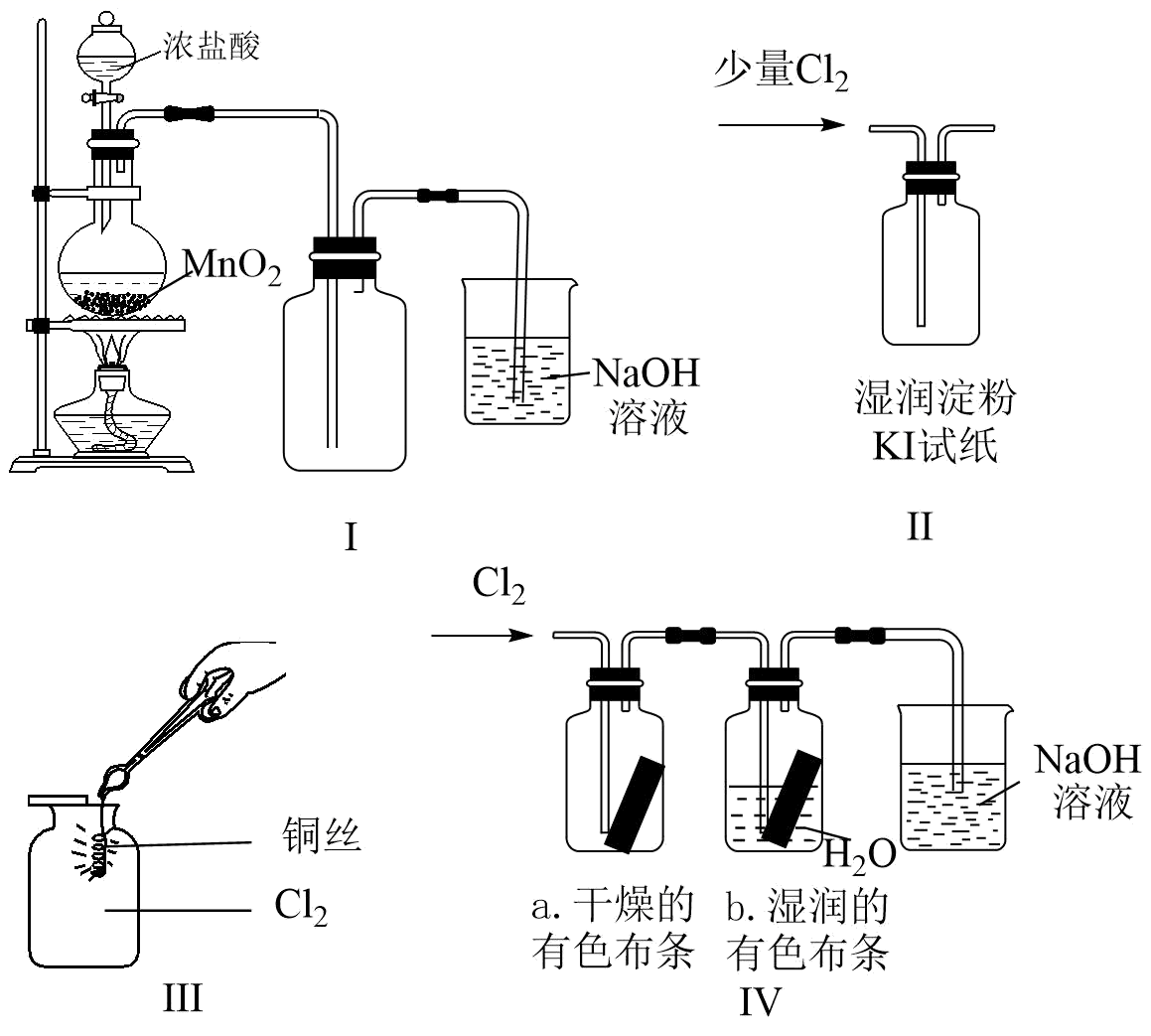
 过量,则浓盐酸可全部消耗完
B . 图Ⅱ:淀粉KI试纸变蓝
C . 图Ⅲ:产生白色的烟
D . 图Ⅳ:干燥的有色布条不褪色
过量,则浓盐酸可全部消耗完
B . 图Ⅱ:淀粉KI试纸变蓝
C . 图Ⅲ:产生白色的烟
D . 图Ⅳ:干燥的有色布条不褪色
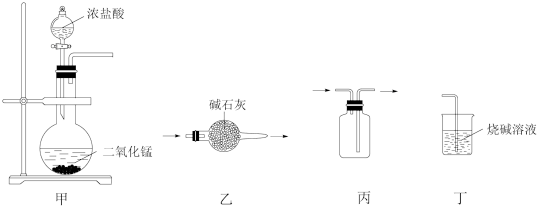
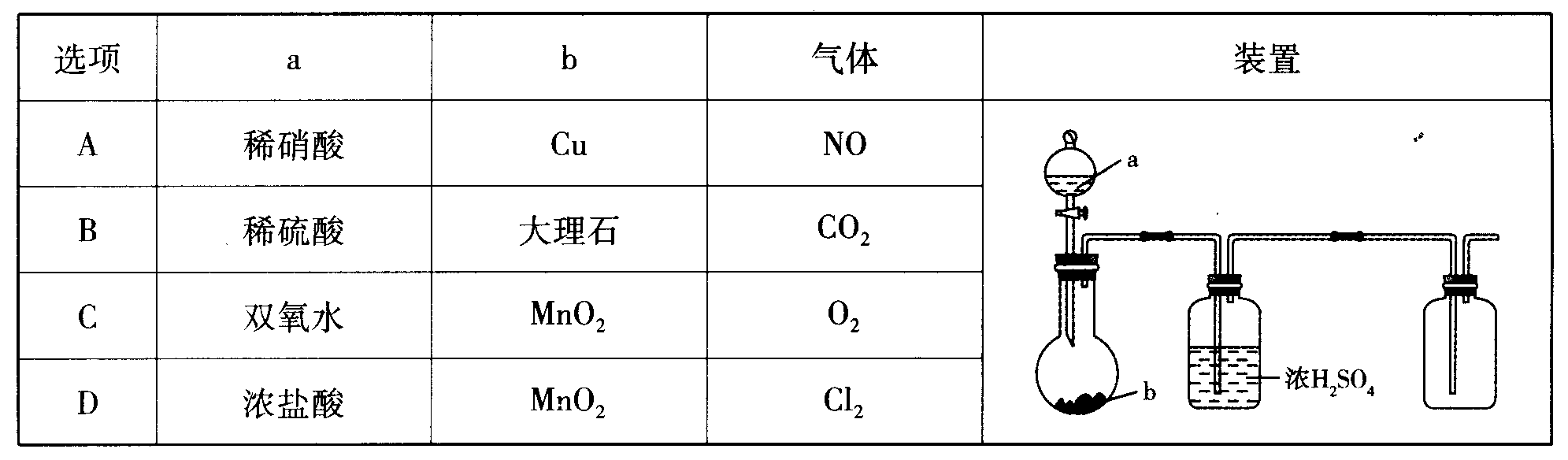
选项 | a | b | 气体 | 装置 |
A | 稀硝酸 | Cu | NO |
|
B | 稀硫酸 | 大理石 | CO2 | |
C | 浓氨水 | 生石灰 | NH3 | |
D | 浓硫酸 | Na2SO3 | SO2 |

| A | B | C | D |
| | | | |
| 蒸发浓缩制NaCl | 制备SO2气体 | 用KMnO4滴定Na2C2O4 | 观察铁的析氢腐蚀 |
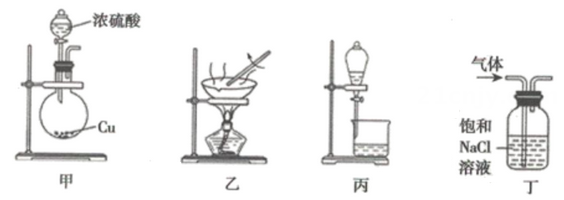
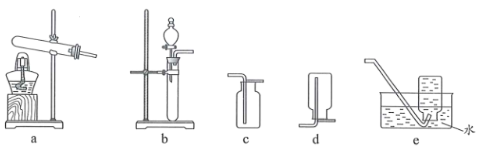
气体 | 试剂 | 制备装置 | 收集方法 | |
A |
|
| b | c |
B |
|
| b | e |
C |
|
| b | c |
D |
|
| a | d |
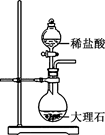
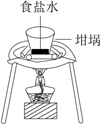




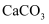 +稀
+稀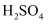

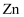 +稀
+稀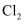
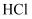 (浓)
(浓)




