电解质溶液的导电性 知识点
电解质溶液的导电性:电解质在溶液中发生电离,电离出自由移动的离子,当通电后,离子由于带电荷,发生定向移动,从而导电,其导电能力与离子浓度,及离子所带电荷的多少决定。
电解质溶液的导电性 知识点题库
下列图象正确的是( )
A . 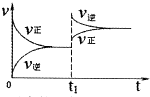 反应的正方向放热(t1时升温)
B .
反应的正方向放热(t1时升温)
B . 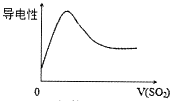 SO2气体通入氯水中
C .
SO2气体通入氯水中
C . 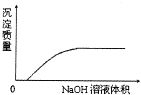 NaOH溶液滴加Ca(HCO3)2溶液中
D .
NaOH溶液滴加Ca(HCO3)2溶液中
D . 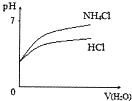 将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
 反应的正方向放热(t1时升温)
B .
反应的正方向放热(t1时升温)
B .  SO2气体通入氯水中
C .
SO2气体通入氯水中
C .  NaOH溶液滴加Ca(HCO3)2溶液中
D .
NaOH溶液滴加Ca(HCO3)2溶液中
D .  将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
下列物质的导电性能最差的是( )
A . 熔化的氢氧化钠
B . 0.1 mol/L盐酸
C . 0.1 mol/L醋酸
D . 氯化钾固体
电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2mol•L﹣1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )
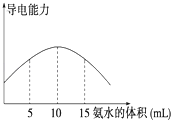
A . 0.5%
B . 1.5%
C . 0.1%
D . 1%
下列说法正确的是( )
A . 纯水导电性很差,所以水不是电解质
B . 判断某化合物是否为电解质,应看其在一定条件下能否电离
C . 酸、碱和盐类都属于电解质,其他化合物都不是电解质
D . NaCl和HCl都是电解质,所以它们熔融状态下都能导电
以下反应会导致溶液导电性减弱最明显的是( )
A . Na2SO4溶液加入BaCl2固体
B . Ba(OH)2溶液中加入CuSO4(少量)固体
C . NaOH溶液通入HCl
D . H2O中加入NaCl固体
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
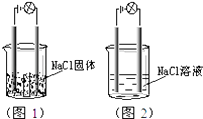
A . NaCl是非电解质
B . NaCl溶液是电解质
C . NaCl溶液中水电离出大量的离子
D . NaCl在水溶液中电离出了可以自由移动的离子
下列说法中不正确的是( )
A . 强酸、强碱、大多数盐、部分金属氧化物是强电解质,弱酸、弱碱都是弱电质
B . 电解质溶液导电性的强弱跟单位体积溶液里自由移动的离子多少有关
C . 硫酸钡难溶于水,所以硫酸钡属弱电解质
D . 纯净的强电解质在液态时,有的能导电有的不能导电
下列物质中,能够导电的电解质是( )
A . Cu
B . 熔融的MgCl2
C . 氢氧化钠溶液
D . 蔗糖
-
(1) 下列物质属于电解质的是;能导电的是;属于弱电解质的是(均填写序号)。
①醋酸溶液②乙醇③胆矾④熔融氯化钠⑤二氧化硫⑥氨水⑦硫酸钡⑧蔗糖⑨氢氧化铁⑩浓盐酸
-
(2) Cl2通入一定浓度NaOH溶液后生成了三种含氯化合物,其中n(NaClO) :n(NaClO3)= 5:1,写出Cl2 与NaOH溶液反应的化学方程式并用双线桥表示出电子转移的方向和数目:。
-
(3) 标准状况下4.48LCO2溶于100mL3.0mol/LNaOH溶液,所得产物成分是,物质的量为。
下列说法正确的是( )
A . 强电解质溶液的导电能力一定比弱电解质溶液强
B . 将NaOH和氨水各稀释一倍,两者的OH-浓度均减少到原来的1/2
C . 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍
D . 中和等体积、等物质的量浓度的盐酸和醋酸溶液,两者所需要的氢氧化钠一样多
现有物质①铜、②干冰、③盐酸、④液态硫酸、⑤蔗糖、⑥NaHSO4固体、⑦红褐色的氢氧化铁胶体、⑧熔融的NaCl、⑨冰水混合物
-
(1) 能导电的是;属于电解质的是。(填序号)
-
(2) 写出属于酸式盐的物质溶于水后的电离方程式:。
-
(3) 向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至Ba2+恰好完全沉淀,发生反应的离子方程式为;Ba2+恰好沉淀后继续滴加NaHSO4溶液时,发生反应的离子方程式为。
下列几种导电性变化图像,其中实验操作与图像序号相符的是( )
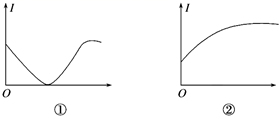
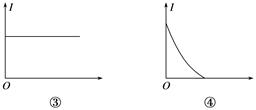
| 选项 | 实验操作 | 图像 |
| A | 向H2SO4溶液中加入等体积、等物质的量浓度的Ba(OH)2溶液 | ① |
| B | 向氨水中通入HCl直至过量 | ① |
| C | 向NaOH溶液中通入少量Cl2 | ③ |
| D | 向饱和石灰水中不断通入CO2 | ④ |
A . A
B . B
C . C
D . D
下列物质不能导电的是( )
A . 稀硫酸
B . 液态HCl
C . 熔融NaCl
D . 石墨棒
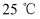 时,pH=2 的盐酸和醋酸各1mL分别加水稀释,pH 随溶液体积变化的曲线如图所示。下列说法正确的是( )
时,pH=2 的盐酸和醋酸各1mL分别加水稀释,pH 随溶液体积变化的曲线如图所示。下列说法正确的是( ) 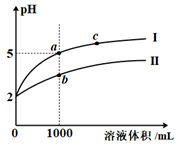
A . 曲线 I 代表醋酸的稀释过程
B . a 点溶液的导电性比 b 点溶液的导电性强
C . b 点水电离的 c(H+)比 c 点水电离的 c(H+)大
D . 将a、b 两点溶液加热至30℃,  变小
变小
 变小
变小
-
(1) I回答下列问题
现有以下物质:①NaCl晶体 ②SO2 ③液态醋酸 ④铜 ⑤固体 BaSO4 ⑥纯蔗糖(C12H22O11)
⑦酒精(C2H5OH) ⑧熔化的 KHSO4 ⑨氨水 ⑩液氮。
请回答下列问题。(填相应序号)
①以上物质能导电的是;
②以上物质属于非电解质的是;
③以上物质属于强电解质的是;
-
(2) II.A、B、C、D四种物分别是 HCl、NH3
 H2O、CH3COOH、NaOH中的一种。常温下进行下列实验:
H2O、CH3COOH、NaOH中的一种。常温下进行下列实验:
0.001mol/L的A溶液pH=3,则A是。
-
(3) B溶液和D溶液显碱性,等浓度两者pH关系B<D
① D是溶液。
② 用水稀释0.1mol/LB时,溶液中随着水量的增加而减小的是(填写序号)。
A.c(OH-) B.c(H+)
C.c(H+)与 c(OH-)的乘积 D.OH-的物质的量
-
(4) pH相同,等体积的两份溶液A和C,分别与不同质量的锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是(填写序号)。
①反应所需要的时间C>A ②开始反应时的速率A>C
③参加反应的锌的物质的量 A=C ④反应过程的平均速率C>A
⑤A溶液里有锌剩余 ⑥C溶液里有锌剩余
某化学兴趣小组进行导电性实验,按照图I连接好线路后发现灯泡不亮,按照图II连接好线路后发现灯泡亮了,由此得出的结论正确的是( )
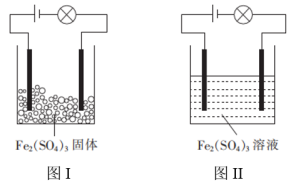
A . Fe2(SO4)3是非电解质
B . Fe2(SO4)3溶液是电解质
C . Fe2(SO4)3的电离方程式为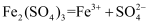 D . Fe2(SO4)3在水溶液中电离出了可以自由移动的离子
D . Fe2(SO4)3在水溶液中电离出了可以自由移动的离子
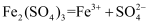 D . Fe2(SO4)3在水溶液中电离出了可以自由移动的离子
D . Fe2(SO4)3在水溶液中电离出了可以自由移动的离子
数字化实验是利用传感器和信息处理终端进行数据采集与分析的实验手段。下图是利用数字化实验测定光照氯水过程中得到的图像,该图像表示的意义是( )
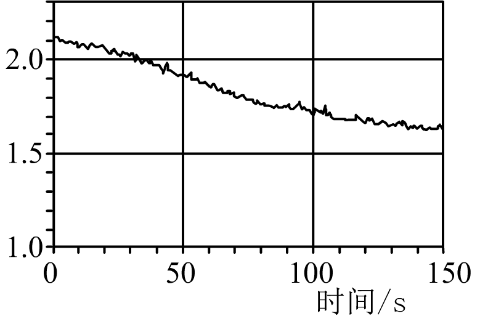
A . 氯离子浓度随时间的变化
B . 氧气体积分数随时间的变化
C . 氯水的pH随时间的变化
D . 氯水导电能力随时间的变化
下列说法正确的一组是( )
①Na2O、MgO、Al2O3均属于碱性氧化物
②已知氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离
③0.5mol/L所有一元酸中氢离子浓度都是0.5mol/L
④苏打、碱石灰、醋酸、小苏打均为电解质
⑤电解质溶液导电的原因是溶液中有自由移动的阴阳离子
⑥熔融的电解质都能导电
A . ①③⑤⑥
B . ②④⑤
C . ②⑤
D . ②⑤⑥
常温下,0.1 mol∙L−1下列溶液:①HCl、②H2SO4、③CH3COOH,导电能力强弱顺序是( )
A . ②>①>③
B . ①=②>③
C . ①>②>③
D . ①=②=③
某温度下,将体积分别为 且
且 相同的
相同的 和
和 加水稀释,溶液中
加水稀释,溶液中 随着加水量的变化曲线如图所示:
随着加水量的变化曲线如图所示:
 且
且 相同的
相同的 和
和 加水稀释,溶液中
加水稀释,溶液中 随着加水量的变化曲线如图所示:
随着加水量的变化曲线如图所示: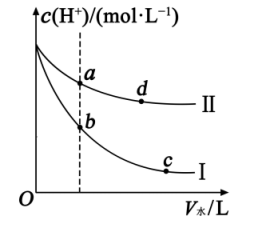
回答下列问题
-
(1) Ⅱ表示的是(填化学式)的变化曲线.
-
(2) a点溶液的导电性b点溶液的导电性(填“<”“>”或“=”,下同),a点酸的电离程度d点酸的电离程度,a点对应酸的总浓度b点对应酸的总浓度.
-
(3) 取等体积的b、c两点对应的溶液与相同浓度的
 溶液反应,消耗
溶液反应,消耗 溶液的体积关系是
溶液的体积关系是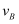
 (填“<”“>”或“=”).
(填“<”“>”或“=”).
最近更新



