探究碳酸钠与碳酸氢钠的性质 知识点题库
选项 | 实验 | 现象 | 结论 |
A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
B | 将铜粉加1.0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
D | 向苏打和小苏打溶液中分别加入过量盐酸 | 均冒气泡 | 两者均能与盐酸反应 |

选项 | X | Y | Z |
A | NH3 | NO2 | HNO3 |
B | SiO2 | Na2SiO3 | H2SiO3 |
C | Al2O3 | NaAlO2 | Al(OH)3 |
D | CO2 | Na2CO3 | NaHCO3 |
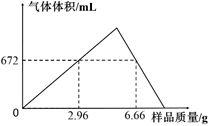
-
(1) 样品中n(Na2CO3) : n(NaHCO3)=。
-
(2) 盐酸的物质的量浓度c(HCl)=mol·L−1。
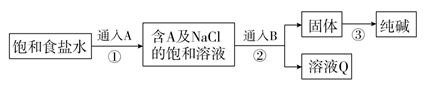
则下列说法中正确的是( )
①金属钠投入FeCl3溶液中
②少量Ca(OH)2投入过量NaHCO3溶液中
③向饱和Na2CO3溶液中通入足量CO2
④向AlCl3溶液中滴入NaHCO3溶液
⑤过量NaOH溶液和明矾溶液混合
| 选项 | 化学性质 | 实际应用 |
| A | ClO2具有强氧化性 | 自来水消毒杀菌 |
| B | SO2具有还原性 | 用作漂白剂 |
| C | NaHCO3受热分解并且生成气体 | 焙制糕点 |
| D | Al(OH)3分解吸收大量热量并有H2O生成 | 阻燃胶合板 |
| 选项 | 实验 | 操作、现象及结论 |
| A | 探究Na2O2与水反应 | 将2mL水滴入盛有1g过氧化钠试管中,立即把带火星木条伸入试管,木条复燃,证明有氧气产生 |
| B | 鉴别NaHCO3与Na2CO3 | 取少许两种物质,加入几滴水,插入温度计,温度降低的是Na2CO3 |
| C | 检验Fe3+中是否含Fe2+ | 向溶液中加入KSCN溶液,变红则含Fe2+ |
| D | 检验溶液中是否含Cl- | 向某溶液中加入盐酸酸化的AgNO3溶液,有白色沉淀,说明含有Cl- |
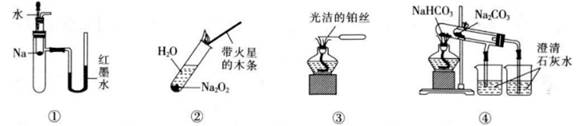
化学性质 | 实际应用 | |
A | Fe粉具有还原性 | 可用于防止食品氧化变质 |
B | NaHCO3受热分解有气体生成 | 可用作焙制糕点的膨松剂 |
C | 二氧化硅导光能力强 | 可作太阳能电池板 |
D | BaSO4难溶于水和酸 | 可在医疗上用作“钡餐”透视 |



