海带成分中碘的检验 知识点题库
从海带提取碘的实验中,下列仪器选用不正确的是( )
A . 用托盘天平称取3.0克海带
B . 在坩埚中灼烧海带
C . 用分液漏斗分离海带灰和水溶液
D . 在烧杯中用H2O2氧化I﹣
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图:
海藻  海藻灰
海藻灰  悬浊液
悬浊液  含I﹣的溶液
含I﹣的溶液  X
X  Y→晶态碘
Y→晶态碘
某化学兴趣小组将上述流程②③设计成如图所示:

【提示:已知②中发生反应的化学方程式为Cl2+2KI═2KCl+I2】
回答下列问题:
-
(1) 写出提取过程①③中实验操作名称:①,③.
根据提示,②中反应 (填“是”或“不是”)氧化还原反应.
-
(2) 四氯化碳本身是色、密度比水的液体,它(填“是”或“不是”)电解质.F中下层液体的颜色为色,上层液体中溶质的主要成分为.
-
(3) 从F中将两层液体进一步分离的操作是.
-
(4) 在萃取过程中,使用到的(除烧杯和铁架台外)实验仪器有(填序号).
A.试管 B.长颈漏斗 C.分液漏斗 D.蒸发皿 E.酒精.
某化学课外小组用海带为原料制取少量碘水,已知:海带中碘元素以I﹣形式存在.提取碘的原理是“在酸性条件下用H2O2将I﹣氧化为碘单质”.
反应后,再进行以下实验步骤:
①把盛有溶液的分液漏斗放在铁架台的铁圈中;②把50mL碘水和15mL CCl4加入分液漏斗中,盖好玻璃塞,倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞把分液漏斗放正;③检验分液漏斗活塞和上口的玻璃塞是否漏液;④旋开分液漏斗活塞,用烧杯接收下层液体;⑤从分液漏斗上口倒出上层液体;⑥将漏斗上口的玻璃塞打开或使塞上凹槽对准漏斗口上的小孔;⑦静置,分层.
就此实验,完成下列填空:
-
(1) 写出用海带制取单质碘的离子方程式:.
-
(2) 正确的实验操作步骤顺序为:→→→⑥→⑦→④→⑤.
-
(3) 第②步操作的名称是,
-
(4) 第②步中,可以用来替代CCl4的溶剂有:A . 汽油 B . 酒精 C . 苯 D . 水.
已知单质碘受热易升华。从海带中提取碘的实验过程中涉及下列操作正确的是( )
A .  B .
B . 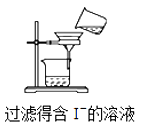 C .
C . 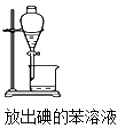 D .
D . 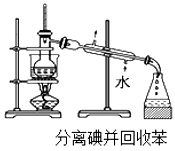
 B .
B .  C .
C .  D .
D . 
溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径如下图所示,则下列有关叙述正确的是( )

A . 碘元素在海水中也有游离态存在
B . 在提取的过程中用的氧化剂可以是H2O2
C . 操作  是结晶或重结晶
D . 操作
是结晶或重结晶
D . 操作  是提纯,常用蒸馏或分馏
是提纯,常用蒸馏或分馏
海带中提取碘的实验中,下列物质分离方法未涉及的是( )
A . 灼烧
B . 萃取
C . 过滤
D . 蒸发
物质分离、提纯的常用装置如图所示,根据题意选择合适的装置填入相应位置。

-
(1) 我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写到:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”所用的是装置(填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
-
(2) 《本草衍义》中对精制砒霜过程的叙述为:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下重如乳,尖长者为胜,平短者次之。”文中涉及的操作方法所用是装置。
-
(3) 海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
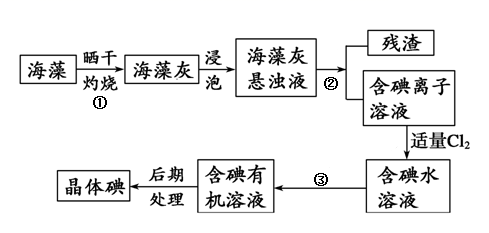
其中分离步骤①、②、③所用分别为:装置、装置、装置。
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行以下实验:
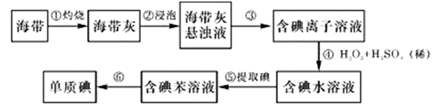
请填写下列空白:
-
(1) 步骤③的操作名称是,碘离子在酸性环境中也能被氧气氧化,请写出相关离子方程式是。
-
(2) 步骤⑤中萃取剂也可用四氯化碳的理由是,该步骤所用主要玻璃仪器的名称是。
海带中含有丰富的碘。为了从海中提取碘,某研究性学习小姐设计并进行了以下实验,请填写下列空白:
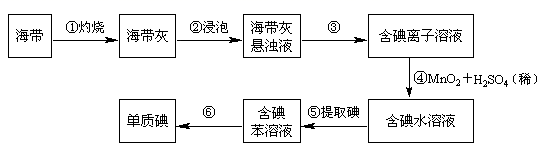
-
(1) 步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___(用标号字母填写在空白处)。A . 烧杯 B . 坩埚 C . 表面皿 D . 泥三角 E . 酒精灯 F . 干燥器
-
(2) 步骤③的实验操作名称是,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是。
-
(3) 步骤④反应的离子方程式是。
-
(4) 步骤⑤中,某学生选择用苯来提取碘的理由是、。
-
(5) 请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:。
为了从海带浸取液中提取碘,某同学设计了如下实验方案:
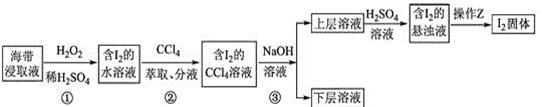
下列说法正确的是( )
A . ①中反应的离子方程式:2I− + H2O2=I2 + 2OH−
B . ②中分液时含I2的CCl4溶液从分液漏斗上口倒出
C . ③中得到的上层溶液中含有I−
D . 操作Z的名称是加热
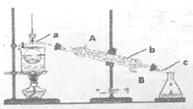
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
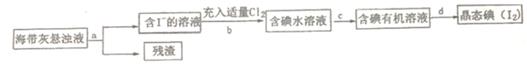
-
(1) 指出提取碘的过程中有关的实验操作名称:a,c。
-
(2) 操作c需要的仪器是,所用的有机试剂可以是CCl4 , 简述选择理由;最后碘的CCl4溶液是通过获得(填“漏斗上口”或“漏斗下口”)。
-
(3) 从含碘的有机溶液中提取碘和回收有机溶液CCl4 , 还需要经过,观察下图所示实验装置,指出仪器名称b,冷却水从进入(填A或B),最后碘留在里。(填仪器名称)
下列所示物质的制备方法合理的是( )
A . 实验室从海带中提取单质碘:取样→灼烧→溶解→过滤→萃取→蒸馏
B . 以海水为原料制得精盐,再电解精盐的水溶液制取钠
C . 以铁矿石、焦炭、空气、石灰石等为原料,通过反应产生的 CO 在高温下还原铁矿石制得铁
D . 从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝
化学小组用海带浸取原液制备碘,甲、乙两种实验方案如下:
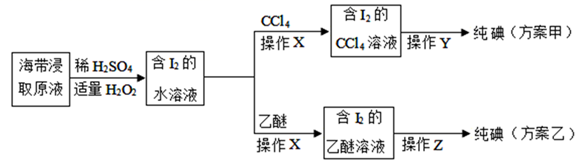
已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5℃,微溶于水,CCl4沸点76.8℃。进行操作Y时,没有观察到碘的升华。
请回答:
-
(1) 写出实验操作名称:操作X;操作Y。
-
(2) 下列说法错误的是________A . 加入过氧化氢的目的是将碘离子氧化为单质碘 B . 碘在乙醚中的溶解度比在水中的溶解度大且乙醚在水中的溶解度小,可用乙醚萃取碘 C . 若用40mLCCl4萃取,甲直接用40mL CCl4萃取1次,乙萃取4次,每次用10mL CCl4 , 甲的萃取效率高 D . 操作Z时,不需要加沸石等来防止暴沸
-
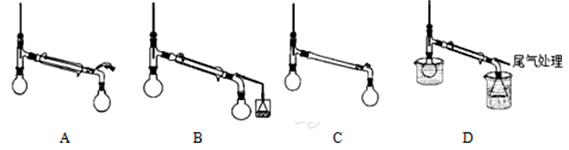
(3) 从下面的装置中选择操作Z的最合适的装置图
-
(4) 请选择合适的编号,按正确的操作顺序完成用乙醚萃取碘的实验(假设只放气一次):c→a→倒入溶液和萃取剂→ →→→→f→a→d→使下层液体慢慢流出→c→上层液体从上口倒出。
a.打开上口玻璃塞; b.塞上上口玻璃塞; c.关闭旋塞;d.打开旋塞;e.倒转分液漏斗振摇; f.放在铁圈上静置;g.手持静置。
-
(5) 从碘的四氯化碳溶液中获取碘,还可以用以下流程:

请解释氢氧化钠溶液的作用。
海带中含有碘元素,某校研究性学习小组设计了如下实验步骤来提取碘:①通足量氯气②将海带烧成灰,向灰中加水搅拌③加CCl4振荡④过滤⑤用分液漏斗分液。合理的操作顺序为( )
A . ①→③→⑤→②→④
B . ②→①→③→④→⑤
C . ②→④→①→③→⑤
D . ③→①→②→⑤→④
下列实验操作正确且能达到实验目的的是( )
A . 灼烧碎海带 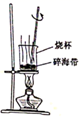 B . 混合浓硫酸和乙醇
B . 混合浓硫酸和乙醇  C . 吸收氨气防止倒吸
C . 吸收氨气防止倒吸  D . 乙酸乙酯的制取
D . 乙酸乙酯的制取 
 B . 混合浓硫酸和乙醇
B . 混合浓硫酸和乙醇  C . 吸收氨气防止倒吸
C . 吸收氨气防止倒吸  D . 乙酸乙酯的制取
D . 乙酸乙酯的制取 
溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径和装置如下图所示,下列有关叙述正确的是( )
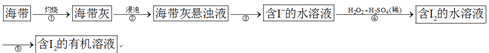

A . 完成步骤①需要装置Ⅲ
B . 完成步骤③需要装置Ⅰ
C . 步骤⑤中溶剂可选用酒精或苯
D . 完成步骤②和④需要装置Ⅳ
海带、紫菜等藻类植物含有丰富的碘元素。某化学实验小组同学从海带中提取碘并计算海带中的碘元素含量,进行以下实验:
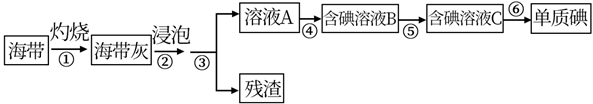 已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
回答下列问题:
-
(1) 在进行步骤①之前,他们称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入中灼烧至海带完全成灰烬。乙同学认为甲的操作不合理,其理由是。
-
(2) 海带提碘的一系列操作中需要过滤的步骤是。
-
(3) 步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,发现未明显变化,再加入氯水后溶液颜色变蓝,此反应的离子方程式是;乙同学认为使用稀硫酸和
 溶液能更有利于提取碘,其理由。
溶液能更有利于提取碘,其理由。
-
(4) 步骤⑤中用分液漏斗得到碘的四氯化碳溶液,其操作顺序是(填写字母)。
a.
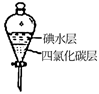 b.
b. 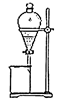
c.
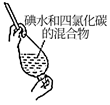 d.
d. 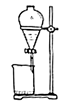
请设计一种简单的实验方法,检验提取碘后的水溶液中还含有单质碘:。
-
(5) 将得到的单质碘,干燥、称量,其质量为n g:则海带中碘元素的含量为。
下列说法正确的是( )
A . 向3mL95%乙醇溶液中加入几颗CoCl2·6H2O晶体,充分溶解后再滴加蒸馏水至溶液恰好呈粉红色,用酒精灯加热该试管,溶液呈蓝色
B . 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
C . 实验室从海带中提取碘单质的方法是:取干海带→浸泡→ 过滤→氧化→结晶→ 过滤
D . 制备KNO3晶体实验中,为得到较大颗粒晶体,可将热KNO3溶液快速冷却
下列说法不正确的是( )
A . 在“镀锌铁皮锌镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,可以判断锌镀层已反应完全
B . 在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干
C . 在“海带中碘元素提取”实验中,为保证Iˉ 完全氧化为I2 , 加入的氧化剂(H2O2或新制氯水)均应过量
D . 在“反应条件对化学平衡的影响”实验中,氯化钴呈蓝紫色时,表示仍具有吸水能力
小铭同学为了从海带浸取液中提取碘,设计了如图所示实验方案:

-
(1) 实验中操作Z的名称是,在步骤②萃取操作时需用到一种重要的玻璃仪器,其名称是
-
(2) 步骤①发生的离子反应方程式为;
-
(3) 步骤②用于提取碘的物质还可以是____A . 乙醇 B . 苯 C . 乙酸 D . 葡萄糖
-
(4) 步骤③可通过反萃取法得到单质碘。向含碘的CCl4溶液中加入浓
 溶液,得到含
溶液,得到含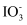 的溶液,反应的离子方程式为。
的溶液,反应的离子方程式为。
最近更新



