氮气的化学性质 知识点
氮气的化学性质:氮气的氧化性和还原性,氧化性常表现在如氮气和氢气的反应,氮气和金属镁的反应。还原性常表现在氮气和氧气的反应。
氮气的化学性质 知识点题库
甲、乙、丙、丁四种物质,甲、乙、丙含同一种元素.下列各组物质可按下图转化的是( )
① | ② | ③ | ④ | |
甲 | C | N2 | S | Fe |
丙 | CO2 | NO2 | SO3 | Fe(NO3)3 |
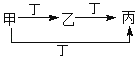
A . ①②
B . ②③
C . ①④
D . ③④
下列物质之间的转化都能一步实现的是( )
A . Si→SiO2→H2SiO3→Na2SiO3
B . Al→Al2O3→Al(OH)3→NaAl(OH)4
C . N2→NH3→NO→NO2→HNO3→NO2
D . S→SO3→H2SO4→SO2→Na2SO3→Na2SO4
在常温常压下,下列各组气体不能共存的是( )
A . SO2与O2
B . NO2与NO
C . O2与N2
D . NO与O2
氮元素的氢化物在工业生产和国防建设中都有广泛应用,回答下列问题:
-
(1) 氮气的结构式为,氮的氢化物除了氨气,还有一种在常温下呈液态的肼,分子式为N2H4 , 请写出肼的电子式;
-
(2) NH3与NaClO反应可得到肼,该反应的化学方程式为;
-
(3) 肼在碱性环境下可以形成肼一空气燃料电池,肼被氧化为N2 , 该电池负极的反应式为,每生成56g N2要消耗标准状况下的氧气的体积为 L.
常温下能发生反应的一组气体是( )
A . NH3、HCl
B . N2、O2
C . H2、CO
D . CO2、O2
下列解释事实的方程式错误的是( )
A . 用湿润的淀粉—KI试纸检验Cl2: Cl2+2I-= 2 Cl-+I2
B . 工业固氮:N2+3H2 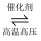 2NH3
C . 用FeCl3溶液腐蚀铜质线路板:2Fe3++Cu=2Fe2++Cu2+
D . 铝热法焊接铁轨:2Fe+Al2O3
2NH3
C . 用FeCl3溶液腐蚀铜质线路板:2Fe3++Cu=2Fe2++Cu2+
D . 铝热法焊接铁轨:2Fe+Al2O3  2Al+Fe2O3
2Al+Fe2O3
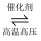 2NH3
C . 用FeCl3溶液腐蚀铜质线路板:2Fe3++Cu=2Fe2++Cu2+
D . 铝热法焊接铁轨:2Fe+Al2O3
2NH3
C . 用FeCl3溶液腐蚀铜质线路板:2Fe3++Cu=2Fe2++Cu2+
D . 铝热法焊接铁轨:2Fe+Al2O3  2Al+Fe2O3
2Al+Fe2O3
有关物质用途的叙述中,不正确是( )
A . 石膏可用于制造模型
B . 氮气可用于保鲜水果
C . 明矾可用做消毒剂
D . 碳酸氢铵可用做肥料
氮元素是地球大气中含量最多的元素,请完成下列有关问题:
-
(1) 写出氮元素的原子结构示意图:。
-
(2) 通常情况下,氮气性质不活泼,其原因是__________。A . 氮分子是双原子分子 B . 氮元素的非金属性很强 C . 氮原子的半径较小 D . 破坏氮分子中的化学键很难
-
(3) N2的电子式:,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是。
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
-
(4) 氨气的电子式:。
-
(5) 实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式。
-
(6) 下面是实验室制取氨气的装置和选用的试剂,其中不正确是。
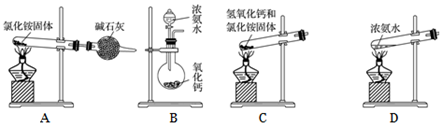
-
(7) 收集氨气应使用法,要得到干燥的氨气可选用做干燥剂。
-
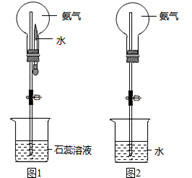
(8) 用圆底烧瓶收集干燥的氨气,用图1装置进行喷泉实验,挤压滴管的胶头时,可以得到红色喷泉,原因(用方程式表示) 。
-
(9) 如果只提供如图2的装置,请说明引发喷泉的方法。
-
(10) NH4NO3是常用的铵态氮肥,在施用时若受热会释放出而降低肥效。检验NH4+的方法是。
不能由单质直接与O2反应生成的氧化物是( )
A . Fe3O4
B . NO2
C . SO2
D . CuO
中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理如下图所示。下列关于该过程的说法不正确的是( )
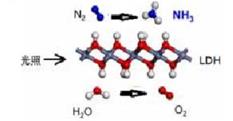
A . 该过程属于氮的固定
B . LDH降低了反应的活化能
C . 氧化剂和还原剂的物质的量之比为1:3
D . 该过程证明,N2和H2合成NH3的反应是放热反应
关于氮气的性质的说法中,错误的是( )
A . 氮在自然界中既以游离态存在又以化合态存在
B . 通常情况下,氮气性质很不活泼
C . 在反应3Mg+N2=Mg3N2中N2作氧化剂
D . 放电条件下可与氧气反应生成二氧化氮
下列物质间的转化不能通过一步反应实现的是( )
A . S→SO2
B . H2S→S
C . SiO2→H2SiO3
D . N2→Mg3N2
下列装置图的使用说法正确的是( )
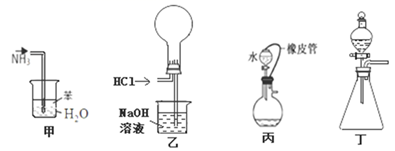
A . 甲装置吸收 NH3制氨水
B . 乙装置收集并吸收多余的 HCl
C . 丙装置打开分液漏斗活塞即可检验其气密性
D . 丁装置中,向酸性高锰酸钾溶液中滴加草酸溶液,溶液的紫红色逐渐褪去
常温常压下用LDH(一种固体催化剂)合成NH3的原理如图所示。下列说法错误的是( )
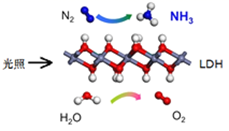
A . 原料气N2可通过分离液态空气获得
B . 该过程将太阳能转化成为化学能
C . 该过程中,只涉及共价键的断裂与生成
D . 发生反应的n(N2):n(H2O)=1:2
下列关于氮气说法正确的是( )
A . 氮气的电子式 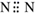 B . 将大气中游离态的氮转化为含氮的固体化合物的过程叫做氮的固定
C . 豆科植物根瘤菌将氮气转化成氨,实现了自然固氮
D . 氮气化学性质稳定,可以用作镁合金熔化时的保护气
B . 将大气中游离态的氮转化为含氮的固体化合物的过程叫做氮的固定
C . 豆科植物根瘤菌将氮气转化成氨,实现了自然固氮
D . 氮气化学性质稳定,可以用作镁合金熔化时的保护气
下列说法不正确的是( )
A .  能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的
能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的  D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
 能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的
能导致“光化学烟雾”的形成
B . 浓硝酸可用铝槽车运输
C . 石灰石在高温下可用于消除燃煤烟气中的  D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
D . 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在
磁性材料在很多领域具有应用前景,其制备过程如下(各步均在  氛围中进行):
氛围中进行): ①称取  ,配成
,配成  溶液,转移至恒压滴液漏斗中。
溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入  溶液。
溶液。
③持续磁力搅拌,将  溶液以
溶液以 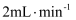 的速度全部滴入三颈烧瓶中,100℃下回流3h。
的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在  干燥。
干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:
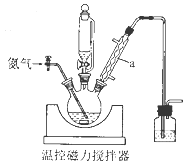
回答下列问题:
-
(1) 仪器a的名称是;使用恒压滴液漏斗的原因是。
-
(2) 实验室制取
 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为,对应的装置为(填标号)。
有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为,对应的装置为(填标号)。 可供选择的试剂:
 、
、 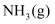 、
、  、
、  、饱和
、饱和  、饱和
、饱和 
可供选择的发生装置(净化装置略去):

-
(3) 三颈烧瓶中反应生成了Fe和
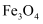 ,离子方程式为。
,离子方程式为。
-
(4) 为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。A . 采用适宜的滴液速度 B . 用盐酸代替KOH溶液,抑制
 水解
C . 在空气氛围中制备
D . 选择适宜的焙烧温度
水解
C . 在空气氛围中制备
D . 选择适宜的焙烧温度
-
(5) 步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为;使用乙醇洗涤的目的是。
-
(6) 该实验所得磁性材料的产率为(保留3位有效数字)。
下列有关物质的性质与用途,具有对应关系的是( )
A . 二氧化硫具有强还原性,可用作漂白纸张
B . 氧化镁熔点高,可用作电解冶炼镁的原料
C . 氨气分解时吸热,可用作制冷剂
D . 氮气常温下化学性质稳定,可用作粮食保护气
下列说法错误的是( )
A . 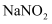 能使酸性
能使酸性 溶液变为绿色
B . 铁在纯氧中燃烧生成
溶液变为绿色
B . 铁在纯氧中燃烧生成 C .
C . 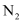 在放电或高温条件下与
在放电或高温条件下与 生成
生成 D . 乙烯能使溴的四氯化碳溶液褪色
D . 乙烯能使溴的四氯化碳溶液褪色
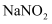 能使酸性
能使酸性 溶液变为绿色
B . 铁在纯氧中燃烧生成
溶液变为绿色
B . 铁在纯氧中燃烧生成 C .
C . 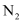 在放电或高温条件下与
在放电或高温条件下与 生成
生成 D . 乙烯能使溴的四氯化碳溶液褪色
D . 乙烯能使溴的四氯化碳溶液褪色
自然界中氮的循环如图所示。下列说法错误的是( )
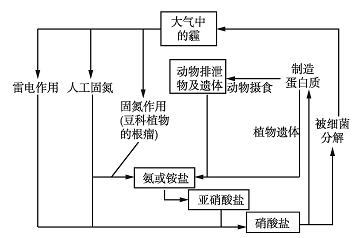
A . 工业合成氨属于人工固氮
B . 在雷电作用下N2与O2发生化学反应
C . 在氮的循环过程中不涉及氧化还原反应
D . 含氮无机物与含氮有机物可相互转化
最近更新



