铵盐 知识点
铵盐 知识点题库
(1)二氧化碳通入氨水的过程中,先有 晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体.
(2)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠.实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③ ;④加入盐酸调pH;⑤加入 ;⑥过滤;⑦灼烧,冷却,称重.
(3)上述步骤②中所加入的试剂为 、 .
(4)上述步骤④中加盐酸调pH的目的是
氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵.主要的工艺流程如图所示:

-
(1) 吸收塔中发生反应的化学方程式是
-
(2) 有数据表明,吸收塔中溶液的pH在5.5~6.0之间,生产效率较高.当控制一定流量的尾气时,调节溶液的pH的简便方法
-
(1) 取少量肥料配成溶液,加入(填化学式)溶液至沉淀不再产生,(填实验操作名称);
-
(2) 取(1)中生成的溶液于试管,滴加(填化学式)溶液,若产生,则说明该肥料含有氯化铵;反之,则无.
(NaHCO3的制备)
反应原理:NH3+NaCl+CO2+H2O=NH4Cl+NaHCO3↓
反应装置:

-
(1) 启普发生器中发生的离子反应方程式为,如果上述装置中导管被堵塞,启普发生器中观察到的现象是。
-
(2) 仪器3中盛装的试剂是;已知常温,NaCl的溶解度为35.9g,仪器4中含氨的饱和食盐水的配制方法是将20.0mL浓氨水与8.0gNaCl混合振荡过滤,试推测过滤除去的物质为。
-
(3) 观察仪器4中CO2流速的方法是,仪器5中试剂的作用是。
-
(4) 反应结束后,对仪器4进行冷却并趁冷过滤其中的悬浊液,“趁冷”的目的是。
-
(5) (Na2CO3的制备)
将(4)所得固体转移至蒸发皿中加热得到Na2CO3;请设计简单实验证明NaHCO3固体已分解完全。
-
(6) (NH4Cl的制备)
向(4)所得母液中加入两种物质并降温,NH4Cl会逐步结晶析出,所加物质的名称是,过滤NH4Cl晶体后的滤液可以再次循环使用。
-
(1) 已知NH3、PH3常温下都是气体,试比较二者沸点高低:NH3PH3 , 并解释原因
-
(2) NH4I与PH4I结构相似加热条件下,用化合物PH4I和烧碱反应制取PH3的化学方程式
 NF3+3NH4F.Ka(HF)=6.3×10−4 , Kb(NH3·H2O)=1.8×10−5。下列关于氨和铵盐的说法正确的是( )
NF3+3NH4F.Ka(HF)=6.3×10−4 , Kb(NH3·H2O)=1.8×10−5。下列关于氨和铵盐的说法正确的是( )
 中氮原子的轨道杂化类型不同
C . 25 ℃,0.1 mol·L−1 NH4F溶液的pH<7
D . 25 ℃,NH3与HNO3反应生成N2和H2O
中氮原子的轨道杂化类型不同
C . 25 ℃,0.1 mol·L−1 NH4F溶液的pH<7
D . 25 ℃,NH3与HNO3反应生成N2和H2O
酸化反应:MgCl2·6NH3+6HCl=MgCl2+6NH4Cl;
碳化反应:MgCl2+2NH4HCO3=Mg(HCO3)2+2NH4Cl;
热解反应:Mg(HCO3)2→xMgCO3·yMg(OH)2·zH2O↓+CO2↑(未配平)。
下列说法正确的是( )
 ,其中a为一个可持续鼓入空气的橡皮球。
,其中a为一个可持续鼓入空气的橡皮球。 
请回答下列问题:
-
(1) 写出装置B中发生反应的化学方程式 。
-
(2) 已知 1mol
 与液态水反应生成
与液态水反应生成  溶液和NO气体放出热量46kJ写出该反应的热化学方程式;该反应是一个可逆反应,欲要提高
溶液和NO气体放出热量46kJ写出该反应的热化学方程式;该反应是一个可逆反应,欲要提高  的转化率,可采取的措施是 (填序号)。
的转化率,可采取的措施是 (填序号)。 A.升高温度 B.降低温度 C.增大压强 D.减小压强
-
(3) 装置C中浓硫酸的作用是。
-
(4) 实验结束后,关闭止水夹b、c,将装置D浸入冰水中,现象是。
-
(5) 实验室制取
 也可以用浓氨水与生石灰反应,反应的化学方程式为。
也可以用浓氨水与生石灰反应,反应的化学方程式为。
-
(6) 干燥管中的碱石灰用于干燥
 ,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下:
,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下: 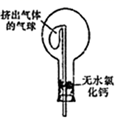
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是,由此该同学得出结论:不能用
 代替碱石灰来干燥氨气。
代替碱石灰来干燥氨气。
物质 用途 A.浓硫酸——————a.作干燥剂 B.二氧化硫 b.作红色颜料 C.碳酸氢铵 c.作漂白剂 D.氧化铁 d.作膨松剂 E.氨气 e.作制冷剂 |



