硫酸盐 知识点
硫酸盐 知识点题库
-
(1) Na2S2O3溶液与足量氯水反应的离子方程式为.(S元素被氧化为SO
 )
)
-
(2) 硫代硫酸钠(Na2S2O3)露置在空气中易氧化变质,其可能的变质后生成物如下:
假设一:
假设二:只有Na2SO4固体
假设三:
-
(3) 现有一瓶Na2S2O3固体,可能混有Na2SO4固体.设计实验验证该假设,写出实验步骤、预期现象和结论.限选试剂:1mol•L﹣1 H2SO4、1mol•L﹣1HNO3、1mol•L﹣1HCl、1mol•L﹣1NaOH、0.1mol•L﹣1BaCl2、0.01mol•L﹣1KMnO4、蒸馏水.
实验步骤
预期现象和结论
步骤1:取少量固体于试管中,加蒸馏水溶解.
步骤2:
步骤3:
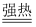 3Na2SO4 + Na2S
C . 固体产物中加入稀盐酸可能有淡黄色沉淀产生
D . 加入BaCl2溶液,出现白色沉淀,则能确定产物中有Na2SO4
3Na2SO4 + Na2S
C . 固体产物中加入稀盐酸可能有淡黄色沉淀产生
D . 加入BaCl2溶液,出现白色沉淀,则能确定产物中有Na2SO4
请回答:
-
(1) D中溶质的化学式,H2O2的电子式。
-
(2) A和水反应的化学方程式。
-
(3) B→E的离子方程式。
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X一定是浓盐酸 |
| B | 用玻璃棒蘸取溶液Y进行焰色反应实验 | 火焰呈黄色 | 溶液Y中一定含Na+ |
| C | 向Fe(NO3)2溶液中滴加硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| D | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品中含有SO42- |
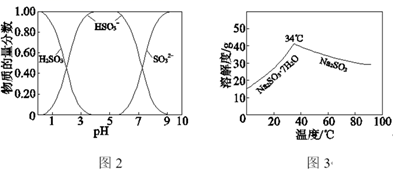
已知:H2SO3、HSO3−、SO32−在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。
-
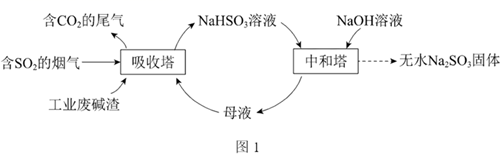
(1) Na2CO3溶液显碱性,用离子方程式解释其原因:。
-
(2) 吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为。
②已知下列反应:
SO2(g)+2OH−(aq)=SO32−(aq)+H2O(l)ΔH1=−164.3kJ·mol−1
CO2(g)+2OH−(aq)=CO32−(aq)+H2O(l)ΔH2=−109.4kJ·mol−1
2HSO3−(aq)=SO32−(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol−1
吸收塔中Na2CO3溶液吸收SO2生成HSO3−的热化学方程式是。
③吸收塔中的温度不宜过高,可能的原因是(写出1种即可)。
-
(3) 制备无水Na2SO3
①中和塔中反应的离子方程式为。
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度,同时还要,以防止Na2SO3氧化。

-
(1) Ba(OH)2溶液的物质的量浓度为mol•L-1。
-
(2) 该混合溶液MgSO4和(NH 4)2SO4物质的量之比为。
-
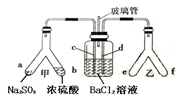
(1) I.甲组同学设计的实验装置如图所示,回答下列问题:
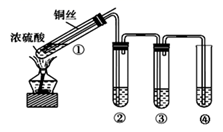
试管①中反应的化学方程式为。
-
(2) 试管②中的品红溶液褪色。欲证明品红褪色的原因是SO2 , 需要补充的实验操作及应出现的实验现象是。
-
(3) 试管③中的溴水褪色,体现SO2具有 性(填“还原”、“氧化”或“漂白”)。
-
(4) 试管④中的试剂是NaOH溶液,反应的离子方程式为。
-
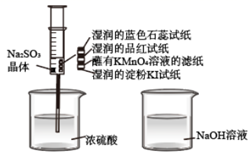
(5) II.乙组同学设计的实验装置如下图所示,回答下列问题:

已知:BaSO3是白色难溶于水的物质,但可溶于盐酸。
⑤中反应的化学方程式为 。
-
(6) ⑥中产生了不溶于盐酸的白色沉淀,该沉淀是。
-
(7) 经过分析,乙组同学认为装置中的空气是出现白色沉淀的原因。他们在不改变实验装置的情况下增加了某操作过程,证实了这种猜测是正确的。他们的操作及实验现象是。
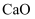 可以减少酸雨的形成及温室气体的排放
D . 中国华为自主研发的
可以减少酸雨的形成及温室气体的排放
D . 中国华为自主研发的 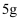 芯片巴龙5000的主要材料是硅
芯片巴龙5000的主要材料是硅
任务I:从以下试剂中选择合适的试剂实现 →
→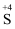 的转化。
的转化。
试剂清单:①浓H2SO4②稀H2SO4③酸性KMnO4溶液④品红⑤Cu
-
(1) 写出实现转化的化学方程式。
-
(2) 设计实验证明实现了该转化(写出操作和现象)。
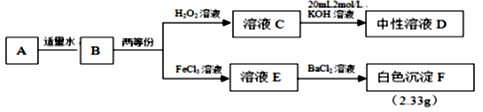
任务II:实现硫元素在不同价态之间的转化。
 溶液
溶液 SO2
SO2 Na2SO3溶液
Na2SO3溶液 Na2SO4溶液
Na2SO4溶液 -
(3) 欲制备Na2S2O3 , 从氧化还原角度分析,合理的是____(填字母)。A . Na2S+S B . Na2SO3+S C . Na2SO3+Na2SO4 D . SO2+Na2SO4
-
(4) 转化Ⅱ中加入的物质可以是。(填物质类别)
-
(5) 转化Ⅲ可以通入氧气来实现,写出相应离子方程式。