高一化学上册单元测试免费试卷完整版
| 1. 选择题 | 详细信息 |
|
下列关于胶体的叙述不正确的是( ) A. 用饱和氯化铁溶液滴入沸水中至红褐色,得到的氢氧化铁胶体带正电荷 B. 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 C. 用丁达尔效应可区别氯化钠溶液和氢氧化铁胶体 D. 氢氧化铁胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
|
| 2. 选择题 | 详细信息 |
|
氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C A.上述反应中,N2是还原剂,Al2O3是氧化剂 B.上述反应中,每生成1mol AlN需转移3mol电子 C.AlN中氮元素的化合价为+3 D.AlN的摩尔质量为41g |
|
| 3. 选择题 | 详细信息 |
|
城市环保部门为了使生活垃圾得到合理利用,实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶等属于( ) A.无机物 B.有机物 C.盐类 D.非金属 |
|
| 4. 选择题 | 详细信息 |
|
R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( ) A.R2+>X2+>Z2+>Y2+ B.X2+>R2+>Y2+>Z2+ C.Y2+>Z2+>R2+>X2+ D.Z2+>X2+>R2+>Y2+ |
|
| 5. 选择题 | 详细信息 |
|
关于反应2Na+2H2O=2NaOH+H2↑的说法错误的是( ) A.属于氧化还原反应 B.金属钠发生还原反应 C.水发生还原反应 D.H2是还原产物 |
|
| 6. 选择题 | 详细信息 |
|
单质钛(Ti)抗腐蚀能力强(放在大海中几周后仍金光闪闪),机械强度高,有“未来金属”之称。又因用它制的“骨头”置入人体后可以在上面长肉,所以又有“亲生物金属”之美誉。工业上常用硫酸分解钛铁矿(FeTiO3,铁为+2价)的方法来制取TiO2,再由TiO2制金属钛。主要反应有: ①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O ②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4 ③H2TiO3 ④TiO2+2C+2Cl2 ⑤TiCl4+2Mg 上述反应中,属于氧化还原反应的有( ) A.①② B.①⑤ C.③④ D.④⑤ |
|
| 7. 选择题 | 详细信息 |
|
下列关于硫酸铜溶液和泥水的说法中不正确的是 A. 都是混合物 B. 都是分散系 C. 分散剂相同 D. 分散质粒子相同 |
|
| 8. 选择题 | 详细信息 |
|
某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为11∶1,则Cl2与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( ) A.1∶3 B.4∶3 C.2∶1 D.3∶1 |
|
| 9. 选择题 | 详细信息 |
|
下列粒子不具有还原性的是 A. H2 B. Fe2+ C. I- D. H+ |
|
| 10. 选择题 | 详细信息 |
|
经分析可知某物质中含有两种元素,此物质不可能是( ) A.化合物 B.纯净物 C.混合物 D.单质 |
|
| 11. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A.元素的存在形态只有两种:化合态和游离态 B.同一元素,呈化合态时,其化合价一定比游离态时高 C.有多少种元素就有多少种物质 D.同一元素在不同的物质中的价态一定不同 |
|
| 12. 选择题 | 详细信息 |
|
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150 mL 4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( ) A. 0.21 mol B. 0.25 mol C. 0.3 mol D. 0.35 mol |
|
| 13. 选择题 | 详细信息 |
|
与铁、石灰水、石灰石都能发生离子反应的是( ) A.盐酸 B.CO2 C.O2 D.Na2CO3溶液 |
|
| 14. 选择题 | 详细信息 |
|
为了除去硫酸亚铁溶液中的硫酸铁和硫酸铜,最好选用的试剂是( ) A. 烧碱溶液 B. 浓氨水 C. 铁粉 D. 硫酸 |
|
| 15. 选择题 | 详细信息 | |||||||||||||||
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可采取多种分类方法。下列各组归类不合理的是( )
|
||||||||||||||||
| 16. 填空题 | 详细信息 |
|
有下列物质:①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4•5H2O晶体。请用序号填空: (1)上述状态下可导电的是________。 (2)属于电解质的是________。 (3)属于非电解质的是________。 (4)上述状态下的电解质不能导电的是________。 |
|
| 17. 填空题 | 详细信息 |
| 根据酸、碱、盐、氧化物之间的转化关系,写出硫酸分别与镁及其化合物(类别不同)反应生成硫酸镁的化学方程式。①_________________________________;②_________________________________;③_________________________________;④_________________________________。 | |
| 18. 填空题 | 详细信息 | ||||
|
从氧化还原反应的角度看,在制备下列三种气体时,盐酸起什么作用:(填序号) (1)制备H2Zn+2HCl=ZnCl2+H2↑ 盐酸起______作用 (2)制备Cl2MnO2+4HCl =MnCl2+Cl2↑+2H2O 盐酸起______作用 (3)制备CO2CaCO3+2HCl=CaCl2+CO2↑+H2O 盐酸起______作用
|
|||||
| 19. 综合题 | 详细信息 |
|
亚铁盐、铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用,现用铁屑与硫酸反应制备硫酸亚铁。 已知:①4Fe2++O2+4H+===4Fe3++2H2O ②硫酸亚铁在水中的溶解度如下图: 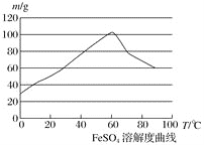 (1)首先,将铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。此步骤中,分离出液体的方法通常不用过滤,使用的操作是____________(填写操作名称)。 (2)向处理过的铁屑中加入适量的硫酸,在一定温度下使其反应到不再产生气体,趁热过滤,得硫酸亚铁溶液。 ①硫酸浓度应选择(填字母序号)__________; A.浓硫酸 B.10 moL·L-1硫酸 C.3 moL·L-1硫酸 D.任意浓度硫酸 ②温度宜控制在________,加热的同时需适当补充水,原因是___________________; ③反应中应保持 (3)亚铁盐在空气中易被氧化,但形成复盐可稳定存在,如“摩尔盐”,即(NH4)2SO4·FeSO4·6H2O(硫酸亚铁铵),就是在硫酸亚铁溶液中加入少量稀硫酸溶液,再加入饱和硫酸铵溶液,经过_______、_______、_______、_______等一系列操作后所得。 |
|
| 20. 填空题 | 详细信息 |
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下: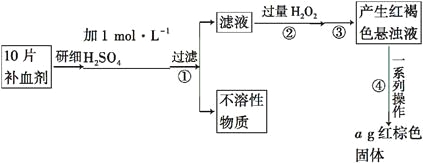 请回答下列问题: (1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加____,该过程的现象为__________________________________________________。 (2)步骤②加入过量H2O2的目的是___________________________________。 (3)步骤③中反应的离子方程式是__________________________________。 (4)步骤④中一系列处理的操作步骤:过滤、____________、灼烧、______、称量。 (5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为____g。 |
|
| 21. 填空题 | 详细信息 |
|
实验室里迅速制备少量氯气可利用如下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应不需加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。 (1)该反应中,氧化剂是________,还原剂是________。 (2)当参加反应的氧化剂的物质的量是1mol时,被氧化的还原剂的物质的量是________,产生的氯气在标准状况下的体积为________,电子转移数目为________。 (3)氯化氢在该反应过程中表现出的化学性质有________。 A 酸性B 还原性C 氧化性D 挥发性 |
|
| 22. 计算题 | 详细信息 |
| 在2 L硫酸铜和硫酸铁的混合溶液中,加入30 g铁粉,最后得到2 L 0.25 mol·L-1的硫酸亚铁溶液及26 g固体沉淀物。分别求原混合溶液中硫酸铁和硫酸铜的物质的量浓度。 | |
| 23. 计算题 | 详细信息 |
|
已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。 (1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。 (2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。 |
|
| 24. 计算题 | 详细信息 |
|
医学上经常用硫酸亚铁糖衣片给这种贫血病人补铁。现取20粒糖衣片,质量为10g,溶于40g水中,向所配溶液中滴加氢氧化钠溶液至略过量过滤、洗涤、干燥,然后进行灼烧到固体质量不再发生改变,质量为0.8g。试计算: (1)该糖衣片中硫酸亚铁的质量分数______。 (2)1粒糖衣片中含铁元素的质量______。 |
|
最近更新



