九年级化学上学期中考模拟完整试卷(2019年福建)
| 1. 选择题 | 详细信息 |
|
我国是历史悠久的文明古国。下列古代工艺不属于化学变化的是 A. 稻草造纸 B. 纺纱织布 C. 冶炼金属 D. 火药爆炸 |
|
| 2. 选择题 | 详细信息 |
|
糖醋鱼是百姓喜爱的家常菜。制作时用到的下列原料,富含蛋白质的是 A. 草鱼 B. 白糖 C. 淀粉 D. 植物油 |
|
| 3. 选择题 | 详细信息 |
|
俗话说“雷雨发庄稼”。雷雨天,氮气经一系列变化后,转化为农作物所需的肥料,该肥料属于 A. 钾肥 B. 磷肥 C. 复合肥 D. 氮肥 |
|
| 4. 选择题 | 详细信息 |
|
下列物质的用途中利用其物理性质的是 A. 天然气作燃料 B. 小苏打用于烘焙面包 C. 干冰实施人工增雨 D. 氮气用于粮食保护气 |
|
| 5. 选择题 | 详细信息 |
|
下列图示的实验操作中正确的是 A. 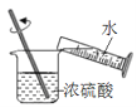 稀释浓硫酸 稀释浓硫酸B. 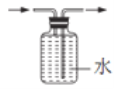 收集O2 收集O2C.  验证:可燃物燃烧需要与O2接触且温度达到着火点 验证:可燃物燃烧需要与O2接触且温度达到着火点D. 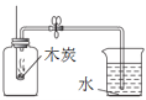 测定空气中O2的体积分数 测定空气中O2的体积分数 |
|
| 6. 选择题 | 详细信息 |
|
化学上把同种元素组成的不同单质互称为同素异形体。下列各组物质互为同素异形体的是 A. 液氧和氧气 B. CO和CO2 C. 金刚石和石墨 D. 冰和干冰 |
|
| 7. 选择题 | 详细信息 |
复方冬青油软膏有强力镇痛作用。其有效成分的分子模型如图。下列说法中错误的是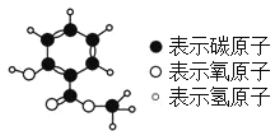 A. 该物质属于有机物 B. 该物质的化学式为C8H8O3 C. 该物质完全燃烧生成CO2和H2O D. 该物质分子中氢、氧原子的质量比为8∶3 |
|
| 8. 选择题 | 详细信息 |
某反应的微观示意图如下,下列说法正确的是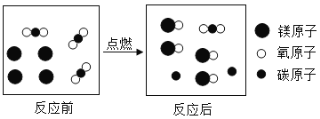 A. 图中反应的基本类型是置换反应 B. 反应前后元素的种类及化合价均不变 C. 反应涉及到的物质中, D. 参加反应的 |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
下列根据实验操作所得出的现象和结论均正确的是
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图甲、图乙所示。将图甲与图乙的阴影部分进行叠加,发现两者基本重合。下列有关分析错误的是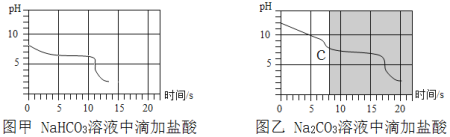 A. 图甲涉及反应的化学方程式为NaHCO3 + HCl = NaCl + H2O + CO2↑ B. 实验中所使用的NaHCO3溶液的碱性比Na2CO3溶液弱 C. 实验中碳酸氢钠、碳酸钠溶液完全反应,消耗的盐酸一样多 D. 图乙中c点对应溶液的溶质含有NaHCO3 |
|
| 11. 填空题 | 详细信息 |
|
2019年4月,中国海军建军70周年,盛大的阅兵仪式彰显大国风采。 (1)军舰外壳材料为合金钢,具有极佳的抗压性、延展性和焊接性。合金钢是______(填序号)。 a.合成材料 b.复合材料 c.无机材料 (2)制造国产航母的升降机需要用到铝合金。用石墨作电极电解氧化铝,在阴极区得到铝,阳极区得到氧气。反应过程中,______能转化为化学能。在电解过程中阳极区的石墨易消耗的原因是______(用化学方程式表示)。 (3)航母的螺旋桨由铜合金制造。铜合金比纯铜的硬度______(填“大”或“小”),铜比铁在海水中耐腐蚀的原因是______。 |
|
| 12. 填空题 | 详细信息 |
如图A是氟原子的结构示意图,B、C是钙、氟元素在元素周期表中的信息。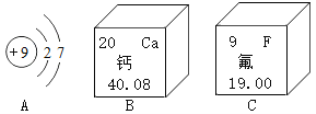 (1)氟元素的质子数为______。 (2)A粒子在化学反应中容易______(填“得到”或“失去”)电子形成离子。氟元素与钙元素组成的化合物的化学式为______。 (3)金(Au)位列元素周期表中79号。 ①俗话说“真金不怕火炼”。这反映出黄金的化学性质______。 ②“愚人金”(铜与锌的合金)的外观与黄金非常相似。下列可用于区分“愚人金”和黄金的试剂有______。 a.稀盐酸 b.食盐水 c.硝酸银溶液 ③黄金可溶解于王水(浓盐酸和浓硝酸按一定比例混合而成的溶液)。已知王水中氮、氯元素的原子个数比为1:3,则王水中HNO3和HCl的质量比为______(填最简整数比)。 |
|
| 13. 填空题 | 详细信息 |
|
水和溶液在生产生活中起着十分重要的作用。 (1)“直饮水机”可将自来水净化为饮用水,其内部使用的活性炭主要起______作用。实验室常用______方法降低水的硬度。 (2)C1O2是饮用水常用的消毒剂。制取C1O2的反应如下:C12+2NaC1O2=2C1O2+2X,则X的化学式为______。 (3)食盐水能导电是由于食盐溶于水形成______。 (4)如图是甲、乙两种不含结晶水的固体物质的溶解度曲线。 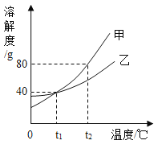 ①t1℃时,甲物质的溶解度是_____g。 ②t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是_____ (填“甲”或“乙”)物质的饱和溶液。 ③t2℃时,将一瓶溶质质量分数为10%的乙溶液,蒸发掉60 g水后,溶质质量分数变为20%,则原溶液中溶质的质量为_____g。 |
|
| 14. 流程题 | 详细信息 |
氯碱工业生产中,以氯化钠为主要化工原料来生产烧碱。下图为某工厂的一种生产流程: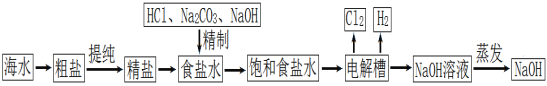 (1)从“海水→粗盐→精盐”的过程中,不涉及到的实验操作是______。 a.过滤 b.蒸发 c.洗气 d.溶解 (2)“精制”过程中加入的NaOH可除去MgCl2,写出该反应的化学方程式______。 (3)“电解槽”中,发生反应的化学方程式为______。 (4)氯碱工业的产品中常含有Na2CO3,其原因是______。 |
|
| 15. 实验探究题 | 详细信息 |
试剂A、B、C是Na2CO3溶液、稀盐酸、Ca(OH)2溶液中的一种。某同学进行如图所示的实验,观察到试管①中无明显现象,试管②中溶液变浑浊。实验结束后,该同学把试管①、②中的物质全部倒入烧杯中,发现溶液变澄清,并有气泡冒出。请回答: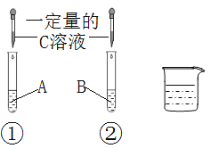 (1)A是______,B的溶质是______(填俗名)。 (2)写出烧杯中溶液变澄清的反应化学方程式:______。 (3)烧杯中所得溶液的溶质可能是______(填序号)。 a. NaCl、Na2CO3 b. NaCl、CaCl2、HCl c. NaCl、CaCl2 d. NaCl、CaCl2、Na2CO3 |
|
| 16. 实验探究题 | 详细信息 |
化学小组利用下图装置,多次连续进行氧气的制取和性质的实验。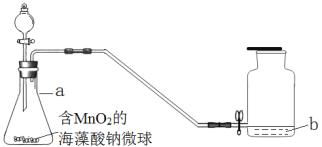 (1)a的仪器名称是______。 (2)该装置制取氧气时,发生反应的化学方程式为______,收集氧气的方法是______。 (3)该实验中,用含MnO2的海藻酸钠微球比直接使用MnO2的优点是______。 (4)进行氧气的性质实验时,实验不同,集气瓶中盛放的物质b不同。 ①铁丝燃烧,b为水,其作用是______。 ②硫粉燃烧,b为氢氧化钠溶液,其作用是______。 ③蜡烛燃烧,b为______,可以验证蜡烛中含有碳元素。 |
|
| 17. 科学探究题 | 详细信息 | ||||||||||||||||||||||
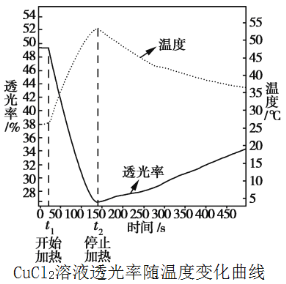
化学小组进行如图所示实验:将稀盐酸、稀硫酸分别加入到装有少量氧化铜粉末的试管甲、乙中,微热,观察到黑色固体完全溶解,试管甲中的溶液显绿色,试管乙中的溶液显蓝色。激发了他们的兴趣,进行如下探究活动。 (1)写出氧化铜与稀盐酸反应的化学方程式______。 探究一:为什么CuCl2溶液显绿色而CuSO4溶液显蓝色? (查阅资料) 氯化铜溶液与硝酸银溶液反应的化学方程式为:CuCl2 + 2AgNO3 = 2AgCl↓ + Cu(NO3)2 (猜想与假设)①硫酸铜溶液显蓝色与硫酸根离子有关; ②氯化铜溶液显绿色与氯离子有关。 (实验1) (2)取少量氧化铜粉末于试管中,加入一定量的稀硝酸,加热,观察到黑色固体完全溶解,溶液显______色,说明硫酸铜溶液显蓝色与硫酸根离子无关,与铜离子有关。 (实验2) (3)小组的操作:取试管乙中的溶液滴加一定量的______,观察到溶液由蓝色变绿色,则猜想②成立。 (4)请你再设计一个实验证明猜想②成立。实验方案:取试管甲中的溶液,______(请简述实验操作与现象)。 探究二:氯化铜溶液显绿色是否与溶液的浓度有关。 (实验3) 步骤Ⅰ. 用托盘天平称取无水氯化铜固体5.0 g置于小烧杯中; 步骤Ⅱ. 往小烧杯中加入一定量的蒸馏水,搅拌,观察溶液的颜色并记录。 室温下的实验现象及数据记录如下表:
|
|||||||||||||||||||||||
| 18. 计算题 | 详细信息 |
|
化学在防治环境污染方面起着重要作用。某发电厂用石灰石浆吸收燃煤废气中二氧化硫,反应原理为:2CaCO3 + 2SO2 + O2 = 2CaSO4 + 2CO2。原料使用的碳酸钙粉末价格是400元/吨,处理过程中回收的硫酸钙价格是700元/吨。 (1)若该厂每天可回收2.72 t硫酸钙,则可处理的二氧化硫质量是多少?_____ (2)回收硫酸钙的价值______(填“大于”、“等于”或“小于”)原料碳酸钙粉末的价值。 |
|
最近更新