广西武宣县第二中学高一化学上册期末考试考题同步训练
| 1. 选择题 | 详细信息 |
|
下列说法正确的是 A. 氧化还原反应的本质是元素化合价的升降 B. 氧化还原反应一定有氧元素参加 C. 氧化反应一定先于还原反应 D. 发生氧化反应的物质也可能同时发生还原反应 |
|
| 2. 选择题 | 详细信息 |
|
已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法正确的是( ) (说明:一种小球代表一种元素的原子) A.图中的反应物都是化合物 B.该反应属于置换反应 C.该反应属于非氧化还原反应 D.该反应不符合质量守恒定律 |
|
| 3. 选择题 | 详细信息 |
|
下列反应的离子方程式正确的是( ) A.少量的碳酸氢钠溶液与澄清石灰水混合:2 B.过量的碳酸氢钠溶液与澄清石灰水混合: C.碳酸氢钠溶液与少量的盐酸溶液混合: D.碳酸钠溶液与过量的盐酸溶液混合:Na2CO3+2H+=2Na++CO2↑+H2O |
|
| 4. 选择题 | 详细信息 |
|
分类方法在化学学科的发展中起到了非常重要的作用,下列分类标准合理的是 A.根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等 B.根据纯净物的元素组成,将纯净物分为单质和化合物 C.根据能否与碱反应将非金属氧化物分为酸性氧化物和不成盐氧化物 D.根据其溶液是否导电,将物质分为电解质和非电解质 |
|
| 5. 选择题 | 详细信息 |
|
某胶体遇盐卤(MgCl2)或石膏水发生凝聚,而遇食盐水或硫酸钠溶液不易发生凝聚,下列说法中错误的是( ) A. 胶体粒子直径在l~100 nm之间 B. 遇BaCl2溶液或氢氧化铁胶体可发生凝聚 C. 电泳时,该胶体向阴极方向移动 D. 钠离子使此胶体凝聚的效果不如Ca2+、Mg2+ |
|
| 6. 选择题 | 详细信息 |
|
下列各组微粒中,在一定条件下均可以作氧化剂的是( ) A. Fe、H2O、CO2 B. Fe3+、MnO4—、NO3— C. Cl2、HClO、Mg D. ClO-、Cl-、Ag+ |
|
| 7. 选择题 | 详细信息 |
|
浓盐酸与次氯酸钙能发生反应Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质是( ) ①CO2 ②HCl ③H2O(g) ④O2 A. ①②③ B. ②③④ C. ②③ D. ①④ |
|
| 8. 选择题 | 详细信息 |
|
已知氧元素的原子结构示意图为 A.F |
|
| 9. 选择题 | 详细信息 |
|
加热5g碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为 A.3.38g B.4.58g C.4.16g D.4.41g |
|
| 10. 选择题 | 详细信息 |
|
实验室里需要240 mL 0.1 mol·L-1的硫酸铜溶液,现选取250 mL容量瓶进行配制,以下叙述正确的是( ) A. 称取4.0 g无水硫酸铜,加水250 mL B. 称取6.25 g胆矾,加水250 mL C. 称取3.84 g无水硫酸铜,配成250 mL溶液 D. 称取4.0 g无水硫酸铜,配成250 mL溶液 |
|
| 11. 选择题 | 详细信息 |
|
某无色透明溶液中,能大量共存的离子组是( ) A.Cu2+、Na+、SO42-、Cl﹣ B.Ba2+、Na+、OH﹣、SO42- C.OH﹣、HCO3﹣、Ca2+、Na+ D.K+、Na+、OH﹣、NO3﹣ |
|
| 12. 选择题 | 详细信息 |
|
R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是(m、n均为正整数)( ) A.若R(OH)n为强碱,则W(OH)n+1也为强碱 B.若HnXOm为强酸,则Y是活泼非金属元素 C.若Y的最低化合价为-2,则Z的最高正化合价为+6 D.若X的最高正化合价为+5,则五种元素都是非金属元素 |
|
| 13. 选择题 | 详细信息 |
用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。 一种生成Na2FeO4的反应如下:Fe2O3+Na2O2(氧为-1价) A.Na2O2既是氧化剂又是还原剂 B.Fe2O3在反应中失去电子 C.配平后为Fe2O3+3Na2O2=2Na2FeO4+Na2O D.Na2FeO4能消毒杀菌是因其具有强氧化性 |
|
| 14. 选择题 | 详细信息 |
|
短周期元素A、B、C原子序数依大增大,A3-与B2-、C+电子层结构相同,则下列说法中不正确的是 A. 三种元素可组成CAB2和CAB3型化合物 B. 离子半径:C+>B2->A3- C. H2B在同主族元素气态氢化物中最稳定 D. B的某种单质可用于杀菌消毒 |
|
| 15. 选择题 | 详细信息 |
|
现有下列几个离子反应: ①Cr2O72-+14H++6Cl-=2Cr3++3Cl2↑+7H2O ②2Fe2++Br2=2Fe3++2Br- ③2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ 下列有关性质的比较中正确的是( ) A.氧化性:Cr2O72->Cl2>Fe3+ B.氧化性:Cl2>Br2> Cr2O72- C.还原性:SO2<Fe2+<Br- D.还原性:Cl->Cr3+>Fe2+ |
|
| 16. 选择题 | 详细信息 |
|
下列反应中关于“H2O”的说法错误的是( ) A. 2F2+2H2O=4HF+O2反应中,水作还原剂,失电子 B. 2Na+2H2O=2NaOH+H2↑反应中,水被氧化 C. CH4+2O2=CO2+2H2O反应中,H2O是还原产物 D. Na2O+H2O=2Na++2OH﹣反应中,水既不是氧化剂也不是还原剂 |
|
| 17. 选择题 | 详细信息 |
|
下列分子中含有的电子数目与HF相同,且只有两个极性共价键的是( ) A.CO2 B.N2O C.H2O D.CH4 |
|
| 18. 选择题 | 详细信息 |
|
下列化学用语中,正确的是( ) A.溴化钠的电子式为Na:Br: B.镁的原子结构示意图为 C.用电子式表示氯化氢分子的形成过程为H·+ D.重水的化学式为 |
|
| 19. 选择题 | 详细信息 |
|
铅笔芯的主要成分是石墨。如果铅笔芯写一个字消耗的石墨质量约为1×10-3g,那么一个铅笔字含有的碳原子数约为 A. 5×1019个 B. 5×1022个 C. 2.5×1022个 D. 2.5×1019个 |
|
| 20. 选择题 | 详细信息 |
|
实现下列转化,必须加入氧化剂或还原剂的是( ) A. NO2→HNO3+NO B. C. NH3→NO D. P2O5→H3PO4 |
|
| 21. 选择题 | 详细信息 |
|
除去氧化铁中的二氧化硅,可采用的试剂是 A. 盐酸 B. 硝酸 C. 蒸馏水 D. 烧碱溶液 |
|
| 22. 选择题 | 详细信息 |
|
下列物质中均为既含有离子键又含有共价键的一组是( ) A.NaOH、H2O、NH4Cl B.KOH、Na2O2、(NH4)2S C.MgO、CaBr2、NaCl D.Na2SO4、HCl、MgCl2 |
|
| 23. 选择题 | 详细信息 |
|
20 ℃时,饱和氯化钾溶液的密度为1.174 g/mL,物质的量浓度为4.0 mol/L,则下列说法中正确的是 A.25 ℃时,饱和氯化钾溶液的浓度小于4.0 mol/L B.此溶液中氯化钾的质量分数为 C.20 ℃时,密度小于1.174 g/mL的氯化钾溶液是不饱和溶液 D.将此溶液蒸发部分水,再恢复到20 ℃时,溶液密度一定大于1.174 g/mL |
|
| 24. 实验题 | 详细信息 |
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: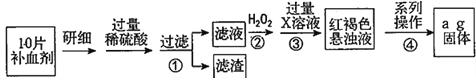 请回答下列问题: (1)向操作①的滤液中滴加KSCN 溶液后变为红色,则该滤液中含有______(填离子符号)。 (2)操作②中反应的离子方程式:__________________________________。 (3)操作③中反应的离子方程式:__________________________________。 (4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。 (5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示) |
|
| 25. 实验题 | 详细信息 |
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题(Cl2易溶于CCl4)。 (1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2质量总是小于3.55 g的原因是________________________________。 (2)①装置B中盛放的试剂名称为________________,作用是________________________________,现象是_____________________________。 ②装置D和E中出现的不同现象说明的问题是___________________。 ③装置F的作用是__________________________________________。 (3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填写试剂或用品名称)。 |
|
| 26. 综合题 | 详细信息 |
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。 根据反应中观察到的现象,回答下列问题: (1)金属钠的变化现象________。 (2)U形管中溶液的颜色_____,说明有__________生成。 (3)铜丝的变化现象____________,说明有________生成;若去掉后面的装置,简述检验气体的方法____ (4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______。 |
|
| 27. 推断题 | 详细信息 |
已知:甲、乙、丙、丁为常见化合物,A、B为单质,相互转化关系如图。其中甲是天然气的主要成分。回答下列问题: (1)丁物质的名称:______,丙物质的化学式:_________________________________________。 (2)检验化合物乙的化学方程式:___________________________________________________。 (3)试剂X可能的化学式:________、________(要求:所选物质类别不同)。 (4)通过分析表明:燃料充分燃烧的条件之一是______________________________。 (5)取变红溶液于试管中加热,观察到的现象有_______________________________________。 |
|
| 28. 推断题 | 详细信息 |
A、B、C、D、E五种物质是含钠元素的单质或化合物,其中B为淡黄色固体,它们有如图所示的转化关系: (1)推断各符号所代表的物质的化学式: A____________,B____________,C____________,D____________,E____________。 (2)分别写出反应②、⑤的化学方程式: ②______________________________________, ⑤__________________________________________。 (3)写出反应③的离子方程式____________________________________________。 |
|
| 29. 推断题 | 详细信息 |
|
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。 (1)把与下面元素有关性质相符的曲线标号填入相应的空格中: a.  b. b.  c. c.  d. d.  ①第ⅡA族元素的价电子数________。 ②第三周期元素的最高化合价________。 ③F-、Na+、Mg2+、Al3+的离子半径________。 (2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答: ①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。 ②N的最高价氧化物的水化物的化学式为________________。 ③M的最高价氧化物的化学式为________________________。 |
|
最近更新



