安徽省定远县育才学校2021届高三8月月考化学题带答案和解析
| 1. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是 A. 1molFeI2与足量氯气反应时转移的电子数为2NA B. 标准状况下,22.4LSO3含有NA个SO3分子 C. 3molNO2和H2O完全反应,被还原的NO2分子数目为1NA D. 56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
|
| 2. 选择题 | 详细信息 |
|
下列有关物质的性质、制取或应用等的说法中正确的是 A. 二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 B. Al2O3的熔点很高,可制作耐高温材料,工业上也电解Al2O3来冶炼Al C. K2FeO4具有还原性,可用于自来水的杀菌消毒 D. 水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
|
| 3. 选择题 | 详细信息 |
草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。某学生拟用下图装置做草酸晶体的分解实验并验证部分产物,下列说法错误的是 A. 装置A中的大试管口应略向下倾斜,是因为加热草酸晶体时会产生水 B. 装置B的主要作用是冷凝(水蒸气、草酸)等,防止草酸进入装置C中,干扰CO2的检验 C. 装置C中可观察到的现象是有气泡冒出,澄清石灰水变浑浊 D. 本实验能证明草酸晶体的分解产物有二氧化碳 |
|
| 4. 选择题 | 详细信息 |
|
下列有关实验的选项正确的是 ( ) A.  X若为苯,可用于吸收NH3或HCl,并防止倒吸 X若为苯,可用于吸收NH3或HCl,并防止倒吸B.  除去CO中的CO2 除去CO中的CO2C.  可用于分离C2H5OH和H2O的混合物 可用于分离C2H5OH和H2O的混合物D.  记录滴定终点读数为12.20 mL 记录滴定终点读数为12.20 mL |
|
| 5. 选择题 | 详细信息 |
|
高铁酸钾(K2FeO4)是一种比Cl2、O3、KMnO4氧化性更强的多功能水处理剂.工业上可先制得高铁酸钠(离子反应为2Fe(OH)3+3ClO-+4OH-=2FeO42-+ 3Cl-+5H2O).然后在高铁酸钠溶液中加入一定量的KOH.可析出高铁酸钾.下列说法不正确的是 A. 高铁酸钾能除去水中溶解的H2S等 B. 高铁酸钾中Fe为+6价,具有强氧化性,能消毒杀毒 C. 业上制各高铁酸钠时每生成1mol还原产物,转移3mol电子 D. 高铁酸钾的还原产物易水解形成胶体,可使水中悬浮物凝聚沉降 |
|
| 6. 选择题 | 详细信息 |
|
已知H2SO3+I2+H2O == H2SO4+2HI,将0.1mol Cl2通入100mL含等物质的量的HI与H2SO3的混合溶液中,有一半的HI被氧化,则下列说法正确的是 A. 物质的还原性:HI>H2SO3>HCl B. H2SO3的物质的量浓度为0.6 mol·L-1 C. 若再通入0.05mol Cl2,恰好能将HI和H2SO3完全氧化 D. 通入0.1mol Cl2发生反应的离子方程式为:5Cl2+4H2SO3+2I-+4H2O == 4SO42-+I2+10Cl-+16H+ |
|
| 7. 选择题 | 详细信息 |
|
将38.4g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL 2mol/L NaOH 溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O;NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为 A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol |
|
| 8. 选择题 | 详细信息 |
|
确认化学反应先后顺序有利于解决问题,下列反应先后顺序判断正确的是 A. 在各1mol的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ B. 在各2mol的Ba(OH)2、KOH的溶液中通入CO2:KOH,Ba(OH)2、BaCO3 C. 在各 2mol的 Fe2+、Ag+、Cu2+、H+的溶液中加入 Zn:Ag+、Cu2+、H+、Fe2+ D. 在各1mol 的 AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- |
|
| 9. 选择题 | 详细信息 |
工业上用铝土矿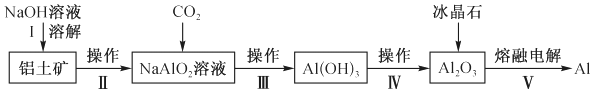 下列叙述错误的是( ) A.操作I增大NaOH溶液用量可提高 B.操作Ⅱ、Ⅲ为过滤,操作Ⅳ为灼烧 C.通入过量 D.加入的冰晶石目的是降低 |
|
| 10. 选择题 | 详细信息 |
下图为A、B、C、D、E之间的相互转换关系A为一种气态单质,D是一种红棕色气体。下列说法正确的是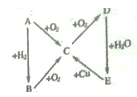 A. C 物质和O2必须在催化剂表面才能反应生成D B. Cu 和E 溶液反应体现了E 的强氧化性和酸性 C. 可用NaOH 溶液除去混在D物质中的少量B 物质 D. B 生成C 的反应中,氧化剂与还原剂之比为4: 5 |
|
| 11. 选择题 | 详细信息 |
|
将13.6gCu和Cu2O组成的混合物加入250 mL—定浓度的稀硝酸中,固体完全溶解生成Cu(NO3)2和NO。向所得溶液中加入1.0 L 0.5 mol • L-1的NaOH溶液,生成沉淀的质量为19.6 g,此时溶液呈中性,且金属离子(钠离子除外)沉淀完全。下列说法正确的是 A. 原固体混合物中,Cu和Cu2O的物质的量之比为1:1 B. 原稀硝酸的浓度为1.3 mol·L-1 C. 固体溶解后剩余硝酸的物质的量为0.1 mol D. 产生的NO的体积为2.24L |
|
| 12. 选择题 | 详细信息 | ||||||||||||||||||||
由下列实验及现象推出的相应结论正确的是
|
|||||||||||||||||||||
| 13. 选择题 | 详细信息 |
|
在含0.2 mol KOH和0.1 mol Ba(OH)2的混合溶液中持续通入6.72 L(标况)CO2的过程中,溶液中离子的物质的量n和通入CO2体积V的关系示意图正确的是( ) A.  B. B.  C.  D. D. 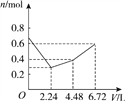 |
|
| 14. 选择题 | 详细信息 | ||||||||||||
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是
A.盐酸的物质的量浓度为5.0mol·L-1 |
|||||||||||||
| 15. 选择题 | 详细信息 |
标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是 A. a点对应溶液的导电性比d点强 B. 氢硫酸的酸性比亚硫酸的酸性强 C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀 D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1 |
|
| 16. 实验题 | 详细信息 | |||||||||
半导体生产中常需要使用掺杂剂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去) 已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;②PCl3遇水会强烈水解生成H3PO3和HCl;③PCl3遇O2会生成POCl3,POCl3溶于PCl3;④PCl3、POCl3的熔沸点见下表:
|
||||||||||
| 17. 实验题 | 详细信息 |
|
铝元素含量居金属首位, 主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领城应用广泛。 Ⅰ、工业上用铝土矿制备铝的某种化合物的工艺流程如下:  (1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。 ①该过程中涉及某氧化还原反应如下,请完成: Fe2++□ClO-+□ ═□Fe(OH)3↓+□Cl-+□__________ ②检验滤液B中是否还含有铁元素的方法为:_________________________ ③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________(选填代号) A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳 ④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、__________(填操作名称)、过滤、洗涤。 Ⅱ、明矾(KAl(SO4)2·12H2O)在日常生活、生产中也占有一席之地。 (1)明矾曾经是净水明星,用离子方程式表示其净水原理_____________________________。 (2)明矾净水时,若不慎过量会有一定程度的副作用。将含有明矾的水溶液中加入Ba(OH)2溶液至铝离子恰好完全沉淀,并且过滤,就可以避免,请用离子反方程式描述其过程______________。 |
|
| 18. 实验题 | 详细信息 |
|
已知: Mg能在NO2中燃烧,可能产物为Mg3N2、MgO和N2。Mg3N2容易与水反应。 (1) 某实验探究小组探究Mg与NO2反应的固体产物成分,对固体产物提出三种假设: I.假设为: 固体产物为MgO;II.假设为:________;III.假设为: ________。 (2) 该小组通过如下实验装置来验证Mg在NO2中燃烧反应产物(夹持装置省略,部分仪器可重复使用  ①实验装置连接的顺序为____________(填字母序号); ②装置B中盛装的试剂可以是_______ (填字母) a.浓硫酸 b.碱石灰 c.无水CaCl2 d.五氧化二磷 ③确定产物中有N2生成的实验现象为_____________________。 (3)设计实验证明: 产物中存在Mg3N2: ____________________。 (4)己知装置C中初始加入Mg粉质量为13.2g,在足量的NO2中充分燃烧,实验结束后,硬质玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为21.0g,产生N2的体积为1120mL(标准状况)。写出玻璃管中发生反应的化学方程式:_________________。 |
|



