2019届九年级一模化学免费试卷完整版(天津市部分区)
| 1. | 详细信息 |
|
下列变化属于化学变化的是 A. 粉笔折断 B. 盐酸挥发 C. 粮食酿酒 D. 冰棒融化 |
|
| 2. | 详细信息 |
|
下列物质属于纯净物的是 A. 水泥砂浆 B. 澄清石灰水 C. 空气 D. 二氧化硫 |
|
| 3. | 详细信息 |
|
某同学患了夜盲症,到了傍晚就看不清东西,他体内缺乏的是 A. 维生素A B. 锌 C. 维生素C D. 铁 |
|
| 4. | 详细信息 |
|
能源是人类赖以生存的基础。下列关于能源的说法正确的是 A. 可燃冰将成为未来新能源,其主要成分是干冰 B. 乙醇是可再生能源,添加变性剂与汽油按一定比例可配成汽车燃料 C. 化石燃料是指煤、石油、煤气等不可再生能源 D. 氢能是理想的清洁能源,作为零污染和零碳能源正在被广泛应用 |
|
| 5. | 详细信息 |
下图为镁元素和氯元素在元素周期表中的部分信息,下列有关说法不正确的是 A. 氯是一种非金属元素 B. 镁元素的相对原子质量是24.31g C. 氯原子中质子数是17 D. 镁、氯属于不同种元素的最本质原因是质子数不同 |
|
| 6. | 详细信息 |
|
下列图示的实验操作中不正确的是 A.  读取液体体积 B. 读取液体体积 B.  蒸发结晶 蒸发结晶C. 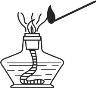 点燃酒精灯 D. 点燃酒精灯 D. 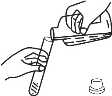 倾倒液体 倾倒液体 |
|
| 7. | 详细信息 |
|
下列是对一瓶饱和氢氧化钠溶液的叙述,说法不正确的是 A. 该溶液可以导电 B. 外界条件不改变,氢氧化钠不会从溶液中分离出来 C. 溶液均一、稳定是因为钠离子和氢氧根离子均匀分散在水中静止不动 D. 改变条件,能够使氢氧化钠的饱和溶液与不饱和溶液相互转化 |
|
| 8. | 详细信息 |
|
化学实验中常常表现出颜色美,下列化学实验中的颜色变化符合事实的是 A. 铁钉放入适量硫酸铜溶液中,铁钉表面有蓝色物质出现 B. 将在空气中燃着的硫伸入到盛有氧气的集气瓶中,火焰由黄色变为蓝紫色 C. 红磷在空气中燃烧时,产生大量的白雾 D. 高温加热木炭与氧化铜的混合物,完全反应后固体由黑色变成红色 |
|
| 9. | 详细信息 |
 A. 参加反应的两种分子个数比是2:1 B. 该反应是化合反应 C. 反应生成两种生成物 D. 每个生成物分子由3个原子构成 |
|
| 10. | 详细信息 |
|
下列是有关碳及其化合物的说法,正确的是 A. —定条件下,一氧化碳和二氧化碳可以相互转化 B. 金刚石、石墨是碳单质, C. 金刚石、石墨和 D. —氧化碳和二氧化碳的化学性质不同是因为构成这两种物质的原子数目不同 |
|
| 11. | 详细信息 |
|
下列说法中不正确的是 A. 墙内开花墙外可闻到花香,是因为分子总是在不断运动着 B. 甲烷燃烧放出大量的热,是因为所有化学反应都放出热量 C. 在生煤火炉时,点燃木柴来引燃煤是为了使温度达到煤的着火点 D. 稀释浓硫酸时,将浓硫酸慢慢注入水中是防止溶解放出的热造成液滴飞溅 |
|
| 12. | 详细信息 | |||||||||||||||
下列实验方法能达到实验目的的是
|
||||||||||||||||
| 13. | 详细信息 |
|
下列对露置在空气中已部分变质的氢氧化钠溶液样品进行的相关分析和实验中,合理的是 A. 变质原因:氢氧化钠溶液吸收空气中的二氧化碳生成碳酸钠 B. 检测变质:取少量溶液样品,滴加氯化钡溶液,有白色沉淀生成或向样品中滴加稀盐酸,有气泡冒出 C. 证实部分变质:取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化納 D. 除去杂质:向溶液样品中加入过量的澄清石灰水至完全反应后过滤,可除去样品中的杂质 |
|
| 14. | 详细信息 |
|
向氧化铜和铁粉的混合物中加入一定量稀硫酸,反应停止后,过滤,向滤渣中再滴加稀硫酸,未看见有任何变化。下列判断正确的是 A. 滤液中一定含有硫酸铁 B. 滤液中一定没有硫酸铜和硫酸 C. 滤渣中一定含铜,可能含铁 D. 滤渣中一定含有铜 |
|
| 15. | 详细信息 |
|
现有碳酸钙和碳酸氢钾 A. 混合物中碳酸钙和碳酸氢钾的质量比一定是1:1 B. 混合物充分反应后,所得溶液质量是 C. D. 混合物中碳元素总质量等于 |
|
| 16. | 详细信息 |
|
化学与我们的生活有着密切的联系。现有①金刚石②铜③酒精④氢氧化钠⑤小苏打⑥氦气,从中选择恰当的物质填空(填序号)。 (1)用于治疗胃酸过多症的是_____ (2)用于制造导线的是_____ (3)用于制取肥皂的是_____ (4)用于刻划玻璃的是_____ (5)可用于霓虹灯光源的是_____ (6)用作内燃机的燃料的是_____ |
|
| 17. | 详细信息 |
|
在宏观、微观和符号之间建立联系是化学学科的重要思维方式。 (1)如下图所示,Y是_____,M是_____。 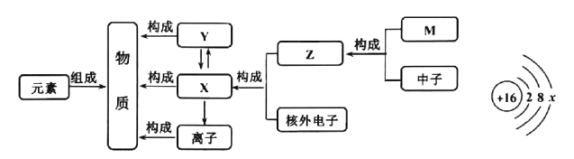 (2)如图是硫元素的原子结构示意图,  (3)从宏观角度看,五氧化二磷是由_____组成,从微观角度看,五氧化二磷是由_____构成。 |
|
| 18. | 详细信息 |
|
水是人类宝贵的自然资源。 (1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质.过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和_____(填仪器名称)。在净水装置中常含有活性炭,活性炭所起的作用为_____。 (2)硬水给生活和生产带来很多麻烦,生活中常用_____的方法降低水的硬度。检验软水和硬水的常用方法是使用_____。 (3)电解水实验中,如果用 |
|
| 19. | 详细信息 |
|
完成下列化学方程式 (1)细铁丝在氧气中燃烧_____; (2)过氧化氧溶液与二氧化锰混合_____; (3)铁丝放入硝酸银溶液中_____。 |
|
| 20. | 详细信息 | ||||||||||||||||||||
下表是
|
|||||||||||||||||||||
| 21. | 详细信息 |
下图是初中化学中常见物质间的转化关系,其中C、D、G为单质,且G是目前世界年产量最高的金属,其余为化合物。A是地球上最多的液态氧化物,F与H的组成元素相同。J不溶于水,是常见的重要建筑材料的主要成分(反应条件、部分反应物和生成物均已略去)。 (1)据上图推断(B、D、E写化学式,I写俗名): B_____、D_____、E_____、I_____; (2)C→F反应的基本类型是_____; (3)写出H+I→J+A的化学方程式_____。 |
|
| 22. | 详细信息 |
根据下图所示实验装置进行回答: (1)写出图中有标号仪器的名称:①_____。 (2)实验室利用高锰酸钾制取并收集氧气,可选用_____装置组合,其反应的化学方程式为_____。收集干燥的氧气需通过多功能装置F,F中应装有_____,氧气需从_____(填“a”或“b”)端通入。 (3)用完酒精灯后,不能用嘴吹灭,应用灯帽盖灭。为了下次使用时容易打开灯帽,盖灭后应趁热_____。 (4)实验室制取并收集二氧化碳,可用装置的组合为_____,反应的化学方程式为_____。 |
|
| 23. | 详细信息 |
|
金属材料用途广泛,根据所学知识回答: (1)我国科技迅猛发展,航海及军事领域取得重大突破。建造航母用到了钛合金,工业制钛有一种反应为: (2)航母外壳使用的是钢铁材料并用涂料将钢铁材料覆盖,使用涂料是为了防止钢铁材料与_____接触而锈蚀。 (3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_____(填序号)。 A B (4)冶炼2900t含四氧化三铁80%的磁铁矿石,理论上能得到含杂质2%的生铁的质量是_____t(结果精确到0.1)。 |
|
| 24. | 详细信息 |
|
水在日常生活及科学实验中不可缺少。 (1)实验室配制一定质量的10%的氯化钠溶液。配制步骤中,_____时要用玻璃棒。溶液配制过程中除了天平、量筒、烧杯、药匙和玻璃棒外,还需要用到的仪器有_____。 (2)用洗涤剂洗涤某件衣服。“拧干”后该湿衣残留的溶液为100g,其中含洗涤剂的质量分数为2%,该湿衣服上残留的洗涤剂质量为_____g。现用6000g清水对这件衣服进行漂洗,“拧干”后残留在湿衣服上的洗涤剂的质量为_____g(用分数表示) |
|
| 25. | 详细信息 |
|
花青素(化学式 (1)花青素中碳、氢、氧元素的质量比为_____; (2)花青素的相对分子质量为_____; (3)花青素中氧元素的质量分数为_____(计算结果精确到0.1%) |
|
| 26. | 详细信息 |
|
将一定质量的某金属R放入l00g 14.6%稀盐酸中,恰好完全反应。实验测得R的氯化物中氯元素含量为52.2%,计算: (1)反应生成的气体质量是多少? (2)金属R的质量是多少克? |
|
最近更新