2019届初三下学期中考模拟化学题开卷有益(安徽省淮北市三铺中学)
| 1. | 详细信息 |
|
下列操作中,从物质变化的角度分析,主要体现物理变化的是( ) A.  鉴别硬水和软水 鉴别硬水和软水B.  在皮蛋上浇醋调味 在皮蛋上浇醋调味C.  自制汽水 自制汽水D.  用大烧杯罩上两个小烧杯 用大烧杯罩上两个小烧杯 |
|
| 2. | 详细信息 |
|
6月5日是世界环境日。但是,随着人口的增多,经济的增长,空气和水污染加重,酸雨的浇淋,森林的锐减,空气质量逐年不尽人意,土壤荒漠化面积的扩大,以及气候的变化……环境承受的压力越来越大,近期的雾霾天气我们有目共睹,济南市的市民也深受其害。今天我们中学生面临着发展和保护环境的双重任务。通过学习化学请你判断人类的下列生产活动不会对地球环境造成破坏的是 A.生活污水及工业废水、废气直接向大气排放 B.大量使用煤、石油、天然气等化石燃料 C.大量砍伐森林,以满足建设需要;大量捕杀濒危野生动物,以满足饮食需要 D.把生产和消费过程中产生的废弃物进行收集和处置,回收可利用资源 |
|
| 3. | 详细信息 |
|
蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料,下列食物中属于糖类的是( ) A.  米饭 B. 米饭 B.  红烧肉 红烧肉C.  鲫鱼 D. 鲫鱼 D.  西红柿 西红柿 |
|
| 4. | 详细信息 |
医学上可用68Ga作放射性示踪剂对某些肿瘤进行诊疗,如图为Ga在周期表中的信息及其某种微粒结构示意图,下列说法正确的是 A. 镓原子的中子数为31 B. 图中x=3 C. 镓原子在化学反应中易得到电子 D. 镓的相对原子质量为69.72 g |
|
| 5. | 详细信息 |
|
多巴胺(C8H11O2N)是一种神经传导物质,能直接影响人的情绪,左右人的行为,在学习和记忆过程中起着关键作用。下列关于多巴胺的说法正确的是( ) A. 多巴胺是由碳、氢、氧、氮四种元素组成的有机高分子化合物 B. 多巴胺中碳元素的质量分数最大 C. 多巴胺中碳、氧、氢、氮元素的质量比为8:11:2:l D. 多巴胺分子中质子与电予的数目不相等 |
|
| 6. | 详细信息 |
如图是某密闭容器中物质变化过程的微观示意图。下列说法中正确的是( ) A. R、M、N均是混合物 B. 变化Ⅰ、Ⅱ、Ⅲ均属于物理变化 C. 变化Ⅱ、Ⅲ说明分子间有间隔 D. R、M、N中共有两种分子 |
|
| 7. | 详细信息 |
|
下列实验不能达到目的是( ) A. 探究金属的活动顺序 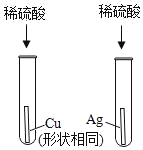 B. 测定空气中氧气的含量  C. 证明CO2不能燃烧、不能支持燃烧,密度比空气大  D. 证明分子不断运动  |
|
| 8. | 详细信息 |
|
归纳总结和逻辑推理是化学学习中常用的思维方法。下列归纳推理正确的是( ) A. 化合物中含不同种元素,所以含不同种元素的物质都是化合物 B. 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 C. 非金属氧化物能与碱溶液反应,所以CO2、SO2 、CO均可与碱溶液反应 D. 点燃可燃性气体前要验纯,所以点燃甲烷前一定要验纯 |
|
| 9. | 详细信息 |
已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成。如图:在温度计示数为280℃以上时,快速推动活塞,观察到蜡烛立 即熄灭,其主要原因是( )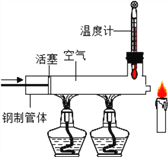 A. 隔绝氧气 B. 降温到着火点以下 C. 移走可燃物 D. 无法判断 |
|
| 10. | 详细信息 |
近年来,我国航空、航天、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标志着我国的航空强国梦又迈出了一大步。大飞机使用的化学材料如甲图。请回答: (1)钛合金属于_____________(填“金属”或“合成”)材料。 (2)图乙是钛原子结构示意图,则x=_______;钛元素位于元素周期表第____________周期。 (3)铁比铝的强度大,但制造飞机却用铝合金而不用铁合金,主要原因是铝比铁的密度小且抗腐蚀性能强。铝具有很好的抗腐蚀性的原因是_____________。 (4)大飞机的化学材料不能用纯金属,这是因为纯金属容易腐蚀,例如铁制品生锈是由于铁制品同时与空气中的氧气和_____________接触而锈蚀。 (5)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是___________(填序号)。 ①Fe、CuSO4溶液、Ag ②FeSO4溶液、Cu、Ag ③FeSO4溶液、Cu、AgNO3溶液 ④FeSO4溶液、CuSO4溶液、Ag |
|
| 11. | 详细信息 |
结合下列实验装置回答相关问题: (1)写出A装置中a、b仪器的名称:a ___________b _______________。 (2)用石灰石与盐酸反应制CO2的化学方程式为_____________,收集装应选C____________(填编号)用双氧水制O2的化学方程式为___________________。 (3)若用B作制气装置,与A相比,其优点是_______________(写一点) (4)用KClO3和MnO2制O2,若选用A作发生装置,则还要增加_____________(填仪器名称),并把A作如下改动: ________________。 (5)用排水法开始收集氧气的适宜时刻是__________________,用排水法收集氧气你是怎样确定集气瓶已收集满气体? _________________。 |
|
| 12. | 详细信息 |
二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②特殊条件下电解NaCl溶液制NaClO3;③ClO2的制取。工艺流程如图,其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。 (1)加入过量氢氧化钠的目的是____________________________; 过量的试剂X是__________(填化学式); (2)操作A中用到的玻璃棒的作用是_______________; (3)加入适量HCl至酸性过程中,发生的中和反应的化学方程式是__________________; (4)分析完成反应Ⅱ的化学方程式:_______________________________; (5)该流程中可循环利用的物质是水和____________。 |
|
| 13. | 详细信息 | ||||||||
|
化学反应速率是衡量化学反应进行快慢的物理量。为了探究影响化学反应速率的隐私,以过氧化氢分解为研究对象进行实验。三个小组均采用如图装置进行实验,记录收集10mL氧气的时间。实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。 A组:探究催化剂对化学反应速率的影响 取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
|
|||||||||
| 14. | 详细信息 | |||||||||||||||
等质量的铁粉与过量的盐酸在不同的实验条件下进行反应,测定在相同时间t内产生气体体积V的数据,根据数据绘制得到图1。
|
||||||||||||||||
| 15. | 详细信息 |
|
乙醇是一种清洁燃料,但在氧气不足时燃烧,会生成一氧化碳,现有207 g乙醇与一定量的氧气点燃后发生如下反应:3C2H5OH+8O2 (1)计算207 g乙醇中含碳元素的质量_______。 (2)计算该反应生成一氧化碳的质量________。 |
|