2020年陕西佳县佳芦镇中学中考模拟化学免费试卷
| 1. 选择题 | 详细信息 |
|
能保持氢气化学性质的微粒是 A. |
|
| 2. 选择题 | 详细信息 |
|
下列物质按酸、碱、盐顺序排列的是( ) A.烧碱、盐酸、食盐 B.纯碱、火碱、硫酸 C.硝酸、熟石灰、纯碱 D.盐酸、纯碱、硫酸锌 |
|
| 3. 选择题 | 详细信息 |
|
在科学技术发展史上,为人类增产粮食消除饥荒作出巨大贡献的化学成就是( ) A.合成氨工业 B.金属冶炼 C.石油工业 D.海水的综合利用 |
|
| 4. 选择题 | 详细信息 |
|
下列对于事故的处理方法不正确的是( ) A.家中煤气泄漏,立即开门开窗 B.火灾现场逃生,湿毛巾捂嘴弯腰前行 C.实验中,不小心打翻酒精灯,应立即用湿毛巾盖灭 D.如果不慎将浓硫酸溅到皮肤上,立即用NaOH溶液冲洗 |
|
| 5. 选择题 | 详细信息 |
|
能在水中大量共存的一组离子是 A.NH4+、Na+、C1-、SO42- B.H+、Na+、NO3-、CO32- C.K+、Ba2+、OH-、SO42- D.K+、Ag+、NO3-、C1- |
|
| 6. 选择题 | 详细信息 |
|
下列物质不属于溶液的是( ) A.食盐水 B.苏打水 C.蒸馏水 D.澄清石灰水 |
|
| 7. 选择题 | 详细信息 |
|
下列物质暴露在空气中,质量会减小的是( ) A.浓硫酸 B.食盐 C.氢氧化钠 D.浓盐酸 |
|
| 8. 选择题 | 详细信息 |
|
使用绿色能源有利于保护环境。下列能源不属于绿色能源的是( ) A.氢能源 B.化石能源 C.风能 D.太阳能 |
|
| 9. 选择题 | 详细信息 |
|
下列常见的生活物品中,所含的主要原料属于天然纤维的是( ) A. 纯棉衣服 B. 不锈钢刀 C. 橡胶轮胎 D. 塑料花盆 |
|
| 10. 选择题 | 详细信息 |
|
“酒香不怕巷子深”这句俗语,体现了乙醇具有的性质是( ) A.还原性 B.氧化性 C.可燃性 D.挥发性 |
|
| 11. 选择题 | 详细信息 |
|
天然气是我国已经推广使用的清洁能源,其主要成分是( ) A.CO B.H2 C.CH4 D.C2H4 |
|
| 12. 选择题 | 详细信息 |
|
下列图标中,在运输浓硫酸的罐车上需粘贴的是( ) A.  B. B. C. C. D. D. |
|
| 13. 选择题 | 详细信息 |
|
下列变化过程属于化学变化的是( ) A.冰川融化 B.木炭燃烧 C.干冰升华 D.海水晒盐 |
|
| 14. 选择题 | 详细信息 |
|
下列实验操作中,正确的是( ) A.滴加液体  B.闻气体的气味 B.闻气体的气味 C.读取液体的体积 C.读取液体的体积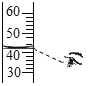 D.取用液体试剂 D.取用液体试剂 |
|
| 15. 选择题 | 详细信息 |
|
下列名称与化学式不相符的是( ) A.烧碱﹣﹣NaOH B.生石灰﹣﹣CaO C.干冰﹣﹣CO2 D.金刚石﹣﹣C60 |
|
| 16. 选择题 | 详细信息 |
|
下列化学方程式书写正确的是( ) A.Fe2O3+6HCl═2FeCl3+3H2O B.2Fe+6HCl═2FeCl3+3H2↑ C.Na2SO4+K2CO3═Na2CO3+K2SO4 D.Cu+Mg(NO3)2═Mg+Cu(NO3)2 |
|
| 17. 选择题 | 详细信息 |
|
逻辑推理是化学常用的思维方法。下列推理正确的是( ) A.单质中只含一种元素,所以只含一种元素的纯净物一定是单质 B.溶液是均一稳定的混合物,所以均一稳定的物质一定是溶液 C.燃烧都伴随着发光、发热现象,所以有发光、发热现象的一定是燃烧 D.蔗糖的饱和溶液不能再溶解蔗糖,也一定不能再溶解其他物质 |
|
| 18. 选择题 | 详细信息 | ||||||||||||||||||||
下列对实验现象的描述及解释不正确的是( )
|
|||||||||||||||||||||
| 19. 选择题 | 详细信息 |
粗盐中常含有CaCl2、MgCl2和可溶性的硫酸盐等。除杂操作中为了保证反应完全,所加试剂都应适当过量。如图是粗盐提纯的简单流程。 X、Y、Z、W代表所加溶液,X、Y、Z、W分别是( ) A.BaCl2 Na2CO3 NaOH HCl B.Na2CO3 BaCl2 HCl NaOH C.Na2CO3 BaCl2 NaOH HCl D.NaOH Na2CO3 HCl BaCl2 |
|
| 20. 选择题 | 详细信息 |
|
已知:2Na2O2+2CO2═2Na2CO3+O2.现将5.6 g CO在足量的O2中完全燃烧生成CO2,再将CO2通入足量Na2O2中充分反应,假设CO2反应完全,则固体增加的质量是( ) A.8.8g B.11.2g C.2.8g D.5.6g |
|
| 21. 填空题 | 详细信息 |
|
用化学符号或符号表示的意义填空。 (1)氧原子__。 (2)铜元素__。 (3)3个镁离子__。 (4)SO42﹣__。 (5)氯化钙____。 (6)2个水分子__。 |
|
| 22. 填空题 | 详细信息 |
在下列图片和各自意义的表述中,找到对应字母填空。 A 富含淀粉的食物 B 用于称量的仪器 C 菜肴调味品 D 太阳能转变为电能 E 氯化氢分子微观示意图 F 属于不可再生能源 (1)____;(2)____;(3)___;(4)____;(5)___;(6)___; |
|
| 23. 填空题 | 详细信息 |
|
请在A﹣H八种物质中,选择符合题意的物质,用序号填空。 A 酒精 B 肥皂水 C 氧气 D 合成橡胶 E 二氧化硫 F 一氧化碳 G pH试纸 H 石墨 (1)具有良好导电性的物质是___。 (2)造成酸雨的气体是____。 (3)用于医疗急救的气体是____。 (4)可用于测定溶液酸碱度的是____。 (5)易与血红蛋白结合而造成人体中毒的气体是____。 (6)实验室常用作液体燃料的是___。 (7)属于有机高分子材料的是___。 (8)可用于区别硬水与软水的物质是____。 |
|
| 24. 填空题 | 详细信息 |
如图是甲、乙两种物质的溶解度曲线。 (1)由图可以看出,甲物质溶解度随温度升高而____(填“增大”“减小”或“不变”)。 (2)甲、乙两物质的溶解度在20℃时相等,此时对应饱和溶液溶质质量分数是____。 (3)A点表示甲物质在40℃时的不饱和溶液。若将该溶液变为40℃的饱和溶液可以采取的措施有___(写出一种)。 |
|
| 25. 填空题 | 详细信息 |
|
铝是一种比较活泼的常见金属,它与酸、碱溶液都能反应产生氢气。 (1)写出铝与稀硫酸反应的化学方程式:_____。 (2)完成铝与氢氧化钠溶液反应生成氢气的化学方程式:2Al+2NaOH+____═2NaAlO2+3H2↑。 (3)已知NaAlO2与少量盐酸反应的化学方程式:NaAlO2+HCl+H2O═Al(OH)3↓+NaCl.请写出NaAlO2与过量盐酸反应的化学方程式:____。 |
|
| 26. 填空题 | 详细信息 |
元素周期表中部分元素的原子结构示意图如图所示,请根据表中信息回答下列问题。 (1)氧原子的质子数为____,画出S2﹣的结构示意图___。 (2)同周期元素性质变化规律:从左到右,金属性逐渐减弱,非金属性逐渐增强,原子的半径逐渐减小。第三周期中金属性最强的元素是___(填元素符号),S、Cl中半径较小的是___。 (3)元素的化学性质主要由最外层电子数决定。碳与硅的最外层电子数___,所以它们有相似的化学性质。已知CO2+2NaOH═Na2CO3+H2O,写出SiO2与NaOH溶液反应的化学方程式:___。 |
|
| 27. 流程题 | 详细信息 |
硫酸锌是木材保存剂的主要成分。某工厂产生的废渣(主要成分为ZnO,少量Fe2O3、CuO)可用于制备ZnSO4,其工艺流程如图所示。 (1)“粉碎”的目的是_____。 (2)“浸取”所得溶液的金属阳离子有Zn2+、Cu2+和_____(填离子符号)。 (3)“除铁”步骤中加入氨水后的操作是____,在实验室该操作必须用到的玻璃仪器是漏斗、烧杯和___。 (4)“除铜”时发生反应的化学方程式是___。 (5)将90 g废渣进行以上流程实验,最终得到6.4 g铜和161 g的ZnSO4,假设废渣中金属元素没有损失,则该废渣中ZnO的质量分数是_____。 |
|
| 28. 实验探究题 | 详细信息 |
|
氯气是一种重要的工业原料。下图是实验室制取收集氯气以及验证氯气性质的实验装置图。 [查阅资料]氯气是一种黄绿色的剧毒气体,密度大于空气。 制取氯气的化学方程式:2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O。 氯气与水反应的化学方程式:Cl2+H2O═HCl+HClO。 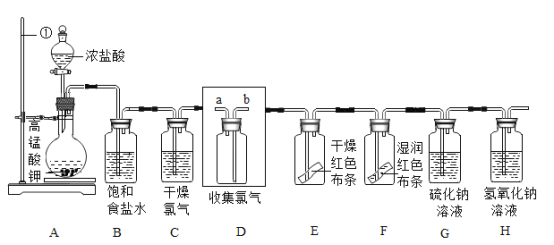 (1)A中仪器①的名称是__,实验时连接好仪器,要先__(填操作名称)再装药品。 (2)从A装置中出来的Cl2混有H2O和__(填化学式),C装置中的试剂是__,C装置的导管应该与D装置导管口__(填“a”或“b”)端连接。 (3)E中红色布条不褪色,F中红色布条褪色,说明Cl2没有漂白性,而是Cl2与水反应生成的___(填化学式)有漂白性。 (4)G中出现淡黄色沉淀,说明反应生成了硫单质,该反应的化学方程式为____。 (5)H是尾气(Cl2)处理装置,反应的化学方程式为____。 |
|
| 29. 科学探究题 | 详细信息 | |||||||||||||||
|
某饮用水中含有较多Ca(HCO3)2和Mg(HCO3)2,该水属于____(填“硬水”或“软水”),常用来烧开水的铝制水壶壶底有一层水垢。某实验小组对该水垢进行探究实验。 [提出问题]该水垢的主要成分是什么? [查阅资料] (1)水垢主要是由两种化合物组成的混合物。 (2)CaCO3、Mg(OH)2难溶于水,Ca(OH)2、MgCO3微溶于水。 [猜想与假设]猜想一:Mg(OH)2、Ca(OH)2;猜想二:____; 猜想三:CaCO3、Mg(OH)2;猜想四:Ca(OH)2、MgCO3。 [设计实验]
|
||||||||||||||||
| 30. 计算题 | 详细信息 |
|
锌不但能与稀硫酸反应,还能与浓硫酸反应。现将19.5克锌加入含有49克H2SO4的浓硫酸溶液中,充分反应后,测得锌与硫酸恰好反应完全,得到SO2和H2的混合气体。已知锌与浓硫酸反应的化学方程式:Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O。 (1)H2SO4由 (填元素名称)元素组成。 (2)ZnSO4中硫原子与氧原子的个数比为 。 (3)SO2的相对分子质量为 ,其中硫元素的质量分数为 。 (4)计算上述反应产生的气体中SO2的质量。(要求写出计算过程) |
|
最近更新



