2020年九年级化学下学期试卷完整版
| 1. 选择题 | 详细信息 |
|
下列现象能用物理变化解释的是( ) A. 水壶烧水出现水垢 B. 房屋倒塌,粮食被埋而生霉 C. 石灰浆粉刷墙壁后,墙面变硬 D. 冬季室内窗玻璃上出现水雾 |
|
| 2. 选择题 | 详细信息 |
|
2018世界地球日主题为“引领绿色生活•推进绿色发展”,下列做法不符合这一主题的是 A. 燃放烟花爆竹,增强节日气氛 B. 共享单车绿色出行,减少空气污染 C. 限用塑料制品,减少白色污染 D. 推广使用清洁能源,缓解温室效应 |
|
| 3. 选择题 | 详细信息 |
|
测定空气里氧气含量通常使用的是 A. 硫 B. 木炭 C. 红磷 D. 蜡烛 |
|
| 4. 选择题 | 详细信息 |
|
小美发现荔枝园旁边的水稻叶子发黄,并倒下了一片,认为应该向稻田施用的是( ) A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.KNO3 |
|
| 5. 选择题 | 详细信息 |
|
下列实验操作正确的是( ) A. 倾倒液体  B. 装入粉末药品  C. 量取液体  D. 加热液体  |
|
| 6. 选择题 | 详细信息 |
|
随着我国人民生活水平的不断提高,家居生活用品应有尽有,对下列家居生活用品分类错误的是( ) A. 混合物:天然气、洗涤剂和牙膏 B. 氧化物:水、酒精和过氧化氢 C. 盐类:氯化钠、小苏打和纯碱 D. 有机化合物:蔗糖、淀粉和醋酸 |
|
| 7. 选择题 | 详细信息 |
|
下列说法完全正确的是( ) A. 地壳中含量最多元素—O;硅的元素符号—Si;2个氮原子—2N B. 决定元素种类—核外电子数;决定元素的化学性质—最外层电子数;决定相对原质量的是—质子数和中子数 C. 铁—由分子构成;二氧化碳—由原子构成;氯化钠—由离子构成 D. 分子—化学变化中的最小粒子;原子—保持物质化学性质的最小粒子;离子—带电的原子 |
|
| 8. 选择题 | 详细信息 |
|
与水相关的叙述正确的是( ) A. 保持水化学性质的最小微粒是氢、氧原子 B. 电解水的化学方程式是H2O C. 电解水产生的氢气和氧气的质量比为 2:1 D. 电解水实验说明水是一种化合物 |
|
| 9. 选择题 | 详细信息 |
|
下列物质的性质,属于物理性质的是( ) A. 酸性 B. 氧化性 C. 吸附性 D. 还原性 |
|
| 10. 选择题 | 详细信息 |
现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是 A. 滴加氢氧化钠溶液质量为a~cg时,溶液中发生的反应为: B. 滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大 C. 滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质 D. 滴加氢氧化溶液质量至cg时,溶液呈中性 |
|
| 11. 选择题 | 详细信息 |
|
工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下: ①  ②  ③ ④  下列说法不正确的是( ) A. 反应①②④均有元素化合价发生变化 B. 反应①④不属于四种基本反应类型中的任何一种 C. 反应②③属于化合反应 D. 四个反应的产物都有氧化物 |
|
| 12. 选择题 | 详细信息 |
|
某些食物的近似pH为:牛奶6.3~6.6,葡萄3.5~4.5,玉米粥6.8~8.0,苹果2.9~3.3,其中酸性最强的是( ) A. 葡萄 B. 牛奶 C. 苹果 D. 玉米粥 |
|
| 13. 选择题 | 详细信息 |
洁厕灵、84消毒液是两种常见的清洁、消毒用品,混合使用时会发生如图反应: 下列说法正确的是( ) A. 该反应是分解反应 B. 有毒气体是Cl2 C. 反应前后元素化合价不变 D. 84消毒液、洁厕灵能混合使用 |
|
| 14. 选择题 | 详细信息 |
|
某同学想用实验证明FeCl3溶液显黄色不是由Cl﹣形成的,下列实验无意义的是( ) A. 加水稀释后,FeCl3溶液黄色变浅 B. 观察KCl溶液没有颜色 C. 向FeCl3溶液中滴加适量NaOH溶液,振荡后静置,溶液黄色消失 D. FeCl3溶液滴加适量无色AgNO3溶液,振荡后静置,溶液黄色未消失 |
|
| 15. 选择题 | 详细信息 |
|
生活中的下列做法符合科学道理的是( ) A. 用大量亚硝酸钠(NaNO2)腌渍火腿 B. 为防止CO中毒,可在煤炉上放一盆水 C. 碳酸钙可做补钙剂 D. 为了提高农业产量.可多施用化肥和农药 |
|
| 16. 选择题 | 详细信息 |
如图是不含结晶水的a、b、c 三种物质的溶解度曲线,下列说法正确的是 ( )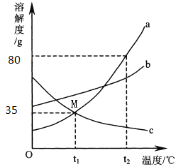 A.t2℃时,将50g a 物质加入到50g 水中充分搅拌,得到100g a的饱和溶液 B.用等质量的a、b、c 三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液 > b溶液 > a溶液 C.将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是: b > a = c D.将t2℃时a、b 两种物质的饱和溶液降温到t1℃时,析出晶体的质量: a > b |
|
| 17. 填空题 | 详细信息 |
|
化学与生活息息相关. (1)为了防止儿童患佝偻病,必须摄入适量的___元素. (2)人体山50多种元素组成,根据含量多少,可分为常量元素和微量元素.其中人体内所含的镁元素属于___(填“常量”或“微量”)元素 (3)洗洁精能清除油污,这是应为洗洁精具有___功能. (4)铁制容器不能盛放硫酸铜溶液,其原因是___(应化学方程式表示). (5)每年4月22为“世界地球日”.下列说法中与“世界地球日”有关的是___(填序号) A 燃料脱硫以减少酸雨的产生 B 开发利用太能能、水能等无污染能源 C 提倡生产和使用可降解塑料 (6)某原子结构示意图和在周围表中的信息如图所示  ①该元素的原子核内质子数为___; ②该元素化学性质由___决定; ③该元素与碳元素的本质区别为___. |
|
| 18. 填空题 | 详细信息 |
|
在上个月我校举行的缤纷体育节系列活动中运动健儿们沉着参赛,稳定发挥,在春季的田径运动场上绽放青春. (1)下列用品中,主要含有有机合成材料的是___; A 橡胶跑道 B 纯棉运动服 C 铅球 (2)赛前食堂为同学们准备了各种早餐:炒青菜、鸡蛋、蔬菜粥、馒头.其中蛋白质含量最高的是___; (3)裁判员高举发令枪,枪声一响,产生大量白烟(枪中火药的主要成分是一种暗红色固体),请写出化学方程式___; (4)比赛准备工作时,小颖发现铁质的起跑器生锈了,她想用稀盐酸来除铁锈,请写出反应方程式___. |
|
| 19. 实验探究题 | 详细信息 |
化学是一门以实验为基础的自然科学,初中化学课上做过许多实验,根据下列四个实验,回答问题: (1)A实验中先_____,再点燃氢气,以免发生爆炸,氢气燃烧的化学方程式是______。 (2)B实验中开始时U型管两端的红墨水液面相平,一段时间后,能观察到的现象是___________。 (3)将白纸剪的五角星用紫色石蕊试液喷湿,放入集气瓶C中,观察到的现象是____,用化学方程式表示产生这种现象的原因___________。 (4)集气瓶D中的铁丝没有燃烧,从燃烧条件来说,原因是_________。 |
|
| 20. 实验探究题 | 详细信息 |
超细碳酸钙可用于生产钙片,牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示图,如图: (1)石灰石的主要成分的化学式为___。 (2)乳化池中,生石灰与水发生反应,其反应方程式为___。其基本化学反应类型是__。 (3)过筛与过滤类似,其目的是拦截___(填“大于”或“小于”)筛孔直径的颗粒。 (4)碳化塔中反应的化学方程式为___。 |
|
| 21. 填空题 | 详细信息 |
|
请根据所学及生活知识参与有关金属制品探究。 (1)将以下金属材料的冶炼按年代的先后顺序排序___(填序号), A 铁 B 青铜 C 铝 从以上顺序可以看出,金属制品的出现顺序与___有关; (2)西汉时期我国的劳动人民发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用化学反应方程式表示其冶炼原理:_; (3)“百炼成钢”是指生铁在高温条件下经过反复锤打转化为钢,反复锤打的目的是降低生铁的__。 |
|
| 22. 实验探究题 | 详细信息 |
如图是初中化学教材中的一些实验,按要求回答下列问题: (1)实验①的实验现象为_____; (2)实验②中薄铜片上的乒乓球碎片先燃烧,滤纸碎片后燃烧,说明燃烧的条件之一是:_____; (3)实验③在白色点滴板上进行实验的优点有_____。(答一条) |
|
| 23. 科学探究题 | 详细信息 | ||||||||
|
2018年春节南昌市出台了禁止燃放烟花爆竹的规定。针对烟花爆竹燃放产生的气体成分,化学兴趣小组同学展开了如下探究: (提出问题)烟花爆竹燃烧后生成哪些气体? (查阅资料) (1)爆竹的主要成分是黑火药,含有硫磺、木炭粉、硝酸钾。 (2)SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3,将SO2气体通入紫红色的酸性高锰酸钾溶液中,溶液会褪色。 (提出猜想)猜想1:CO2 猜想2:SO2 猜想3:CO2和SO2 (实验探究)兴趣小组同学合作设计了如下实验装置,验证猜想的气体。  (现象与结论)
|
|||||||||
| 24. 计算题 | 详细信息 |
|
完成下列计算(除不尽的数据,保留小数点后两位数据): (1)乙二酸(HOOC﹣COOH)中O元素的质量分数为_____. (2)t℃下,将20gNaCl投入80g水,充分搅拌,刚好形成了饱和溶液,如果在t℃下继续向上述溶液中投入20gNaCl并充分搅拌,则所得溶液的溶质质量分数为_____. (3)某同学为了测定双氧水中溶质的质量分数,用烧杯取双氧水溶液50克,加入二氧化锰1克,完全反应后,称得烧杯内剩余物的总质量为49.4克.则该双氧水中的溶质质量分数是___?(写出解题过程). |
|
最近更新



