2019-2020年高一上半年期中考试化学试卷完整版(内蒙古包头市第四中学)
| 1. 选择题 | 详细信息 |
|
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( ) A.  B. B. C.  D. D. |
|
| 2. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.1molH2O的质量为18g/mol B.摩尔是国际单位制中的一个基本物理量 C.3.01×1023个SO2分子的质量为32g D.C2H5OH的摩尔质量为46g |
|
| 3. 选择题 | 详细信息 |
|
在使用容量瓶配制溶液时,下列操作正确的是( ) A. 使用容量瓶前必须检查容量瓶是否漏水 B. 容量瓶用蒸馏水洗净后,再用待配溶液润洗 C. 称好的固体试样需用纸条小心地送入容量瓶中 D. 摇匀后发现凹液面下降,再加水至刻度线 |
|
| 4. 选择题 | 详细信息 |
|
下列仪器中,不能用于加热的是 A. 坩埚 B. 量筒 C. 烧杯 D. 试管 |
|
| 5. 选择题 | 详细信息 |
|
要除去NaCl溶液中含有的MgCl2,应选用的试剂和操作方法是( ) A.加入适量Na2SO4后蒸发 B.加入适量NaOH溶液后过滤 C.加入过量NaOH溶液后蒸发 D.加入过量Na2CO3后过滤 |
|
| 6. 选择题 | 详细信息 |
|
进行过滤操作应选用的一组仪器是 A. 烧杯、酒精灯、试管、铁架台(铁圈)、漏斗 B. 滤纸、烧杯、试管夹、漏斗、玻璃棒 C. 烧杯、漏斗、玻璃棒、铁架台(铁圈)、滤纸 D. 滤纸、试管、漏斗、铁架台(铁圈)、玻璃棒 |
|
| 7. 选择题 | 详细信息 |
|
用NA表示阿伏加德罗常数的值,下列叙述正确的是( ) A.1mol氩气在标准状况下的体积约为11.2L B.20℃、101MPa状态下,32gO2和O3的混合气体所含原子数为2.5NA C.标准状况下,11.2LCCl4含有的原子数为3NA D.常温常压下,44gCO2含有的原子数为3NA |
|
| 8. 选择题 | 详细信息 |
|
胶体区别于其他分散系的最本质特征是( ) A. 能产生丁达尔效应 B. 粒子带电 C. 能透过滤纸 D. 分散质粒子的直径在1~100nm之间 |
|
| 9. 选择题 | 详细信息 |
|
有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,SO42-的物质的量浓度为0.7 mol·L-1,则此溶液中K+的物质的量浓度为( ) A. 0.1 mol·L-1 B. 0.15 mol·L-1 C. 0.2 mol·L-1 D. 0.25 mol·L-1 |
|
| 10. 选择题 | 详细信息 |
|
下列有关0.1mol/LNaOH溶液的叙述正确的是( ) A.1L该溶液中含有NaOH40g B.100mL该溶液中含有OH-0.01mol C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01mol/L D.在1L水中溶解4gNaOH即可配制得0.1mol/LNaOH溶液 |
|
| 11. 选择题 | 详细信息 |
|
下列有关实验室一般事故的预防和处理方法正确的是 A. 燃着的酒精灯打翻失火,应立即用水浇灭 B. 皮肤上沾有少量浓硫酸,可立即用NaOH冲洗。 C. 少量酸或碱滴到实验台上,立即用湿抹布擦净,再用水冲洗抹布 D. 蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却 |
|
| 12. 选择题 | 详细信息 |
|
下列反应中,既属于氧化还原反应,又属于离子反应的是( ) A. 甲烷与氧气的反应 B. 铝片与稀盐酸的反应 C. 灼热的碳与二氧化碳反应生成一氧化碳 D. 氢氧化钠溶液与稀盐酸的反应 |
|
| 13. 选择题 | 详细信息 |
|
己知丙酮(C3H6O)无色液体,可溶于水,密度小于1 g/mL,沸点约为56℃,要从水域丙酮的混合物里将丙酮分离出来,下列方法最合理的是 A. 蒸馏 B. 升华 C. 过滤 D. 蒸发 |
|
| 14. 选择题 | 详细信息 |
|
只用一种试剂就能将NaCl、BaCl2、KOH三种无色溶液区别开,此试剂是 A. Na2CO3 B. 盐酸 C. Fe2(SO4)3溶液 D. 硫酸 |
|
| 15. 选择题 | 详细信息 |
|
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( ) A. 铜器出现铜绿[Cu2(OH)2CO3] B. 铁制菜刀生锈 C. 大理石雕像被酸性较强的雨腐蚀毁坏 D. 铝锅表面生成致密的薄膜(Al2O3) |
|
| 16. 选择题 | 详细信息 | ||||||||||||||||||||
下图表示的一些物质或概念间的从属关系中正确的是
|
|||||||||||||||||||||
| 17. 选择题 | 详细信息 |
|
下列用双线桥表示电子转移的方向和数目不正确的是( ) A.  B. B. C.  D. D.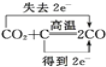 |
|
| 18. 选择题 | 详细信息 |
|
下列离子检验的方法正确的是( ) A.某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl- B.某溶液中加Ba(OH)2溶液生成蓝色沉淀,说明原溶液中有Cu2+ C.某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- D.某溶液中加稀硫酸溶液产生无色气体,说明原溶液中有CO32- |
|
| 19. 选择题 | 详细信息 |
|
已知下列溶液的溶质都是强电解质,这些溶液中的Cl-浓度与50mL 1mol·L-1 MgCl2溶液的Cl-浓度相等的是( ) A.150mL 1mol·L-1 NaCl溶液 B.75mL 2mol·L-1 CaCl2溶液 C.150mL 2mol·L-1 KCl溶液 D.75mL 1mol·L-1 AlCl3溶液 |
|
| 20. 选择题 | 详细信息 |
|
下列指定反应的离子方程式正确的是( ) A.Fe与稀硫酸反应:2Fe+6H+=Fe3++3H2↑ B.Cu与AgNO3溶液反应:Cu+2Ag+=Cu2++2Ag C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O D.向澄清石灰水中通入少量CO2:CO2+OH-=HCO3- |
|
| 21. 选择题 | 详细信息 |
|
下列反应中必须加入还原剂才能进行的是 A. O2→OH- B. Zn→Zn2+ C. H2→H2O D. CuO→CuCl2 |
|
| 22. 选择题 | 详细信息 |
|
下列反应中,水既不是氧化剂、也不是还原剂的氧化还原反应是 A. Mg+2H2O=Mg(OH)2+H2↑ B. 2F2+2H2O=4HF+O2 C. Na2O+H20=2NaOH D. 2Na2O2+2H2O=4NaOH+O2↑ |
|
| 23. 选择题 | 详细信息 |
|
在无色溶液中,下列离子能大量共存的是 A.Na+、NH4+ 、NO3-、MnO4- B.K +、 SO42-、Cl-、Mg2+ C.K +、 H+ 、 HCO3-、Br- D.Ba2+ 、Na+ 、OH-、CO32- |
|
| 24. 选择题 | 详细信息 |
|
下列有关阿伏伽德罗定律的说法不正确的是 A.同温同压下,相同质量的NO和C2H4(气体)体积相同 B.同温同压下,气体的密度之比等于摩尔质量之比 C.同温同压下,相同体积的H2和CO2的原子数之比为2:3 D.同温同体积的气体,若物质的量相同则压强相同 |
|
| 25. 填空题 | 详细信息 |
|
现有下列12种物质:①Fe;②CO2;③空气;④CaO;⑤HNO3;⑥Ca(OH)2;⑦碘酒:⑧CuSO4·5H2O;⑨乙醇:⑩NaHCO3;⑪Fe(OH)3胶体: (1)属于混合物的是___________(填序号,下同); (2)属于氧化物的是___________; (3)属于酸的是___________; (4)属于碱的是___________; (5)属于盐的是___________; (6)属于(或含有)有机物的是___________; (7)可出现丁达尔效应的是___________。 |
|
| 26. 填空题 | 详细信息 |
|
现有下列七种物质:①铝 ②蔗糖 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥红褐色的氢氧化铁胶体 ⑦HCl. (1)上述物质中属于电解质的有__________(填序号)。 (2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是________________________。 (3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH﹣═H2O,则该反应的化学方程式为______________________________。 (4)⑦的浓溶液与高锰酸钾发生反应的化学方程式为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O。 ①该反应中的氧化剂是________,氧化产物是_________。 ②浓盐酸在反应中显示出来的性质是____________。 ③产生0.1mol Cl2,则转移的电子的物质的量为_______mol。 |
|
| 27. 实验题 | 详细信息 |
|
实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL。 (1)配制溶液时,必须用到的仪器有天平、药匙、玻璃棒、烧杯、___。要完成本实验该同学应称出___gNaOH。 (2)使用容量瓶前必须进行的一步操作是___,具体操作方法为____。 (3)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是___。 A.转移溶液时不慎有少量洒到容量瓶外面 B.定容时俯视刻度线 C.未冷却到室温就将溶液转移到容量瓶并定容 D.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线 |
|
| 28. 实验题 | 详细信息 |
|
为除去粗盐中的Ca2+、Mg2+、SO42- 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量): (1)判断BaCl2已过量的方法是_______________________________________________。 (2)第④步中,相关的离子方程式是___________________________________________。 (3)若先用盐酸再过滤,将对实验结果产生影响,其原因是______________________________。 (4)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,下图是该同学转移溶液的示意图,其中的错误是____________________________________________。  |
|
最近更新



