2019-2020年高二上期第二次月考化学考题(陕西省咸阳百灵中学)
| 1. 选择题 | 详细信息 |
|
下列说法正确的是 A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 B.反应NH4HCO3(s) =NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol 能自发进行,原因是体系有自发向混乱度增大的方向转变的倾向 C.焓变和熵变都与反应的自发性有关,所以焓变和熵变均可以单独作为反应能否自发进行的判据 D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
|
| 2. 选择题 | 详细信息 |
|
下列各组物质,按强电解质、弱电解质、非电解质、既不是电解质又不是非电解质的顺序排列的是 A. NaOH、NaCl、SO2、NaCl溶液 B. BaSO4、SO3、CuSO4晶体、Na2O2 C. NaCl、H2S、CO2、Cu D. SO3、AgCl、NH3•H2O、Ag |
|
| 3. 选择题 | 详细信息 |
|
稀氨水中存在着下列平衡:NH3·H2O ①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgCl2固体。 A.①②③⑤ B.③⑥ C.③ D.③⑤ |
|
| 4. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.pH=0的溶液不存在 B.使用广泛pH试纸测得某溶液的pH=3.5 C.中性溶液的pH不一定等于7 D.酸或碱溶液在稀释时,溶液的pH均减小 |
|
| 5. 选择题 | 详细信息 |
|
下列说法正确的是 A.1 mol·L-1的稀硫酸中存在OH- B.Kw随溶液c(H+)和c(OH-)的变化而改变 C.水的电离只受温度影响,酸碱性对其无影响 D.Kw=10-14适用于任何温度、任何溶液 |
|
| 6. 选择题 | 详细信息 |
|
25 ℃时,水的电离达到平衡:H2O A.将纯水加热到95 ℃时,Kw变大,pH不变,水仍呈中性 B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 C.向纯水中加入少量碳酸钠固体,影响水的电离平衡,c(H+)减小,Kw不变 D.向纯水中加入醋酸钠固体或盐酸,均可抑制水的电离,Kw不变 |
|
| 7. 选择题 | 详细信息 |
|
pH=2的盐酸和pH=2的稀硫酸相比较,下列说法正确的是 A.两溶液的物质的量浓度相同 B.两溶液的c(H+)相同 C.等体积的两溶液分别与足量的Zn反应,产生H2的量不同 D.将两溶液均稀释100倍后,pH不同 |
|
| 8. 选择题 | 详细信息 |
|
常温下,4 L的pH=9的Ca(OH)2溶液与1 L的pH=13的NaOH溶液混合后,溶液中氢离子的浓度为 A.5×10-13 mol·L-1 B.2×10-12 mol·L-1 C.4×10-5 mol·L-1 D.4×10-9mol·L-1 |
|
| 9. 选择题 | 详细信息 |
|
下列说法正确的是 A.c(H+)>1.0×10-7 mol·L-1的溶液一定呈酸性 B.c(H+)·c(OH-)=1.0×10-14的溶液一定呈中性 C.中性溶液中的c(H+)一定等于1.0×10-7 mol·L-1 D.c(H+)=c(OH-)的溶液一定是中性溶液 |
|
| 10. 选择题 | 详细信息 |
|
下列说法正确的是 A.25 ℃水的电离常数是1.0×10-12 B.中性溶液的c(H+)= C.纯水在100 ℃时,c(H+)>10-7 mol·L-1,所以此时纯水中c(H+)>c(OH-) D.pH<7的溶液一定是酸溶液 |
|
| 11. 选择题 | 详细信息 |
|
下列四种溶液中,由水电离出的氢离子浓度之比(①:②:③:④)是 ①c(H+)=1 mol·L-1的盐酸 ②0.1 mol·L-1的盐酸 ③0.01 mol·L-1的NaOH溶液 ④c(OH-)=1 mol·L-1的NaOH溶液 A.1:10:100:1 B.1:10-1:10-12:10-14 C.14:13:12:14 D.14:3:2:1 |
|
| 12. 选择题 | 详细信息 |
|
pH=13的 强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为 A.9:1 B.1:11 C.1:9 D.11:1 |
|
| 13. 选择题 | 详细信息 |
pH=2的A、B两种酸溶液各1 mL,分别加水稀释到1 000 mL,其中pH与溶液体积V的关系如图所示。下列说法正确的是( )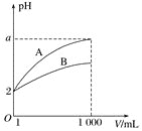 A.A、B两酸溶液的物质的量浓度一定相等 B.稀释后,A酸溶液的酸性比B酸溶液的酸性强 C.a=5时,A是强酸,B是弱酸 D.一定有关系:5>a>2 |
|
| 14. 选择题 | 详细信息 |
|
在25℃时,某稀溶液中由水电离产生的c(OH-)=10-10 mol•L-1.下列有关该溶液的叙述正确的是( ) A. 该溶液一定呈酸性 B. 该溶液中 C. 该溶液的pH可能为4也可能为10 D. 该溶液有可能呈中性 |
|
| 15. 选择题 | 详细信息 |
|
关于溶液的酸碱性说法正确的是 ( ) A.c(H+)很小的溶液一定呈碱性 B.PH=7的溶液一定呈中性 C.不能使酚酞试液变红的溶液一定呈酸性 D.c(OH-)= C(H+)的溶液一定呈中性 |
|
| 16. 计算题 | 详细信息 |
氢能的优点是燃烧热值高,无污染。目前工业制氢气的一个重要反应为CO(g)+H2O(g)===CO2(g)+H2(g) ΔH,反应过程和能量的关系如图所示: (1)CO(g)+H2O(g)===CO2(g)+H2(g) ΔH______(填“>”“<”或“=”)0。 (2)过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热________(填“相等”或“不相等”),原因是____________________________________________________________________。 (3)已知:H2(g)+ H2O(l)===H2O(g) ΔH=+44.0 kJ·mol-1 则H2(g)燃烧生成H2O(l)的热化学方程式为_________________________________________。 |
|
| 17. 计算题 | 详细信息 |
|
有下列物质的溶液:①CH3COOH ②HCl ③H2SO4 ④NaHSO4 (1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为____________(用序号表示,下同)。 (2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为___________,经测定溶液中c(CH3COO-)为1.4×10-3 mol/L,此温度下醋酸的电离常数Ka=____________,温度升高,Ka将_____(填“变大”“不变”或“变小”,下同),加入少量CH3COONa后c(H+)______,Ka______。 |
|
| 18. 计算题 | 详细信息 |
|
(1)在常温下的0.05 mol·L-1硫酸溶液中,c(H+)=_______mol·L-1,水电离出的c(H+)=___________mol·L-1,水电离出的c(OH-)=_________ mol·L-1。 (2)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时c(OH-)为_____________mol·L-1。若温度不变,滴入稀盐酸使c(H+)=5×10-4 mol·L-1,则溶液中c(OH-)为_______________mol·L-1,此时温度_______(填“高于”、“低于”或“等于”)25 ℃。 |
|
| 19. 综合题 | 详细信息 |
|
合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g) (1)①该反应的化学平衡常数表达式为________________。 ②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越______。 (2)某温度下,若把10 mol N2与30 mol H2置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的K=_________(可用分数表示)。能说明该反应达到化学平衡状态的是_______(填字母)。 a.容器内的密度保持不变 b.容器内压强保持不变 c.v正(N2)=2v逆(NH3) d.混合气体中c(NH3)不变 (3)对于合成氨反应而言,下列有关图像一定正确的是_________(选填序号)。 a. 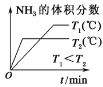 b. b.  c. c.  (4)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a______b(填“>”“=”或“<”,下同),Q1_____92.4。 |
|
最近更新



