жё…еҚҺеӨ§еӯҰдёӯеӯҰз”ҹж ҮеҮҶеӯҰжңҜиғҪеҠӣиҜҠж–ӯжҖ§жөӢиҜ•й«ҳдёүеҢ–еӯҰдёҠеҶҢејҖеӯҰиҖғиҜ•ж‘ёеә•иҖғиҜ•йўҳ
| 1. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҢ–еӯҰеҸҜд»Ҙи®©дәәзұ»з”ҹжҙ»жӣҙзҫҺеҘҪпјҢдёӢеҲ—жңүе…іеҢ–еӯҰзҹҘиҜҶзҡ„иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲ пјү A.зғӯзҡ„зәҜзўұжә¶ж¶ІеҸҜд»Ҙд»ЈжӣҝйӨҗжҙ—еҮҖдҪңеҺЁжҲҝвҖңжҙ—ж¶ӨеүӮвҖқ B.й“ҒзІүеҸҜеҒҡйЈҹе“ҒиўӢдёӯзҡ„вҖңжҠ—ж°§еүӮвҖқ C.CuSO4еӣ е…·жңүж°§еҢ–жҖ§пјҢж•…з”Ёе…¶еҲ¶жҲҗзҡ„жіўе°”еӨҡж¶ІеҸҜдҪңвҖңжқҖиҸҢеүӮвҖқ D.дәҡзЎқй…ёй’ е…·жңүиҮҙзҷҢжҖ§пјҢдҪҶзҒ«и…ҝиӮ еҠ е·ҘдёӯеҸҜеҠ е°‘йҮҸдҪңвҖңйҳІи…җеүӮвҖқгҖҒвҖңеҸ‘иүІеүӮвҖқ |
|
| 2. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗеҢ–еҗҲзү©Mзҡ„з»“жһ„з®ҖејҸеҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү A.MеҸҜд»ҘеҸ‘з”ҹеҸ–д»ЈгҖҒеҠ жҲҗгҖҒеҠ иҒҡгҖҒзј©иҒҡеҸҚеә” B.ж ёзЈҒе…ұжҢҜж°ўи°ұе…ұжңү9дёӘеҗёж”¶еі° C.1molMдёҺи¶ійҮҸжәҙж°ҙеҸҚеә”жңҖеӨҡж¶ҲиҖ—4molBr2 D.1molMдёҺи¶ійҮҸзҡ„NaOHжә¶ж¶ІеҸҚеә”жңҖеӨҡж¶ҲиҖ—3molNaOH |
|
| 3. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
XгҖҒYгҖҒZгҖҒWеӣӣз§Қзҹӯе‘Ёжңҹе…ғзҙ пјҢеҺҹеӯҗзҡ„ж ёз”өиҚ·ж•°дҫқж¬ЎеўһеӨҡпјҢXзҡ„дёҖз§ҚеҺҹеӯҗж— дёӯеӯҗпјҢYгҖҒZеҪўжҲҗзҡ„еҢ–еҗҲзү©е…·жңүжјӮзҷҪжҖ§пјҢе…¶дёӯзҡ„еҺҹеӯҗдёӘж•°жҜ”дёә1пјҡ1пјҢWзҡ„еҚ•иҙЁеёёз”ЁдәҺиҮӘжқҘж°ҙзҡ„жқҖиҸҢж¶ҲжҜ’пјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү A.XдёҺYгҖҒZгҖҒWеҪўжҲҗзҡ„еҢ–еҗҲзү©ж—ўжңүе…ұд»·еҢ–еҗҲзү©д№ҹжңүзҰ»еӯҗеҢ–еҗҲзү© B.XгҖҒYгҖҒWдёүе…ғзҙ еҪўжҲҗзҡ„й…ёйғҪжҳҜејұй…ё C.дёҠиҝ°е…ғзҙ зҡ„з®ҖеҚ•зҰ»еӯҗзҡ„еҚҠеҫ„еӨ§е°ҸйЎәеәҸдёәпјҡr(X)<r(Y)<r(Z)<r(W) D.ZгҖҒXеҪўжҲҗзҡ„еҢ–еҗҲзү©дёҺеҗ«й…ҡй…һзҡ„ж°ҙеҸҚеә”еҗҺе‘ҲзәўиүІпјҢз”ҹжҲҗзҡ„ж°”дҪ“иғҪдҪҝеёҰзҒ«жҳҹзҡ„жңЁжқЎеӨҚзҮғ |
|
| 4. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
дёӢеҲ—е®һйӘҢж“ҚдҪңеҸҠзҺ°иұЎе’Ңз»“и®әеқҮжӯЈзЎ®зҡ„жҳҜпјҲ пјү
|
||||||||||||||||
| 5. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗзЁҖзЎ«й…ёе’ҢзЁҖзЎқй…ёзҡ„ж··еҗҲж¶І25mLпјҢеҗ‘е…¶дёӯйҖҗжёҗеҠ е…Ҙй“ҒзІүпјҢдә§з”ҹж°”дҪ“зҡ„зү©иҙЁзҡ„йҮҸйҡҸй“ҒзІүиҙЁйҮҸеўһеҠ зҡ„еҸҳеҢ–еҰӮеӣҫжүҖзӨә(зЎқй…ёзҡ„иҝҳеҺҹдә§зү©дёәNOпјҢеҝҪз•ҘеҸҚеә”дёӯзҡ„жә¶ж¶ІдҪ“з§ҜеҸҳеҢ–)гҖӮдёӢеҲ—жңүе…іиҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү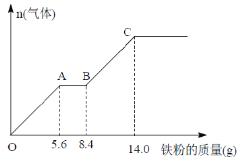 A.OAж®өдә§з”ҹзҡ„ж°”дҪ“жҳҜNOпјҢABж®өеҸ‘з”ҹзҡ„еҸҚеә”дёәFeпјӢ2Fe3пјӢ=3Fe2пјӢпјҢBCж®өдә§з”ҹзҡ„ж°”дҪ“жҳҜH2 B.з”ұжӯӨжҺЁж–ӯиҜҘжқЎд»¶дёӢпјҢж°§еҢ–жҖ§пјҡNO3-ејәдәҺFe3пјӢ C.OAж®өдёҺBCж®өдә§з”ҹзҡ„ж°”дҪ“зҡ„дҪ“з§ҜжҜ”дёә1пјҡ1 D.CзӮ№жә¶иҙЁзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰдёә10 molВ·L-1 |
|
| 6. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗж¶ІжҖҒиӮј(N2H4)зҮғж–ҷз”өжұ иў«е№ҝжіӣеә”з”ЁдәҺеҸ‘е°„йҖҡи®ҜеҚ«жҳҹгҖҒжҲҳз•ҘеҜјеј№зӯүиҝҗиҪҪзҒ«з®ӯдёӯгҖӮе…¶дёӯд»ҘеӣәдҪ“ж°§еҢ–зү©дёәз”өи§ЈиҙЁпјҢз”ҹжҲҗзү©дёәж— жҜ’ж— е®ізҡ„зү©иҙЁгҖӮдёӢеҲ—жңүе…іиҜҘз”өжұ зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү A.aз”өжһҒдёҠзҡ„з”өжһҒеҸҚеә”ејҸдёәN2H4пјӢ2O2-пјӢ4e-=N2вҶ‘пјӢ2H2O B.з”өжұ еҶ…з”өи·ҜдёӯпјҢз”өжөҒж–№еҗ‘пјҡз”өжһҒaвҶ’з”өжһҒb C.еҪ“з”өжһҒaдёҠж¶ҲиҖ—1molN2H4ж—¶пјҢз”өжһҒbдёҠиў«ж°§еҢ–зҡ„O2еңЁж ҮеҮҶзҠ¶еҶөдёӢдҪ“з§Ҝдёә22.4L D.bжһҒйҷ„иҝ‘зҡ„pHеҖјеҸҳеӨ§ |
|
| 7. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
еёёжё©дёӢпјҢе°ҶNaOHеӣәдҪ“йҖҗжёҗеҠ еҲ°жҹҗжө“еәҰзҡ„дёҖе…ғй…ёHAжә¶ж¶ІдёӯпјҢжөӢеҫ—ж··еҗҲжә¶ж¶Ізҡ„pHдёҺеҫ®зІ’жө“еәҰlg A.Ka(HA)зҡ„ж•°йҮҸзә§дёә10пјҚ5 B.AзӮ№жүҖиЎЁзӨәзҡ„жә¶ж¶Ідёӯпјҡc(HA)>c(A-)>c(NaпјӢ)>c(OH-) C.BзӮ№жүҖиЎЁзӨәзҡ„жә¶ж¶Ідёӯпјҡc(HпјӢ)пјқc(HA)пјӢc(OH-)пјҚc(NaпјӢ) D.д»ҺAзӮ№еҲ°CзӮ№пјҢж°ҙзҡ„з”өзҰ»зЁӢеәҰе…ҲеўһеӨ§еҗҺеҮҸе°Ҹ |
|
| 8. е®һйӘҢйўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗе®һйӘҢе°Ҹз»„жҺўз©¶иҝҮйҮҸж°Ёж°”е’Ңж°Ҝж°”зҡ„еҸҚеә”пјҢжҺЁжөӢе…¶дә§зү©дёӯеҸҜиғҪеҗ«жңүNH4ClгҖӮи®ҫи®Ўе®һйӘҢиЈ…зҪ®еҰӮдёӢпјҡ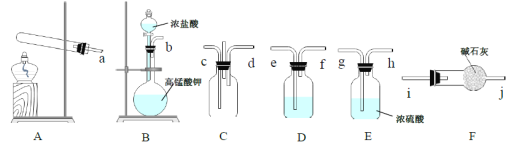 пјҲ1пјүе®һйӘҢе®Өз”ЁAиЈ…зҪ®еҲ¶еҸ–ж°Ёж°”пјҢе…¶дёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә___гҖӮ пјҲ2пјүе®һйӘҢе®Өз”ЁBиЈ…зҪ®еҲ¶еӨҮCl2зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜ___пјҢиЈ…зҪ®Dдёӯзҡ„иҜ•еүӮдёә___пјҢе…¶дҪңз”Ёдёә___гҖӮ пјҲ3пјүдёәдәҶи®©ж°Ёж°”е’Ңж°Ҝж°”ж··еҗҲе……еҲҶпјҢеҗҲзҗҶзҡ„иЈ…зҪ®иҝһжҺҘйЎәеәҸжҳҜ(з”Ёе°ҸеҶҷеӯ—жҜҚеЎ«еҶҷ)пјҡ___жҺҘ___жҺҘ___жҺҘcжҺҘdжҺҘ___жҺҘ___жҺҘ___жҺҘ___жҺҘ___гҖӮ пјҲ4пјүеңЁе®һйӘҢиҝҮзЁӢдёӯпјҢз”ІеҗҢеӯҰеңЁиЈ…зҪ®Cдёӯй—ҙеҜјж°”з®Ўзҡ„дёҠж–№и§ӮеҜҹеҲ°жңүзҷҪйӣҫеҮәзҺ°пјҢеҺҹеӣ жҳҜ___пјҢд№ҷеҗҢеӯҰеңЁиЈ…зҪ®CеҶ…и§ӮеҜҹеҲ°жңүзҷҪзғҹз”ҹжҲҗпјҢеҺҹеӣ жҳҜ___(иҜ·з”ЁеҢ–еӯҰж–№зЁӢејҸиЎЁиҫҫ)гҖӮ пјҲ5пјүеҰӮеӣҫпјҢиҜҘиЈ…зҪ®еӯҳеңЁжҳҺжҳҫзҡ„дёҚи¶іпјҢиҜ·жҢҮеҮә___гҖӮ пјҲ6пјүдёәдәҶиҝӣдёҖжӯҘйӘҢиҜҒиЈ…зҪ®Cдёӯдә§з”ҹзҡ„еӣәдҪ“дёӯжҳҜеҗҰеҗ«жңүNH4ClпјҢжүҖз”ЁиҜ•еүӮйҷӨAgNO3жә¶ж¶ІеӨ–пјҢиҝҳйңҖ___пјҢиҜ•еүӮзҡ„жӯЈзЎ®ж»ҙеҠ йЎәеәҸжҳҜ___гҖӮ |
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
2019е№ҙиҜәиҙқе°”еҢ–еӯҰеҘ–жҺҲдәҲиӢұгҖҒзҫҺгҖҒж—ҘзұҚзҡ„дёүдҪҚ科еӯҰ家пјҢд»ҘиЎЁеҪ°д»–们еңЁй”ӮзҰ»еӯҗз”өжұ з ”еҸ‘йўҶеҹҹеҒҡеҮәзҡ„иҙЎзҢ®гҖӮй”ӮзҰ»еӯҗз”өжұ е№ҝжіӣеә”з”ЁдәҺжүӢжңәгҖҒ笔记жң¬гҖҒз”өеҠЁжұҪиҪҰгҖҒжҷәиғҪжңәеҷЁдәәзӯүдә§е“ҒдёӯгҖӮе·ІзҹҘй’ҙй…ёй”Ӯ(LiCoO2)з”өжұ дёӯиҝҳеҗ«жңүй“қз®”гҖҒзҹіеўЁгҖҒеЎ‘ж–ҷзӯүпјҢеҲ©з”Ёд»ҘдёӢе·ҘиүәжөҒзЁӢеӣһ收еәҹж—§з”өжұ дёӯзҡ„йҮ‘еұһиө„жәҗгҖӮ е·ІзҹҘпјҡLiCoO2еңЁй…ёжҖ§жә¶ж¶Ідёӯжңүејәж°§еҢ–жҖ§гҖӮ пјҲ1пјүзІүзўҺеәҹж—§з”өжұ еҗҺзғӯеӨ„зҗҶеҸҜд»ҘйҷӨеҺ»___(еЎ«зү©иҙЁзҡ„еҗҚз§°)гҖӮ пјҲ2пјүеҶҷеҮәз”ұж»Өж¶ІIеҫ—еҲ°Al(OH)3зҡ„зҰ»еӯҗж–№зЁӢејҸ___гҖӮ пјҲ3пјүз”ЁзЎ«й…ёй…ёжөёж—¶иҰҒжҺ§еҲ¶жё©еәҰдёә80в„ғпјҢеҺҹеӣ жҳҜ___пјҢеҶҷеҮәй…ёжөёж—¶еҸ‘з”ҹзҡ„дё»иҰҒж°§еҢ–иҝҳеҺҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ___гҖӮ пјҲ4пјүеңЁз©әж°”дёӯз……зғ§дәҢж°ҙеҗҲиҚүй…ёй’ҙдёҖе®ҡз”ЁдёҚеҲ°зҡ„д»ӘеҷЁжҳҜ___(еЎ«еӯ—жҜҚ)гҖӮ A.и’ёеҸ‘зҡҝ B.зҺ»з’ғжЈ’ C.зғ§жқҜ D.з“·еқ©еҹҡ пјҲ5пјүе·ІзҹҘLi2CO3еҫ®жә¶дәҺж°ҙпјҢе…¶йҘұе’Ңжә¶ж¶Ізҡ„жө“еәҰдёҺжё©еәҰе…ізі»и§ҒдёӢиЎЁгҖӮдёәдәҶеҮҸе°‘зўій…ёй”Ӯзҡ„жҚҹеӨұпјҢеӣҫдёӯвҖңж“ҚдҪңвҖқеә”дёә___пјҢ90в„ғж—¶Ksp(Li2CO3)зҡ„еҖјдёә___гҖӮ  |
|
| 10. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
з…ӨзҮғзғ§дә§з”ҹзҡ„зғҹж°”дёӯеҗ«жңүSO2е’ҢNOxпјҢз”ЁNaOHгҖҒNaClOгҖҒCa(ClO)2зӯүжә¶ж¶ІдҪңдёәеҗёж”¶еүӮеҸҜеҗҢж—¶еҜ№зғҹж°”иҝӣиЎҢи„ұзЎ«гҖҒи„ұзЎқгҖӮ пјҲ1пјүдёӢеҲ—е…ідәҺеҗёж”¶SO2иҝҮзЁӢеҸ‘з”ҹзҡ„жңүе…іеҸҚеә”пјҢз”ЁдёӢеҲ—ж–№зЁӢејҸиЎЁзӨәпјҡ в‘ SO2(g)пјӢ2OH-(aq)пјқSO32-(aq)пјӢH2O(l) k1 в‘ЎClO-(aq)пјӢSO32-(aq)пјқSO42-(aq)пјӢCl-(aq) k2 в‘ўCaSO4(s) k1гҖҒk2гҖҒk3еҲҶеҲ«иЎЁзӨәеҸҚеә”в‘ гҖҒв‘ЎгҖҒв‘ўзҡ„еҢ–еӯҰе№іиЎЎеёёж•°пјҢеҲҷеҸҚеә”пјҡSO2(g)пјӢCa2пјӢ(aq)пјӢClO-(aq)пјӢ2OH-(aq)=CaSO4(s)пјӢH2O(l)пјӢCl-(aq)зҡ„еҢ–еӯҰе№іиЎЎеёёж•°K=___(з”Ёk1гҖҒk2гҖҒk3иЎЁзӨә)гҖӮ пјҲ2пјүж ҮеҮҶзҠ¶еҶөдёӢпјҢжҠҠSO2йҖҡе…Ҙ11.2mLж°ҙдёӯеҲ¶еҫ—йҘұе’Ңжә¶ж¶ІпјҢжөӢеҫ—е…¶pHпјқ0.74гҖӮе·ІзҹҘпјҡж ҮеҮҶзҠ¶еҶөдёӢSO2еңЁж°ҙдёӯзҡ„жә¶и§ЈеәҰжҢүдҪ“з§ҜжҜ”дёә1пјҡ67.2(еҚіV(H2O)пјҡV(SO2)пјқ1пјҡ67.2)гҖӮ в‘ еҶҷеҮәиҜҘжә¶ж¶ІдёӯеӯҳеңЁзҡ„з”өзҰ»е№іиЎЎ____гҖӮ в‘Ўе·ІзҹҘйҘұе’Ңжә¶ж¶Ідёӯзҡ„SO2жңү пјҲ3пјүSO2зҡ„ж°ҙжә¶ж¶ІдёӯеӯҳеңЁжӯ§еҢ–еҸҚеә”пјҡ3SO2пјӢ2H2O aпјҡSO2пјӢ4I-пјӢ4HпјӢпјқSвҶ“пјӢ2I2пјӢ2H2O bпјҡI2пјӢ2H2OпјӢSO2пјқSO42-пјӢ2I-пјӢ4HпјӢ ж¬ІжҺўз©¶еҸҚеә”aе’Ңbзҡ„еҸҚеә”йҖҹзҺҮдёҺжӯ§еҢ–еҸҚеә”зҡ„йҖҹзҺҮзҡ„е…ізі»пјҢи®ҫи®Ўе®һйӘҢеҰӮдёӢпјҡе°Ҷ18mLSO2зҡ„ж°ҙжә¶ж¶ІеҲҶеҲ«еҠ е…Ҙ2mLдёӢеҲ—иҜ•еүӮдёӯпјҢеҜҶй—ӯж”ҫзҪ®пјҢи§ӮеҜҹзҺ°иұЎгҖӮ(е·ІзҹҘI2жҳ“жә¶дәҺKIжә¶ж¶ІпјҢжә¶ж¶Іе‘ҲжЈ•иӨҗиүІ) 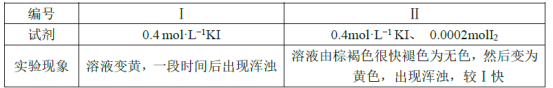 е®ҢжҲҗдёӢеҲ—й—®йўҳпјҡ в‘ з”ұе®һйӘҢзҺ°иұЎеҸҜеҫ—еҮәеҸҚеә”aдёҺеҸҚеә”bзҡ„йҖҹзҺҮпјҡv(a)___v(b)(еЎ«вҖң>вҖқвҖңп№ӨвҖқжҲ–вҖңпјқвҖқ)гҖӮ в‘ЎжөӢеҫ—еҸҚеә”3SO2пјӢ2H2O  в‘ўдёӢеҲ—еҸҷиҝ°иғҪиҜҙжҳҺ3SO2(aq)пјӢ2H2O(l) A.з”ҹжҲҗ1.5molSO2зҡ„еҗҢж—¶ж¶ҲиҖ—1molH2SO4 B.еҸҚеә”иҝҮзЁӢдёӯпјҢжә¶ж¶Ідёӯзҡ„еҲҶеӯҗжҖ»ж•°дёҚеҶҚеҸҳеҢ– C.жҒ’жё©жҒ’е®№ж—¶пјҢж··еҗҲжә¶ж¶ІдёӯзЎ«й…ёзҡ„еҜҶеәҰдҝқжҢҒдёҚеҸҳ D.з»қзғӯжҒ’е®№ж—¶пјҢеҸҚеә”зҡ„еҢ–еӯҰе№іиЎЎеёёж•°дёҚеҶҚеҸҳеҢ– пјҲ4пјүиӢҘжҠҠNaOHеҗёж”¶SO2еҗҺзҡ„зўұжә¶ж¶ІиҝӣиЎҢз”өи§ЈпјҢиЈ…зҪ®еҰӮеӣҫжүҖзӨәгҖӮе…¶дёӯSO2зҡ„зўұеҗёж”¶ж¶Ідёӯеҗ«жңүNaHSO3е’ҢNa2SO3зҡ„жө“еәҰеқҮдёә0.05molВ·L-1гҖӮеҪ“з”өи·ҜдёӯйҖҡиҝҮ0.05molз”өеӯҗж—¶пјҢйҳіжһҒз”ҹжҲҗзҡ„ж°”дҪ“еңЁж ҮеҮҶзҠ¶еҶөдёӢзҡ„дҪ“з§Ҝдёә___LпјҢbе®Өдёӯc(SO32-)___(еЎ«вҖңеўһеӨ§вҖқвҖңеҮҸе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқ)пјҢжә¶ж¶Ідёӯпјҡc(NaпјӢ)пјҚ___=0.05molВ·L-1(з”Ёеҫ®зІ’жө“еәҰзҡ„е…ізі»ејҸиЎЁзӨә)гҖӮ  |
|
| 11. жҺЁж–ӯйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
AгҖҒBгҖҒCгҖҒDдёәеҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§зҡ„еӣӣз§Қе…ғзҙ пјҢз®ҖеҚ•зҰ»еӯҗA2-е’ҢDпјӢзӣёе·®дёҖдёӘз”өеӯҗеұӮпјҢBгҖҒCдёәеҗҢе‘Ёжңҹе…ғзҙ пјҢBеҺҹеӯҗж ёеӨ–з”өеӯҗжҖ»ж•°жҳҜжңҖеӨ–еұӮз”өеӯҗж•°зҡ„3еҖҚпјҢCе…ғзҙ зҡ„еҺҹеӯҗжңҖеӨ–еұӮжңүдёҖдёӘжңӘжҲҗеҜ№з”өеӯҗгҖӮиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүеҹәжҖҒBеҺҹеӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғејҸдёә___гҖӮ пјҲ2пјүAжңүдёӨз§ҚеҗҢзҙ ејӮеҪўдҪ“пјҢе…¶дёӯжІёзӮ№жңҖй«ҳзҡ„жҳҜ___пјҢеҺҹеӣ жҳҜ___гҖӮ пјҲ3пјүBгҖҒCеҸҜз»„жҲҗеҺҹеӯҗдёӘж•°жҜ”дёә1пјҡ3зҡ„еҢ–еҗҲзү©EпјҢе…¶з”өеӯҗејҸдёә___пјҢEжә¶дәҺж°ҙжңүзҷҪйӣҫз”ҹжҲҗпјҢеҶҷеҮәе®ғдёҺж°ҙеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ___гҖӮ пјҲ4пјүеҢ–еҗҲзү©C2Aзҡ„з«ӢдҪ“жһ„еһӢдёә___пјҢдёӯеҝғеҺҹеӯҗзҡ„д»·з”өеӯҗеҜ№ж•°дёә___пјҢз”ЁеҚ•иҙЁCдёҺж№ҝж¶Ұзҡ„Na2CO3жә¶ж¶ІеҸҚеә”еҸҜеҲ¶еҫ—C2AпјҢе…¶еҸҚеә”ж–№зЁӢејҸдёә___гҖӮ пјҲ5пјүAе’ҢDиғҪеӨҹеҪўжҲҗеҢ–еҗҲзү©FпјҢе…¶жҷ¶иғһз»“жһ„еҰӮеӣҫжүҖзӨәпјҢжҷ¶иғһеҸӮж•°a=0.60nmпјҢFзҡ„еҢ–еӯҰејҸдёә___пјҢжҷ¶иғһдёӯAеҺҹеӯҗзҡ„й…ҚдҪҚж•°дёә___пјҢеҲ—ејҸи®Ўз®—жҷ¶дҪ“Fзҡ„еҜҶеәҰ___(gВ·cm-3)гҖӮ  |
|
| 12. жҺЁж–ӯйўҳ | иҜҰз»ҶдҝЎжҒҜ |
й…ёй…җжҳҜз”ұдёҖдёӘжҲ–дёӨдёӘеҲҶеӯҗзҡ„й…ёеҺ»жҺүдёҖеҲҶеӯҗж°ҙиҖҢеҪўжҲҗзҡ„еҢ–еҗҲзү©пјҢдёҖз§Қж–°иҚҜзү©Mз”ұиҠійҰҷж—ҸеҢ–еҗҲзү©AеҗҲжҲҗпјҢе…¶и·ҜзәҝеӣҫеҰӮеӣҫпјҡ е·ІзҹҘдёӢеҲ—дҝЎжҒҜпјҡ в‘ AгҖҒBгҖҒCгҖҒDеқҮдёәиҠійҰҷеҢ–еҗҲзү©дё”йғҪеҗ«дёӨдёӘеҸ–д»ЈеҹәпјҢе…¶дёӯDж—ўиғҪеҸ‘з”ҹ银й•ңеҸҚеә”еҸҲиғҪдёҺFeCl3жә¶ж¶ІеҸ‘з”ҹжҳҫиүІеҸҚеә”гҖӮ в‘ЎR1COR2(H) в‘ўRX пјҲ1пјүAзҡ„еҗҚз§°жҳҜ___пјҢCдёӯжүҖеҗ«зҡ„е®ҳиғҪеӣўзҡ„еҗҚз§°жҳҜ___пјҢDгҖҒEзҡ„з»“жһ„з®ҖејҸеҲҶеҲ«дёә___гҖҒ___гҖӮ пјҲ2пјүEвҶ’FдёҺGвҶ’Hзҡ„еҸҚеә”зұ»еһӢеҲҶеҲ«жҳҜ___гҖҒ___гҖӮ пјҲ3пјүAз”ҹжҲҗBзҡ„еҢ–еӯҰж–№зЁӢејҸдёә___гҖӮ пјҲ4пјүеҗҲжҲҗи·Ҝзәҝдёӯи®ҫи®ЎAвҶ’BпјҢеҶҚд»ҺCвҶ’Dзҡ„зӣ®зҡ„жҳҜ___гҖӮ пјҲ5пјүDзҡ„еҗҢеҲҶејӮжһ„дҪ“дёӯеҗ«жңүиӢҜзҺҜзҡ„иҝҳжңү___з§ҚгҖӮ(дёҚиҖғиҷ‘з«ӢдҪ“ејӮжһ„) пјҲ6пјүеҲ©з”ЁдёҠиҝ°дҝЎжҒҜпјҢд»ҘеҜ№иӢҜдәҢз”ІйҶҮдёәеҺҹж–ҷпјҢеҲ¶еӨҮеҢ–еҗҲзү©пјҡ A |
|
й«ҳдёӯеҢ–еӯҰ иҜ•еҚ·жҺЁиҚҗ
- й«ҳдәҢеҢ–еӯҰдёӢеҶҢиҜҫж—¶з»ғд№ ж‘ёеә•иҖғиҜ•йўҳ
- 2018иҮі2019е№ҙй«ҳдёҖеҗҺеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғйўҳеҗҢжӯҘи®ӯз»ғпјҲзҰҸе»әзңҒе®Ғеҫ·еёӮйғЁеҲҶдёҖзә§иҫҫж ҮдёӯеӯҰпјү
- дёҠжө·еёӮ2016е№ҙй«ҳдәҢеҢ–еӯҰеҗҺеҚҠжңҹжңҹдёӯиҖғиҜ•еёҰеҸӮиҖғзӯ”жЎҲдёҺи§Јжһҗ
- 2017-2018е№ҙй«ҳдәҢеүҚеҚҠжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰиҖғиҜ•е®Ңж•ҙзүҲпјҲжІіеҚ—зңҒеҚ—йҳіеёӮпјү
- 2019зүҲеҝ…дҝ®з¬¬дёҖеҶҢпјҲдё“йўҳ1 жң¬дё“йўҳеӨҚд№ жҸҗеҚҮ-й«ҳдёӯеҢ–еӯҰиӢҸж•ҷпјү
- жӯҰжұүеёӮй«ҳдәҢеҢ–еӯҰдёӢеҶҢжңҹдёӯиҖғиҜ•еҲ·йўҳз»ғд№
- 2016-2017е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲдёҠжө·еёӮйҮ‘еұұдёӯеӯҰпјү
- 2018-2019е№ҙй«ҳдәҢдёҠеӯҰжңҹ1жңҲиҙЁйҮҸжЈҖжөӢеҢ–еӯҰе…Қиҙ№иҜ•еҚ·пјҲеӣӣе·қзңҒеҚ—е……еёӮйҳҶдёӯдёӯеӯҰпјү
жңҖиҝ‘жӣҙж–°



