2019届高三二诊模拟考试理综-化学免费试卷完整版(四川省宜宾市第四中学)
| 1. | 详细信息 |
|
中国传统文化中的“笔、墨、纸、砚”被称为“文房四宝”。下列说法错误的是 A. 毛笔中羊毫的主要成分是蛋白质 B. 墨中炭黑性质稳定可使古代字画长期保存而不褪色 C. 宣纸制作工序中的“加碱蒸煮”主要发生化学变化 D. 砚石中含有二氧化硅,结构式为O=Si=O |
|
| 2. | 详细信息 |
|
检查司机是否酒后驾车的反应原理是:C2H5OH+4CrO3+6H2SO4=2Cr2(SO4)3+2CO2↑+9H2O。NA表示阿伏加德罗常数的值,下列说法正确的是 A. 0.1 mol C2H5OH中含OH-数目为0.1 NA B. 25℃时,pH=1的H2SO4溶液中含有H+的数目为0.1 NA C. 1.8 g H2O中含有共用电子对数目为0.2 NA D. 生成4.48 L CO2气体时,转移电子数目为1.2 NA |
|
| 3. | 详细信息 | |||||||||||||||
下列实验操作规范且能达到目的是
|
||||||||||||||||
| 4. | 详细信息 |
|
X、Y、Z、M、G五种短周期元素原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子;Y、G的单质或两元素之间形成的化合物可作水消毒剂。下列叙述正确的是 A. 元素M的氧化物对应的水化物酸性比G的弱 B. 化合物Z2M、MY2中化学键的类型相同 C. ZX与水的反应属于氧化还原反应 D. 简单离子半径的大小顺序:X<Y<Z<M<G |
|
| 5. | 详细信息 |
在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是 A. 以铅蓄电池为电源,则a极为Pb电极 B. 石墨Ⅱ电极附近的pH逐渐减小 C. 阳极反应为CH3CHO+H2O-2e-=CH3COOH+2H+ D. 每处理含8.8g乙醛的废水,转移电子的数目为0.4NA |
|
| 6. | 详细信息 |
常温下,用0. 1000 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示(饱和H2CO3溶液pH=5.6)。下列有关叙述正确的是  A. 若c(Na2CO3)=0.1000 mol·L-1,则H2CO3的Ka2数量级约为10-6 B. c点处溶液中一定有:c(Na+)=2c(CO32-)+c(HCO3-) C. a、c两点水的c(OH-)之比为10-11.6 :10-7 D. 若z=5.6,则d点有c(Na+)=c(Cl-)>c(H2CO3)>c(OH-) |
|
| 7. | 详细信息 |
对伞花烃(图I)常用作染料、医药、香料的中间体。下列说法错误的是 A. 常温对伞花烃呈液态且难溶于水 B. 图Ⅱ物质的一氯代物有5种结构 C. 对伞花烃最多有9个碳原子共平面 D. 图中氢化反应既是加成反应又是还原反应 |
|
| 8. | 详细信息 |
|
元素铬及其化合物工业用途广泛,但含+6价铬的污水会损害环境,必须进行处理。某工厂的处理工艺流程如下: (1)N2H4的电子式为___________。 (2)下列溶液中,可以代替上述流程中N2H4的是___________。(填选项序号) A.FeSO4溶液 B.浓HNO3溶液 C.酸性KMnO4溶液 D.Na2SO3溶液 (3)已知加入N2H4的流程中,N2H4转化为无污染的物质,则该反应中氧化剂与还原剂的物质的量之比为___________。 (4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。 ①已知含铬酸性废水中存在着Cr2O72-和CrO42-相互转化的平衡,请用离子方程式表示它们之间的转化反应___________; ②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为____________写化学式)。 (5)工业上可用电解法来处理含Cr2O 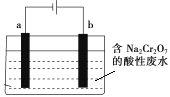 ①装置中b电极的材料是________(填“铁”或“石墨”)。 ②上述处理过程中,Cr2O |
|
| 9. | 详细信息 |
|
利用氢气对废气进行脱碳处理可实现绿色环保、废物利用,对于减少雾霾也具有重要意义。 (1)汽车尾气的主要污染物为NO,用H2催化还原NO可以达到消除污染的目的。 已知:2NO(g) 2H2O(l)===2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1 写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是______________。 (2)某研究小组模拟研究如下:向2 L恒容密闭容器中充入2 mol NO发生反应2NO(g)  ①T2下,在0~5 min内,v(O2)=______________mol·L-1·min-1;该温度下反应N2(g)+O2(g) ②该反应进行到M点放出的热量______________进行到W点放出的热量(填“>”、“<”或“=”)。 M点时再加入一定量NO,平衡后NO的转化率______________(填“变大”、“变小”或“不变”)。 ③反应开始至达到平衡的过程中,容器中下列各项发生变化的是______________(填序号)。 a.混合气体的密度 b.逆反应速率 c.单位时间内,N2和NO的消耗量之比 d.气体的平均相对分子质量 (3)氢气作为一种理想燃料,但不利于贮存和运输。利用氢能需要选择合适的储氢材料,镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) A.增加LaNi5H6(s)的量 B.升高温度 C.使用催化剂 D.减小压强 |
|
| 10. | 详细信息 |
以红土镍矿(主要成分为NiS、FeS和SiO2等) 为原料制备兰尼镍的工艺流程如下所示。 (1)形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________。 (2)Ni2O3有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+,则产生的气体为______(填化学式)。 (3) 滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体时所有反应的离子方程式:__________________________,_________________________。 (4) 已知: 3Fe2+ +2[Fe(CN)6]3-==Fe3[Fe(CN)6]2↓(蓝色沉淀);4Fe3++3[Fe(CN)6]4-==Fe4[Fe(CN)6]3↓(蓝色沉淀)。下列可以用于检验滤液C 中金属阳离子的试剂有____________(填标号) a.KSCN溶液 b.K3[Fe(CN)6] c.K4[Fe(CN)6] d.苯酚 (5)兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金。碱浸镍铝合金后,残铝量对兰尼镍的催化活性有重大影响,根据下图分析,残铝量在_____范围内催化活性最高,属于优质产品。  (6) 仿照下面示例,设计从浸出液E 回收氧化铝的流程: 浸出液E_________________。 (示例: |
|
| 11. | 详细信息 |
中国是最早发现并使用青铜器的国家。司母戊鼎是迄今为止出土的世界上最大、最重的青铜礼器,享有“镇国之宝”的美誉(如图1)。 (1)Cu原子的外围电子排布式为_______。 (2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是_______,I3远大于I2的原因是_______。 (3)图3是某含铜配合物的晶体结构示意图。 ①晶体中H2O和SO42-的中心原子的杂化类型为_______,试判断H2O和SO42-的键角大小关系并说明原因_______。 ②图3中的氢键有(H2O)O—H···O(H2O)和_______。 ③写出该配合物的化学式_______。 (4)一种铜的氯化物晶胞结构如下图所示。 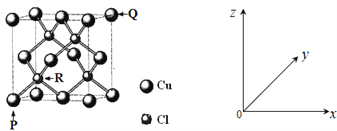 该化合物的化学式为_______,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、 ( |
|
| 12. | 详细信息 |
E是一种环保型塑料,其合成路线如下: 已知:①  ② 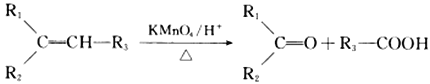 (R1、R2、R3、R为烃基) (R1、R2、R3、R为烃基)请回答下列问题: (1)A中官能团的名称是____________,检验该官能团的试剂为___________________。 (2)反应①的化学方程式是:______________________________,其反应类型为________________,在反应①中,还可以得到另一种分子式为C10H16的化合物,其结构简式为___________________。 (3)已知, (4)写出反应④的化学方程式:______________________________。 (5)C的同分异构体X满足下列条件: ①常温下,与碳酸钠溶液反应放出气体; ②能发生银镜反应。则符合条件的X共有________种。其核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,则X的结构简式为________________。 (6)参照E的上述合成路线,设计一条由4一甲基一3一戊酮酸为起始原料制备 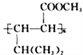 的合成路线(无机试剂任选)_________________________________________。 的合成路线(无机试剂任选)_________________________________________。 |
|
最近更新



