宁夏高三化学2019年上册期中考试网络考试试卷
| 1. 选择题 | 详细信息 |
|
运用化学知识对其进行的分析不合理的是( ) A.商代后期铸造出工艺精湛的司母戊鼎,该鼎属于铜合金制品 B.灼热的炭与CO2反应、Ba(OH)2·8H2O与NH4Cl的反应均可设计成原电池 C.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成 D.地沟油经过分离提纯后可制成生物柴油 |
|
| 2. 选择题 | 详细信息 |
|
下列关于胶体的叙述正确的是 A. 过滤实验可以据此把胶体、溶液分开 B. 胶体和溶液的本质区别是胶体能发生丁达尔现象 C. 用渗析的方法净化胶体时,使用半透膜只能让小分子和离子通过 D. 胶体带电,故在电场作用下会产生电泳现象 |
|
| 3. 选择题 | 详细信息 |
|
下列有关物质的分类与性质的说法正确的是( ) A.液氯、冰醋酸、C4H8均属于纯净物 B.Na2O、Fe2O3、Al2O3属于碱性氧化物 C.常用投加明矾、硫酸铁等电解质的方法处理浑浊的水 D.蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 |
|
| 4. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是() A.通常状况下,11.2 LCl2与足量NaOH 溶液反应时转移的电子数为0.5 NA B.0.1mol熔融状态下的NaHSO4中含有的阴离子数为0.2NA C.标准状况下,2.24LHF中含有的极性键数目为0.1NA D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA |
|
| 5. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法错误的是() A.用惰性电极电解CuSO4溶液后,如果加入0.1 molCu(OH)2能使溶液复原,则电路中转移电子数为0.2NA B.100g质量分数为46%的乙醇溶液中含有氢原子数为12NA C.工业合成氨每断裂NA个N≡N键,同时断裂6NA个N-H键,则反应达到平衡 D.100mL 12mol/L的浓HNO3与过量Cu反应,转移的电子数大于0.6NA |
|
| 6. 选择题 | 详细信息 | ||||||||||||||||||||
下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是
|
|||||||||||||||||||||
| 7. 选择题 | 详细信息 |
|
下列反应的离子方程式正确的是 A. NaHS溶液中滴加少量的硫酸铜溶液:2HS-+Cu2+═CuS ↓+H2S↑ B. 将NO2气体通入H2O中:3NO2+H2O═2H++NO3-+O2↑ C. ICl和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-═I-+ClO-+H2O D. 1.5 mol·L-1 100 mL的FeBr2溶液中通入3.36 L(标准状况)Cl2:2Br-+Cl2═Br2+2Cl- |
|
| 8. 选择题 | 详细信息 |
高铁酸钾的生产流程如图,涉及的离子反应方程式书写错误的是( ) A. 2Cl-+2H2O B. Cl2+2OH-=Cl-+ClO-+H2O C. 3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O D. 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O |
|
| 9. 选择题 | 详细信息 |
|
因反应物的用量、浓度或反应条件不同,下列各项中反应产物不同的是( ) A. Al2O3与NaOH B. Fe与Cl2 C. Cu与HNO3 D. NaHCO3与稀盐酸 |
|
| 10. 选择题 | 详细信息 |
|
明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。 下列叙述错误的是  A. 合理处理易拉罐有利于环境保护和资源再利用 B. 从易拉罐中可回收的金属元素有Al、Fe C. “沉淀”反应的金属离子为Fe3+ D. 上述流程中可用NaHSO4代替NaHCO3 |
|
| 11. 选择题 | 详细信息 |
用无机矿物资源生产部分材料,其产品流程示意图如下,下列说法正确的是( )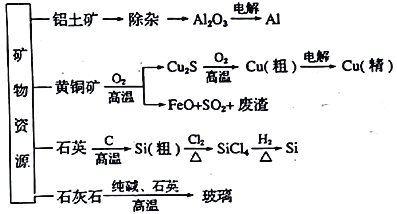 A. 制取粗硅时生成的气体产物为CO2 B. 生产铝、铜、高纯硅及玻璃的过程中都涉及氧化还原反应 C. 电解精炼铜时,当电路中转移0.2mol 电子时阳极质量减轻6.4g D. 粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法 |
|
| 12. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验操作、现象、解释或结论都正确的是
|
|||||||||||||||||||||
| 13. 选择题 | 详细信息 |
下列有关图像的说法正确的是 A. 图甲表示:向某明矾溶液中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与滴加NaOH溶液体积的关系 B. 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量,生成气体的体积与滴加HCl溶液体积的关系 C. 图丙表示:在稀硝酸溶液中逐渐加入铁粉至过量,溶液中Fe3+物质的量与逐渐加入铁粉物质的量的变化关系 D. 除去混在硝酸钾中少量的氯化钠可用“蒸发浓缩、趁热过滤”的方法 |
|
| 14. 选择题 | 详细信息 |
为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是 A.原溶液中一定含有 C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子 |
|
| 15. 选择题 | 详细信息 |
|
下列说法正确的是 A. 将NaOH溶液分多次缓慢注入盐酸中,还是一次性快速注入盐酸中,都不影响中和热测定 B. 已知反应的中和热为ΔH=-57.3 kJ·mol-1,则稀H2SO4和稀Ca(OH)2溶液反应的中和热ΔH=-2×57.3 kJ·mol-1 C. 燃烧热是指在101 kPa时可燃物完全燃烧时所放出的热量,故S(s)+3/2O2(g)═SO3(g)ΔH=-315 kJ·mol-1即为硫的燃烧热 D. 已知冰的熔化热为6.0 kJ·mol-1,冰中氢键键能为20.0 kJ·mol-1,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰中的氢键,则最多只能破坏1 mol冰中15%氢键 |
|
| 16. 选择题 | 详细信息 |
|
下列说法中不正确的是( ) A.SiO2(s)+2C(s)= Si(s)+2CO(g)只能在高温下自发进行,则该反应的ΔH>0 B.3C(s)+CaO(s)= CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0 C.BaSO4(s)+4C(s)= BaS(s)+4CO(g)在室温下不能自发进行,说明该反应的ΔH<0 D.常温下,2NO(g)+O2(g)===2NO2(g)能够自发进行,则该反应的ΔH<0 |
|
| 17. 选择题 | 详细信息 |
|
在一密闭容器中,等物质的量的A和B发生反应:A(g)+2B(g) A.40% B.50% C.60% D.70% |
|
| 18. 选择题 | 详细信息 |
探究Na2O2与水的反应,实验如图:(已知:H2O2 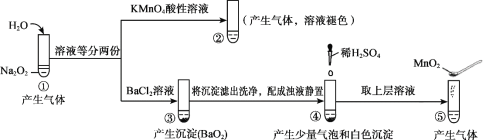 A.①、⑤中产生的气体能使带火星的木条复燃 B.①、④中均发生了氧化还原反应和复分解反应 C.②、⑤中KMnO4与MnO2的作用不同 D.通过③能比较酸性:HCl>H2O2 |
|
| 19. 选择题 | 详细信息 |
一种新型锰氢二次电池原理如图所示。该电池以MnSO4溶液为电解液,碳纤维与Pt/C分别为电极材料,电池的总反应为Mn2++ 2H2O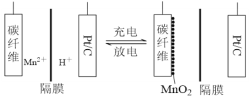 A. 充电时,碳纤维电极做阳极 B. 充电时,碳纤维电极附近溶液的pH增大 C. 放电时,电子由Pt/C电极经导线流向碳纤维电极 D. 放电时,正极反应式为MnO2 + 4H++ 2e-=Mn2++ 2H2O |
|
| 20. 选择题 | 详细信息 |
手持技术的氧电化学传感器可用于测定O2含量,如图为某种氧电化学传感器的原理示意图。已知在测定O2含量过程中,电解质溶液的质量保持不变。一定时间内,若通过传感器的待测气体为a L(标准状况),某电极增重了b g。下列说法正确的是( )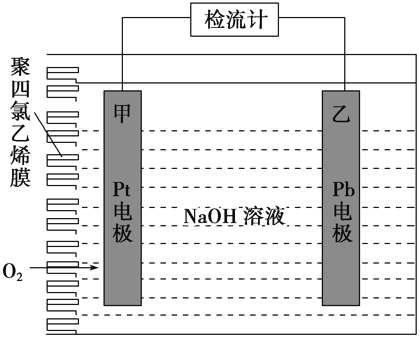 A.Pt上发生氧化反应 B.Pb上发生的电极反应式为Pb+2OH-+2e-=Pb(OH)2 C.反应过程中转移OH-的物质的量为0.25b mol D.待测气体中氧气的体积分数为 |
|
| 21. 选择题 | 详细信息 |
|
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g) A.其它条件不变,加入催化剂,△H变大 B.充入氦气使体系压强增大,可提高反应物的转化率 C.及时除去二氧化碳,有利于NO的转化 D.若升高温度,该反应的平衡常数增大 |
|
| 22. 选择题 | 详细信息 | ||||||||
E和F加入密闭容器中,在一定条件下发生反应:E(s)+4F(g)
|
|||||||||
| 23. 选择题 | 详细信息 |
|
某温度下,在一个2L的密闭容器中,加入4molA和 2molB进行如下反应:3A(g)+2B(g) A.该反应的化学平衡常数表达式是 K= B.此时,B的平衡转化率是40% C.增大该体系的压强,平衡向右移动,化学平衡常数增大 D.增加 B,平衡向右移动,B的平衡转化率增大 |
|
| 24. 选择题 | 详细信息 |
|
对于平衡体系mA(g)+nB(g)⇌pC(g)+qD(g) △H=b kJ·mol-1,下列结论中错误的是 A. 若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q B. 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n C. 保持其它条件不变,升高温度,D的体积分数增大说明该反应的△H<0。 D. 若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
|
| 25. 选择题 | 详细信息 | ||||||||||
将1 mol N2和 3 mol H2充入体积可变的恒温密闭容器中,在380 ℃下发生反应:N2(g)+3H2(g)
|
|||||||||||
| 26. 综合题 | 详细信息 |
|
金属镓是广泛用于电子工业和通讯领域的重要金属,化学性质与铝元素相似。 (1)工业上提纯镓的方法很多,其中以电解精炼法为多。具体原理如下:以待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH水溶液为电解质溶液。在电流作用下使粗镓在阳极溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。 ①已知离子氧化性顺序为Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是_______。 ②GaO2-在阴极放电的电极方程式是__________________________。 (2)工业上利用固态Ga与NH3高温条件下合成固体半导体材料氮化镓(GaN)同时又有氢气生成。反应中每生成3 mol H2时就会放出30.8 kJ热量。 ①该反应的热化学方程式为__________________________。 ②一定条件下,加入一定量的Ga与NH3进行上述反应,下列叙述符合事实且可作为判断反应已达到平衡状态的标志的是_______________。 A.恒温恒压下,混合气体的密度不变 B.断裂3 mol H—H键,同时断裂2 mol N—H键 C.恒温恒压下达平衡后再加入2 mol H2使平衡移动,NH3消耗速率等于原平衡时NH3的消耗速率 D.升高温度,氢气的生成速率先增大再减小 |
|
| 27. 实验题 | 详细信息 | ||||||||||||||||||||
FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
|
|||||||||||||||||||||
| 28. | 详细信息 |
工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如下图所示: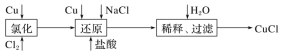 试依据如图转化回答下列问题: (1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是_______。 (2)还原过程中的产物为Na[CuCl2],试写出该反应的化学方程式:___________。 (3)合成结束后所得产品用酒精淋洗的目的是_______________。 (4)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:____。 |
|
| 29. 综合题 | 详细信息 |
如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为2K2S2+KI3=K2S4+3KI,图中的离子交换膜只允许K+通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 1.28 g。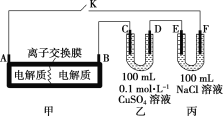 (1)装置甲的A电极为电池的__极,电解质的K+向__(填“左侧”或“右侧”)迁移;B电极的电极反应式为____。 (2)装置乙中D电极析出的气体是___,体积为____mL(标准状况)。 (3)若将装置丙中的NaCl溶液改换成FeCl2和FeCl3的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。 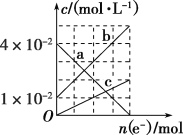 ①图中b表示的是_____(填金属离子符号)的变化曲线。 ②反应结束后,若用0.5 mol·L-1NaOH溶液沉淀丙装置溶液中的金属阳离子(设溶液体积为100 mL),则至少需要0.5 mol·L-1NaOH溶液______mL。 |
|
| 30. 综合题 | 详细信息 |
|
控制、治理氮氧化物对大气的污染是改善大气质量的重要方法。回答下列与雾霾治理有关的问题: Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。已知:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1;②4NO2(g)+2N2(g)= 8NO(g) ΔH=+586 kJ·mol-1。则CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ΔH=________ kJ·mol-1。 (2)工业烟气中的氮氧化物可用NH3催化还原,反应原理如图所示。  其中X为一种无毒的气体,则NH3催化还原氮氧化物的化学方程式为______。 (3)用NH3催化还原烟气中的氮氧化物时,当 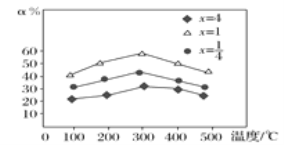 Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如CO(g)+2H2(g) 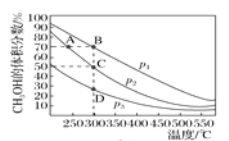 ①图中压强p1、p2、p3的大小关系是_______。 ②C点平衡常数K=___,A、B、D三点的平衡常数K(分别用KA、KB、KD表示)的大小关系是_____。 |
|
| 31. | 详细信息 |
磷酸二氢钾(KH2PO4)在工业、农业、医药及食品等行业均有广泛的应用。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如图所示(部分流程步骤已省略):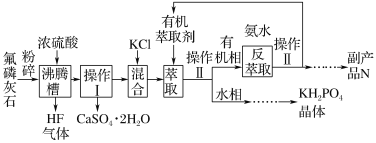 其中,萃取是因为KCl和H3PO4产生的HCl易溶于有机萃取剂。请回答下列问题: (1)氟磷灰石(Ca5P3FO12)中磷元素的化合价是____。 (2)用化学反应原理解释KCl和H3PO4生成KH2PO4的原因: ________。 (3)沸腾槽不能采用陶瓷材质的原因是_______(用化学方程式表示)。 (4)在得到N的流程中“……”的操作步骤是______、洗涤、干燥。 (5)在萃取过程中,影响萃取率的因素复杂,下图是投料比 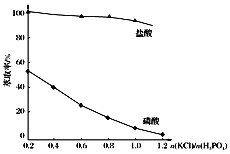 A.0.2~0.4 B.0.4~0.6 C.0.6~0.8 D.0.8~1.0 E.1.0~1.2 (6)电解法制备KH2PO4是用石墨作电极,将电解槽分为a区和b区,中间用阳离子交换膜隔离,a区为3 mol·L-1 H3PO4,b区为3 mol·L-1 KCl。阳极区为____(填“a”或“b”)区,其电极反应式是________。 |
|





