河南九年级化学2019年下册中考模拟在线免费考试
| 1. | 详细信息 |
|
下列变化中,前者是化学变化,后者是物理变化的是( ) A. 轮胎爆炸、石蜡熔化 B. 食物腐败、酒精挥发 C. 工业制氧、光合作用 D. 粮食酿酒、瓦斯爆炸 |
|
| 2. | 详细信息 |
|
化学源于生活,生活离不开化学。下列说法错误的是( ) A. 人体中铁元素的摄入量不足易引发缺铁性贫血 B. 维生素D有助于人体骨骼和牙齿的生长发育 C. 使用福尔马林浸泡的海鲜对人体健康有害 D. 元素周期表中的元素都是人体所必需的 |
|
| 3. | 详细信息 |
|
如图所示的实验操作正确的是( ) A. 加热固体  B. 过滤 B. 过滤 C. 稀释浓硫酸  D. 蒸发食盐水 D. 蒸发食盐水 |
|
| 4. | 详细信息 |
|
推理是一种重要的化学学习方法。下列推理正确的是( ) A. 单质中只含一种元素,所以只含一种元素的物质一定是单质 B. 氧气是由氧元素组成的,所以制取氧气的反应物中一定含有氧元素 C. 离子是带电的微粒,所以带电的微粒一定是离子 D. NaCl、Na2SO4、KNO3的水溶液呈中性,所以盐的水溶液都呈中性 |
|
| 5. | 详细信息 | ||||||||
善于归纳知识,有利于提高学习能力。下列知识整理的内容不完全正确的一组是( )
|
|||||||||
| 6. | 详细信息 |
|
下列物质是由分子构成的是 A. 金刚石 碳酸钙 B. 氯化钠 乙醇 C. 干冰 甲烷 D. 铁 水 |
|
| 7. | 详细信息 |
|
近两年广泛流传一个民生热词“舌尖上的安全”。下列做法合理的是( ) A. 大量使用食品添加剂 B. 用硫酸铜溶液浸泡粽叶 C. 为防止骨质疏松,长期摄入过量钙元素 D. 用碳酸氢钠作发酵粉 |
|
| 8. | 详细信息 |
|
白色粉末硫酸铜属于:①混合物 ②纯净物 ③化合物 ④氧化物 ⑤单质 A. ①③ B. ②③ C. ②③④ D. ①②③④⑤ |
|
| 9. | 详细信息 |
|
实验室配制50g溶质质量分数为15%的氯化钠溶液,下列说法中错误的是 A. 实验的步骤为计算、称取、量取、溶解、转移 B. 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速度 C. 氯化钠称量完毕放回砝码时,发现5g的砝码有缺损,则所配溶液的质量分数大于15% D. 量取水时,用规格为50ml的量筒量取42.5ml蒸馏水 |
|
| 10. | 详细信息 | ||||||||
如表所示对部分化学知识的归纳完全正确的一组是( )
|
|||||||||
| 11. | 详细信息 |
某反应前后分子变化的微观示意图如图,说法正确的是( )(“ A. 反应物都是单质 B. 反应前后分子个数减少 C. 生成物的物质的量之比为 3:2 D. 反应前后各元素都是由游离态变成化合态 |
|
| 12. | 详细信息 |
|
下列各组离子在水中一定能大量共存,并形成无色溶液的是 A. Cu2+、H+、SO42-、CI- B. Ba2+、Na+、Cl-、NO3- C. K+、Ca2+、OH-、CO32- D. Na+、H+、HCO3-、NO3- |
|
| 13. | 详细信息 |
|
下列物质的转变,不能一步实现的是( ) A. KCl→KNO3 B. Fe(NO3)2→FeCl2 C. SO2→Na2SO3 D. H2→Cu |
|
| 14. | 详细信息 |
|
某混合物由Mg和MgO组成,取该混合物12.8g与一定量稀硫酸恰好完全反应,所得溶液中溶质的质量为52g,则原混合物中氧元素的质量为( ) A. 4.8g B. 4.0g C. 3.2g D. 2.4g |
|
| 15. | 详细信息 |
|
请从水、氧气、氦气、硫酸铜中选择适当的物质的化学式填空: 能支持燃烧的是_____;能填充探空气球的是_____;由离子构成的物质是_____. |
|
| 16. | 详细信息 |
某元素的离子结构示意图如图所示,该元素的离子符号为Br﹣。 (1)图中x=_____,Br属于_____元素(填“金属”或“非金属”), (2)如图表示的微粒中,具有相似化学性质的几种微粒是_____。(填序号)以下微粒中与溴元素化学性质相似的是_____。(填序号)  |
|
| 17. | 详细信息 |
如图是 a、b、c 三种固体物质的溶解度曲线,下列说法正确的是_____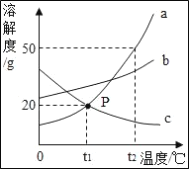 A t1℃时 a、c 的溶解度相等 B 使 t1℃时 a、b 的饱和溶液升温至 t2℃仍为饱和溶 液,需加入的 a 比 b 多 C t1℃时 a、c 的溶液中溶质质量分数一定相等 D t2℃时,将 a、b、c 的饱和溶液的温度降低至 t1℃,所得溶液中溶质质量分数大小关系为_____ |
|
| 18. | 详细信息 |
|
实验室化学试剂常需要密封保存. (1)长期敞口放置浓硫酸,因_____而导致浓度减小,因此浓硫酸常作为_____等气体的干燥剂. (2)氢氧化钠固体不仅能吸收空气中的水蒸气而_____,还能和空气中的二氧化碳反应,其反应的化学方程式为_____. (3)碳酸氢铵是一种白色固体,有吸湿性,因此需要密封保存.36℃时能分解为二氧化碳、氨气(NH3)和水.试写出碳酸氢铵分解的化学方程式_____. |
|
| 19. | 详细信息 |
A〜F是初中化学常见的物质,己知A、B、C、D、E是五种不同类别的物质。a足空气中含有的一种气体,e是地壳中含量最多的金属元素组成的单质,F中各元素质量比为2:1:2,六种物质之间的反应与转化关系均为初中化学常见的化学反应,图中“→”表示相连的物质能相互反应,“一”表示一种 物质转化成另一种物质(部分反应物、生成物及反应 条件己略去)请回答下列问题。 (1)分别写出A、B、E、F物质的化学式: A_____; B_____; E_____; F_____。 (2)E和F反应的化学方程式_____, (3)E和D发生反应的实验现象是_____。 |
|
| 20. | 详细信息 |
| 用氯化钠固体和水配制6%的氯化钠溶液50g,需氯化钠_____g,若量取水时仰视读数,其它操作均正确,则配制的氯化钠溶液中溶质质量分数_____6%(填“>”“<”或“=“)。 | |
| 21. | 详细信息 |
|
写出下列反应的化学方程式: |
|
| 22. | 详细信息 |
根据如图回答下列问题: (1)写出实验中所发生反应的化学方程式。 (2)写出本实验中水的作用。(一条即可) (3)根据“铜片上的白磷燃烧面水中的白磷没有燃烧”这一现象可得出的结论。 |
|
| 23. | 详细信息 |
|
粗盐中含有的杂质有CaCl2、MgC12、Na2SO4和泥沙,为除去杂质得到精盐,加水溶解后可按以下顺序操作:①加过量的NaOH溶液;②加过量的BaCl2溶液;③加过量的Na2CO3溶液;④过滤;⑤加足量的盐酸;⑥蒸发结晶。 (1)写出除去Na2SO4的化学方程式_____。 (2)以上操作一共发生_____个反应。 |
|
| 24. | 详细信息 | |||||||||
现有下列仪器或装置,请回答下列问题: ①仪器a的名称是______:用______ ②选择气体收集方法时,必须考虑的气体性质有______ A 颜色 B 密度 C 溶解性 D 可燃性 ③向“人”字型管G装置
|
||||||||||
| 25. | 详细信息 |
|
酸、碱、盐是中学化学学习和研究的重要化合物。 (1)下列关于硫酸的说法不正确的是_____。 A 稀硫酸能够与锌反应制取氢气 B 硫酸溶液中K+、Ca2+、OH﹣、Cl﹣可以大量共存 C 浓硫酸和浓盐酸敞口放置后溶质质量分数均减小 D硫酸和盐酸溶液中都含有H+,因此它们的化学性质相似 (2)久置的氢氧化钠溶液中通常会变质,写出其化学方程式_____。 (3)已知①中盛有一定量的碳酸钠溶液,根据图示的实验过程回答下列问题。  ①烧杯中加入酚酞溶液的现象是_____。 ②写出烧杯②中加入石灰水后发生反应的化学方程式_____。 ③烧杯③中加入过量的稀盐酸后得到溶液中的溶质一定有哪些?_____ (4)某化学兴趣小组用一定量的碳酸钠溶液和石灰水反应制取氢氧化钠,并对反应后的溶质成分进行探究。某同学认为反应后的溶液一定含有碳酸钠,请你设计实验进行检验。_____ (5)取99g碳酸钠溶液放入烧杯中,加入111g氯化钙溶液恰好完全反应,过滤,得滤渣10g求反应后所得溶液中溶质的质量分数是多少?_____ |
|
最近更新




