北京2017年九年级上学期化学免费试卷完整版
| 1. 选择题 | 详细信息 |
下列属于化学变化的是( )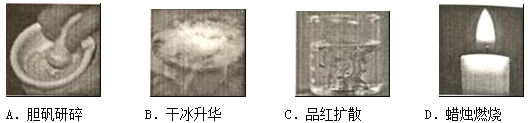 |
|
| 2. 选择题 | 详细信息 |
|
空气成分中,氮气的体积分数约为() A.78% B.21% C.0.03% D.0.94% |
|
| 3. 选择题 | 详细信息 |
|
下列属于氧化物的是 A. O2 B. SiO2 C. KCl D. NaOH |
|
| 4. 选择题 | 详细信息 |
|
下列物质放入水中,能形成溶液的是 A. 面粉 B. 牛奶 C. 白糖 D. 植物油 |
|
| 5. 选择题 | 详细信息 |
|
地壳中含量最多的元素是( ) A. 硅 B. 氧 C. 铁 D. 铝 |
|
| 6. 选择题 | 详细信息 |
|
碳酸氢钠可用于焙制糕点,其俗称是() A.纯碱 B.熟石灰 C.苛性钠 D.小苏打 |
|
| 7. 选择题 | 详细信息 |
|
下列物质中,含有氧分子的是( ) A. 水 B. 液氧 C. 氧化汞 D. 二氧化碳 |
|
| 8. 选择题 | 详细信息 |
|
下列化学符号中,表示2个氢分子的是( ) A H2B 2H C 2H2D 2H+ |
|
| 9. 选择题 | 详细信息 |
|
下列厨房用品所使用的主要材料中,不属于有机合成材料的是( ) A.  铝合金微波炉架 B. 铝合金微波炉架 B. 橡胶食品模具 C. 橡胶食品模具 C. 塑料调料盒 D. 塑料调料盒 D. 涤纶围裙 涤纶围裙 |
|
| 10. 选择题 | 详细信息 |
|
空气中各种成分作为原料广泛用于生产化肥、炼钢、电光源等领域。其中生产氮肥的原料是() A.N2 B.O2 C.Ne D.CO2 |
|
| 11. 选择题 | 详细信息 |
|
下列做法中,不利于保护水资源的是() A.使用节水型马桶 B.使用含磷洗衣粉 C.合理使用农药和化肥 D.工业废水处理达标后排放 |
|
| 12. 选择题 | 详细信息 | ||||||||||
下表为人体内几种体液或代谢产物的正常pH范围,其中碱性最强的是
|
|||||||||||
| 13. 选择题 | 详细信息 |
|
下列物质露置于空气中,一段时间后,质量增大但不会变质的是() A.氢氧化钠固体 B.浓硫酸 C.浓盐酸 D.石灰水 |
|
| 14. 选择题 | 详细信息 |
|
下列实验操作中,不正确的是() A.  蒸发食盐水 蒸发食盐水B. 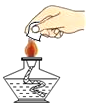 熄灭酒精灯 熄灭酒精灯C.  读取液体体积 读取液体体积D.  稀释浓硫酸 稀释浓硫酸 |
|
| 15. 选择题 | 详细信息 |
|
下列各种物质的用途中,利用其物理性质的是( ) A. 氢气作燃料 B. 氢氧化钠作干燥剂 C. 氧气用于气焊 D. 铁粉用作食品保鲜吸氧剂 |
|
| 16. 选择题 | 详细信息 |
|
中国科学技术馆“物质之妙”展区有一台分子运动模拟器。这台模拟器是由玻璃罩内小球的变化情况来表现固、液、气三态中分子的状态。当向前推动滑竿,模拟温度升高时,玻璃罩中的小球将 A. 间隔变小 B. 质量变大 C. 运动加快 D. 数量增多 |
|
| 17. 选择题 | 详细信息 | ||||||||||||||||||||
下表列出了除去物质中所含少量杂质的方法,其中错误的是
|
|||||||||||||||||||||
| 18. 选择题 | 详细信息 |
《天工开物》是中国古代一部综合性的科学技术著作。在其中一篇《青矾、红矾、黄矾、胆矾》中记载“石矾一名胆矾者……乃山石穴中自结成者,故绿色带宝光。烧铁器淬于胆矾水中,即成铜色也。”以下理解正确的是() A.胆矾是白色固体 B.胆矾中含有铁元素 C.铁可与胆矾水发生化学反应 D.石矾是青矾、红矾、黄矾和胆矾的统称 |
|
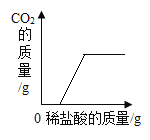
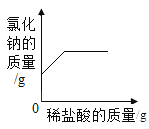
| 19. 选择题 | 详细信息 | ||||||||||||
下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是()
|
|||||||||||||
| 20. 填空题 | 详细信息 |
|
民以食为天,食以安为先。 (1)某校为学生制定的营养午餐食谱为:主食—米饭;副食—花生米、炖牛肉、清蒸鱼;饮品—牛奶。牛肉中主要富含的营养素是_____________。 请从营养均衡角度考虑,为学校再推荐的一道菜是_________________。 (2)食品安全备受关注。下列做法会严重危害人体健康的是_______(填字母序号)。 A 用甲醛溶液浸泡海产品 B 食品包装中充氮气防腐 C 香肠中添加过量的亚硝酸钠延长保质期 D 霉变的大米蒸煮后食用 |
|
| 21. 填空题 | 详细信息 |
| 碳酸饮料中大部分都含有柠檬酸和磷酸,过量摄入会影响某元素的吸收,儿童缺少该元素可能导致佝偻病,该元素为______。新鲜水果榨制成的果汁中含人体所需的营养成分,主要有水、无机盐、糖等,其中能为人体提供能量的营养素是______。 | |
| 22. 填空题 | 详细信息 |
|
关注环境是一种生活态度。 (1)活性炭可用来吸收装修材料释放出来的一些有毒气体,这是利用活性炭的__________。 (2)“低能耗”、“低废水”、“低废弃物”是低碳理念的重要内涵。 下列做法符合低碳理念的是_____________(填字母序号)。 A 发展太阳能、风能等新能源 B 用淘米水浇花 C 家用电器长期处于待机状态 D 推广无纸化办公,双面打印文稿 |
|
| 23. 填空题 | 详细信息 |
|
碳元素是组成许多物质的基本元素。 (1)下列物质的主要成分中(括号所示为主要成分的化学式),能与鸡蛋壳的主要成分反应的是______(填字母序号)。 A  食醋(CH3COOH) 食醋(CH3COOH) B  食用纯碱(Na2CO3) 食用纯碱(Na2CO3) C  味精(C5H8NO4Na) 味精(C5H8NO4Na)(2)化石燃料包括煤、石油和天然气,其中天然气充分燃烧的化学方程式为___________________。 (3)二氧化碳可用于制化肥尿素[CO(NH2)2],其反应的微观示意图如下: 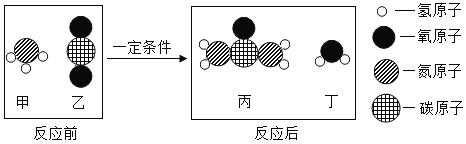 生产尿素的反应中,丙与丁的质量比为______________。 |
|
| 24. 填空题 | 详细信息 |
|
水是最普通、最常见的物质之一。 (1)“水”有很多种。下列“水”属于纯净物的是_________(填字母序号)。 A 河水 B 自来水 C 矿泉水 D 蒸馏水 (2)电解水可证明水由氢、氧两种元素组成,若电解72g水时,生成氢气的质量为______g 。 |
|
| 25. 填空题 | 详细信息 |
氯碱工业以饱和食盐水为原料获得烧碱等化工产品,反应原理为: (1)X的化学式为_____________。 (2)制得的烧碱可用于处理硫酸泄漏,反应的化学方程式为__________________________________。 |
|
| 26. 简答题 | 详细信息 |
|
金属在生产、生活中有广泛的用途。 (1)铝块能制成用于包装的铝箔,是由于铝具有______________。工业上常用电解氧化铝的方法制铝,电解中需加入助熔剂——冰晶石(Na3AlF6),其中氟元素的化合价为_________。 (2)汽车车体表面喷漆不仅美观,而且可有效防止与__________________接触而生锈。 (3)铁是世界上年产量最高的金属。用一氧化碳还原氧化铁的化学方程式为____________________。 (4)将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤。滤液中的溶质一定有___________________,证明滤渣中成分的实验方案是__________________________________。 |
|
| 27. | 详细信息 |
|
阅读下列资料,回答相关问题: 目前,世界上的钠多数采用电解熔融氯化钠的方法制得。氯化钠的熔点为801℃,在技术上有困难。将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,氯气在正极放出,金属钠和金属钙同时被还原出来,浮在负极的共熔物上,从管道溢出。把熔融的金属混合物冷却到105~110℃,金属钙成晶体析出,经过滤分离。 钠原子的结构示意图为 金属钠的应用非常广泛,大部分金属钠用于制造一种抗爆剂——四乙基铅,它能降低汽油的爆震性。钠还用于制造过氧化钠(Na2O2)等化合物。钠和钾组成的合金在常温时是液体,用于快中子增殖反应堆作热交换流体。 (1)在钠的原子结构中,与其化学性质活泼关系最密切的数字是_________________。 (2)金属钠通常保存在石蜡油中,目的是隔绝_____________________。 (3)钠能与水反应,化学方程式为__________________________________________。推测钙能不能与水反应并说明理由__________________________________________。 (4)从上文中总结钠具有的物理性质有__________________________________________(写出4条)。 |
|
| 28. 流程题 | 详细信息 |
工业尾气硫化氢(H2S)是一种有毒气体,溶于水成为氢硫酸(H2S)溶液。目前采用氢氧化钠溶液吸收可以减少对空气的污染,并且可以制得工业产品硫化钠固体(硫化钠可溶于水)。工业流程如下图所示。 (1)可用_______________测定氢硫酸溶液的酸碱度。 (2)吸收塔内发生的是复分解反应,该反应的化学方程式为________________________________________。 (3)系列操作中一定有的步骤是____________操作。 |
|
| 29. 填空题 | 详细信息 |
|
MnSO4在工业中有重要应用,可用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4。 (1)MnO2与MnSO4中锰元素的化合价________(填“相同”或“不同”)。 (2)Fe2O3 中Fe与O的元素质量比为__________。 (3)软锰矿浆中的高活性MnO2可用于催化降解甲醛(HCHO),有关微粒的变化如图所示,该反应过程中甲醛降解的最终产物是________。  |
|
| 30. 推断题 | 详细信息 |
A、B、C、D、E、F是初中化学实验室常用的6种白色固体物质,由氢、碳、氧、氯、钠和钙元素组成。实验教师按其类别放置在药品柜中,下图是以上各种药品摆放的示意图(矩形表示药品柜)。其中,4种盐有两种摆放方式。 (1)B是唯一难溶于水的物质,其化学式为__________。 (2)E的溶液可与A的溶液反应生成D的溶液,其化学方程式为_________________。 (3)证明A、B、F含有部分相同的组成,所需试剂是_____________________________。 (4)C可由其他三种物质分别转化而成,图中的反应①是中和反应,该反应的化学方程式为______________________________。请将这三种物质的代号按照反应的编号填入下图中①是_______、②是_______、③是_______。  |
|
| 31. 实验探究题 | 详细信息 |
根据下图回答问题。 (1)实验室用高锰酸钾制取氧气的化学方程式为______________________________________,选用的发生装置是________(填字母序号,下同)。 (2)实验室制取二氧化碳时,选用的收集装置是_________,选用该方法收集二氧化碳的原因是________________。向该集气瓶中加入紫色石蕊溶液,振荡后,观察到溶液变红,发生反应的化学方程式为________________,该反应可用于____________。 |
|
| 32. 实验探究题 | 详细信息 |
|
以下是初中化学的一些基本实验,根据图示回答问题。 A  测定空气中O2含量 测定空气中O2含量 B  探究蜡烛的元素组成 探究蜡烛的元素组成 C  铁丝在空气中中的变化 铁丝在空气中中的变化(1)A中集气瓶内水的作用是_____________________________________________。 (2)B中得出的实验结论是_____________________________。 (3)一段时间后,C中的实验现象为_______________,产生该现象的原因是______________________。 |
|
| 33. 简答题 | 详细信息 | ||||||||
|
19世纪末,科学家瑞利通过如下两种方法制得氮气,并测得其密度,从而导致了科学史上的某项重大发现。请你参与氮气的科学发现过程。 方法Ⅰ:利用空气分离出氮气
|
|||||||||
| 34. 简答题 | 详细信息 |
用如下图所示装置分别进行以下实验。 (1)打开止水夹,向Ⅰ中液体加入一种黑色固体、Ⅱ中液体加入白磷。Ⅰ和Ⅱ中均有气泡出现,且Ⅱ中白磷燃烧。 ①写出Ⅰ中反应的化学方程式_______________________________。 ②Ⅱ中白磷燃烧的原因是___________________________________。 (2)打开止水夹,向Ⅰ中稀硫酸加入少量碳酸钠固体。Ⅰ和Ⅱ中均有气泡出现,但Ⅱ中盛有的氢氧化钠溶液无其它明显现象。一段时间后,关闭止水夹,发现Ⅱ中液面上升,并产生气泡。 ①关闭止水夹前,Ⅱ中发生反应的化学方程式为_________________________。 ②上述实验能否证明二氧化碳与氢氧化钠发生反应,理由是_____________________________。 |
|
| 35. 科学探究题 | 详细信息 | ||||||||||||||||||||
|
化学小组同学在课外读物中看到:“加热时,过氧化钠(Na2O2)能与木炭发生化学反应”。他们决定探究Na2O2与木炭反应的产物。 (猜想与假设)木炭与Na2O2反应可能生成4种物质:CO、CO2、Na2O和Na2CO3。 (查阅资料) ① 碱性的碳酸钠溶液与中性的CaCl2溶液能发生复分解反应。 ② 氧化钠(Na2O)是白色固体,与H2O反应生成NaOH。 ③ 氯化钯(PdCl2)溶液能检验CO的存在,向溶液中通入CO,产生黑色沉淀。 (进行实验)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)。 
|
|||||||||||||||||||||