дёҠжө·еёӮ2018е№ҙй«ҳдёүеҢ–еӯҰдёҠеҶҢй«ҳиҖғжЁЎжӢҹиҜ•еҚ·е®Ңж•ҙзүҲ
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
19дё–зәӘдёӯеҸ¶пјҢй—ЁжҚ·еҲ—еӨ«зҡ„зӘҒеҮәиҙЎзҢ®жҳҜ A. жҸҗеҮәдәҶеҺҹеӯҗеӯҰиҜҙ B. жҸҗеҮәдәҶе…ғзҙ е‘ЁжңҹеҫӢ C. жҸҗеҮәдәҶеҲҶеӯҗеӯҰиҜҙ D. жҸҗеҮәдәҶеҢ–еӯҰ平衡移еҠЁеҺҹзҗҶ |
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
д»…йҖҡиҝҮзү©зҗҶж–№жі•е°ұиғҪд»Һжө·ж°ҙдёӯиҺ·еҫ—зҡ„зү©иҙЁжҳҜ AпјҺй’ гҖҒй•Ғ BпјҺжәҙгҖҒзўҳ CпјҺйЈҹзӣҗгҖҒж·Ўж°ҙ DпјҺж°Ҝж°”гҖҒзғ§зўұ |
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
еұһдәҺејұз”өи§ЈиҙЁзҡ„жҳҜ( ) A. дёҖж°ҙеҗҲж°Ё B. йҶӢй…ёй“ө C. д№ҷйҶҮ D. зЎ«й…ёй’Ў |
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
еұһдәҺе·Ҙдёҡеӣәж°®зҡ„жҳҜ A. з”ЁN2е’ҢH2еҗҲжҲҗж°Ё B. й—Әз”өе°Ҷз©әж°”дёӯN2иҪ¬еҢ–дёәNO C. з”ЁNH3е’ҢCO2еҗҲжҲҗе°ҝзҙ D. еӣәж°®иҸҢе°Ҷж°®ж°”еҸҳжҲҗж°Ё |
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҺҹеӯҗжңҖеӨ–еұӮз”өеӯҗжҺ’еёғдёә2s22p3пјҢеҲҷиҜҘеҺҹеӯҗ A. ж ёеӨ–жңү5дёӘз”өеӯҗ B. ж ёеӨ–жңү3з§ҚиғҪйҮҸдёҚеҗҢзҡ„з”өеӯҗ C. жңҖеӨ–еұӮз”өеӯҗеҚ жҚ®3дёӘиҪЁйҒ“ D. жңҖеӨ–еұӮдёҠжңү3з§ҚиҝҗеҠЁзҠ¶жҖҒдёҚеҗҢзҡ„з”өеӯҗ |
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҖе®ҡжқЎд»¶дёӢдёҚиғҪдёҺиӢҜеҸ‘з”ҹеҸҚеә”зҡ„жҳҜ( ) A. й…ёжҖ§KMnO4 B. Br2 C. жө“HNO3 D. H2 |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
еҚ•иҙЁй“ҒдёҚеҗҢдәҺй“қзҡ„жҖ§иҙЁжҳҜ A. йҒҮеҶ·зҡ„жө“зЎ«й…ёй’қеҢ– B. иғҪдёҺж°ўж°§еҢ–й’ еҸҚеә” C. иғҪдёҺзӣҗй…ёеҸҚеә” D. иғҪеңЁж°§ж°”дёӯзҮғзғ§ |
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
еҸӘз”ЁдёҖз§ҚиҜ•еүӮеҚіеҸҜеҢәеҲ«зҡ„пјҡNaClгҖҒMgCl2гҖҒFeCl3гҖҒAl2(SO4)3еӣӣз§Қжә¶ж¶ІпјҢиҝҷз§ҚиҜ•еүӮжҳҜ A. AgNO3 B. NaOH C. BaCl2 D. HCl |
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
зҶ”еҢ–ж—¶йңҖз ҙеқҸе…ұд»·й”®зҡ„жҷ¶дҪ“жҳҜ A. NaOH B. CO2 C. SiO2 D. NaCl |
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
SO2еӮ¬еҢ–ж°§еҢ–иҝҮзЁӢдёӯпјҢдёҚз¬ҰеҗҲе·Ҙдёҡз”ҹдә§е®һйҷ…зҡ„жҳҜ A. йҮҮз”ЁзғӯдәӨжҚўеҷЁеҫӘзҺҜеҲ©з”ЁиғҪйҮҸ B. еҺӢејәжҺ§еҲ¶дёә20пҪһ50MPa C. еҸҚеә”жё©еәҰжҺ§еҲ¶еңЁ450в„ғе·ҰеҸі D. дҪҝз”ЁV2O5дҪңеӮ¬еҢ–еүӮ |
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
иғҪдҪҝе“Ғзәўжә¶ж¶ІиӨӘиүІзҡ„зү©иҙЁжҳҜ в‘ жјӮзІүзІҫ в‘ЎиҝҮж°§еҢ–й’ в‘ўж–°еҲ¶ж°Ҝж°ҙ в‘ЈдәҢж°§еҢ–зЎ« A. в‘ в‘ўв‘Ј B. в‘Ўв‘ўв‘Ј C. в‘ в‘Ўв‘ў D. в‘ в‘Ўв‘ўв‘Ј |
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
ж— иүІйҖҸжҳҺзҡ„жҹҗејәй…ёжҖ§жә¶ж¶ІдёӯиғҪеӨ§йҮҸе…ұеӯҳзҡ„зҰ»еӯҗз»„жҳҜ A. Na+гҖҒK+гҖҒOH-гҖҒCl- B. Na+гҖҒCu2+гҖҒSO42-гҖҒNO3- C. Ca2+гҖҒHCO3-гҖҒNO3-гҖҒK+ D. Mg2+гҖҒNa+гҖҒSO42-гҖҒCl- |
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺй’ўй“Ғз”өеҢ–еӯҰдҝқжҠӨдёӨз§Қж–№жі•зҡ„иҜҙжі•й”ҷиҜҜзҡ„жҳҜ A. зүәзүІйҳіжһҒйҳҙжһҒдҝқжҠӨжі•еҲ©з”Ёзҡ„жҳҜеҺҹз”өжұ еҺҹзҗҶ B. еӨ–еҠ з”өжөҒйҳҙжһҒдҝқжҠӨжі•еҲ©з”Ёзҡ„жҳҜз”өи§ЈеҺҹзҗҶ C. зүәзүІйҳіжһҒйҳҙжһҒдҝқжҠӨжі•дёӯй’ўй“ҒдёәиҙҹжһҒ D. еӨ–еҠ з”өжөҒйҳҙжһҒдҝқжҠӨжі•дёӯй’ўй“ҒдёәйҳҙжһҒ |
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
еӮ¬еҢ–еҠ ж°ўдёҚиғҪеҫ—еҲ°2-з”ІеҹәжҲҠзғ·зҡ„жҳҜ( ) A. CH3CH=C(CH3)CH2CH3 B. (CH3)2C=CHCH2CH3 C. CHвүЎC(CH3)(CH2)2CH3 D. CH3CH=CHCH(CH3)2 |
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗж–№зЁӢејҸд№ҰеҶҷй”ҷиҜҜзҡ„жҳҜпјҡ( ) A. й“қзІүжҠ•е…ҘеҲ°NaOHжә¶ж¶Ідёӯпјҡ2Al+2H2O+2OH-=2AlO2-+3H2вҶ‘ B. Al(OH)3жә¶дәҺNaOHжә¶ж¶ІдёӯпјҡAl(OH)3+OH-=AlO2-+2H2O  C. FeCl2жә¶ж¶Іи·ҹCl2еҸҚеә”пјҡ2Fe2++Cl2=2Fe3++2Cl- C. FeCl2жә¶ж¶Іи·ҹCl2еҸҚеә”пјҡ2Fe2++Cl2=2Fe3++2Cl- D. AlCl3жә¶ж¶ІдёӯеҠ е…Ҙи¶ійҮҸзҡ„ж°Ёж°ҙпјҡAl3++ 3OH- = Al(OH)3вҶ“ |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁNaOHж ҮеҮҶжә¶ж¶Іж»ҙе®ҡзӣҗй…ёпјҢд»ҘдёӢж“ҚдҪңеҜјиҮҙжөӢе®ҡз»“жһңеҒҸй«ҳзҡ„жҳҜ A. ж»ҙе®ҡз®Ўз”Ёеҫ…иЈ…ж¶Іж¶Ұжҙ— B. й”ҘеҪўз“¶з”Ёеҫ…жөӢж¶Іж¶Ұжҙ— C. ж»ҙе®ҡз»“жқҹж»ҙе®ҡз®Ўжң«з«Ҝжңүж°”жіЎ D. ж»ҙе®ҡж—¶й”ҘеҪўз“¶дёӯжңүж¶ІдҪ“жә…еҮә |
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
ClO2жҳҜдёҖз§Қж¶ҲжҜ’жқҖиҸҢж•ҲзҺҮй«ҳгҖҒдәҢж¬ЎжұЎжҹ“е°Ҹзҡ„ж°ҙеӨ„зҗҶеүӮпјҢеҸҜйҖҡиҝҮд»ҘдёӢеҸҚеә”еҲ¶еҫ—ClO2: 2KClO3+ H2C2O4+ H2SO4=2ClO2+ K2SO4+ 2CO2+2H2O дёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ A. KClO3еңЁеҸҚеә”дёӯеҫ—еҲ°з”өеӯҗ B. ClO2жҳҜиҝҳеҺҹдә§зү© C. H2C2O4еңЁеҸҚеә”дёӯиў«ж°§еҢ– D. 1mol KClO3еҸӮеҠ еҸҚеә”жңү2mol з”өеӯҗиҪ¬з§» |
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺзӣҗй…ёдёҺйҶӢй…ёдёӨз§ҚзЁҖжә¶ж¶Ізҡ„иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ A. зӣёеҗҢзү©иҙЁзҡ„йҮҸжө“еәҰзҡ„дёӨжёёж¶Ідёӯc(H+)зӣёеҗҢ B. зӣёеҗҢзү©иҙЁзҡ„йҮҸзҡ„дёӨжә¶ж¶Ідёӯе’Ңж°ўж°§еҢ–й’ зҡ„зү©иҙЁзҡ„йҮҸзӣёеҗҢ C. pH=3 зҡ„дёӨжә¶ж¶ІзЁҖйҮҠ100еҖҚпјҢpHеқҮеҸҳдёә5 D. дёӨжә¶ж¶ІдёӯеҲҶеҲ«еҠ е…Ҙе°‘йҮҸеҜ№еә”зҡ„й’ зӣҗеӣәдҪ“пјҢc(H+)еқҮеҮҸе°Ҹ |
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
дёәжЁЎжӢҹж°Ёзўұжі•еҲ¶еҸ–зәҜзўұзҡ„дё»иҰҒеҸҚеә”пјҢи®ҫи®ЎеңЁеӣҫжүҖзӨәиЈ…зҪ®гҖӮжңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ( )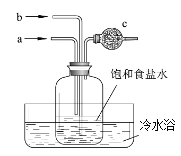 A. е…Ҳд»Һbз®ЎйҖҡе…ҘNH3еҶҚд»Һaз®ЎйҖҡе…ҘCO2 B. е…Ҳд»Һaз®ЎйҖҡе…ҘCO2еҶҚд»Һbз®ЎйҖҡе…ҘNH3 C. еҸҚеә”дёҖж®өж—¶й—ҙе№ҝеҸЈз“¶еҶ…жңүжҷ¶дҪ“жһҗеҮә D. cдёӯиЈ…жңүзўұзҹізҒ°д»Ҙеҗёж”¶жңӘеҸҚеә”зҡ„ж°Ёж°” |
|
| 20. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
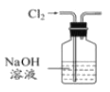
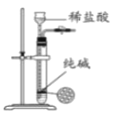
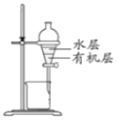
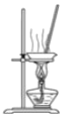
дёӢеҲ—жңүе…іе®һйӘҢиЈ…зҪ®иҝӣиЎҢзҡ„зӣёеә”е®һйӘҢпјҢиғҪиҫҫеҲ°е®һйӘҢзӣ®зҡ„зҡ„жҳҜ
|
|||||||||||||
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
AгҖҒBгҖҒCгҖҒDгҖҒEгҖҒF еқҮдёәзҹӯе‘Ёжңҹдё»ж—Ҹе…ғзҙ пјҢдё”еҺҹеӯҗеәҸж•°дҫқж¬ЎйҖ’еўһгҖӮAзҡ„еҺҹеӯҗж ёеҶ…ж— дёӯеӯҗпјҢBзҡ„еҺҹеӯҗжңҖеӨ–еұӮз”өеӯҗж•°жҳҜж¬ЎеӨ–еұӮз”өдәҺж•°зҡ„2еҖҚпјҢC жҳҜең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„е…ғзҙ пјҢDжҳҜзҹӯе‘ЁжңҹдёӯйҮ‘еұһжҖ§жңҖејәзҡ„е…ғзҙ пјҢEдёҺFдҪҚзҪ®зӣёйӮ»пјҢFжҳҜеҗҢе‘Ёжңҹе…ғзҙ дёӯеҺҹеӯҗеҚҠеҫ„жңҖе°Ҹзҡ„е…ғзҙ гҖӮ е®ҢжҲҗдёӢеҲ—еЎ«з©әйўҳ: пјҲ1пјүBеңЁе…ғзҙ жңҹиЎЁдёӯзҡ„дҪҚзҪ®дёә_______пјҢ1дёӘCеҺҹ еӯҗж ёеӨ–жңү____дёӘжңӘжҲҗеҜ№зҡ„з”өеӯҗгҖӮ пјҲ2пјүDгҖҒEгҖҒFдёүз§Қе…ғзҙ еҪўжҲҗз®ҖеҚ•зҰ»еӯҗе…¶еҚҠеҫ„з”ұlеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜ_____________гҖӮ(з”ЁзҰ»еӯҗз¬ҰеҸ·иЎЁзӨә)гҖӮ пјҲ3пјүеҶҷеҮәD дёҺC еҪўжҲҗеҢ–еҗҲзү©зҡ„з”өеӯҗејҸ______гҖҒ_______гҖӮ пјҲ4пјүеёёжё©дёӢпјҢ1molAзҡ„еҚ•иҙЁеңЁC зҡ„еҚ•иҙЁдёӯе®Ңе…ЁзҮғзғ§з”ҹжҲҗж¶ІжҖҒеҢ–еҗҲзү©пјҢ并ж”ҫеҮә286kJзҡ„зғӯйҮҸпјҢиҜҘеҸҚеә”зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸдёә______________гҖӮ пјҲ5пјүйқһйҮ‘еұһжҖ§зҡ„ејәејұ: E_____F (еЎ«вҖңејәдәҺвҖқгҖҒвҖңејұдәҺвҖқгҖҒвҖңж— жі•жҜ”иҫғвҖқ)пјҢиҜ•д»ҺеҺҹеӯҗз»“жһ„зҡ„и§’еәҰи§ЈйҮҠе…¶еҺҹеӣ ________________гҖӮ пјҲ6пјүNa2SO3еҸҜз”ЁдҪңжјӮзҷҪз»Үзү©ж—¶зҡ„еҺ»йј еүӮгҖӮNa2SO3жә¶ж¶ІеҸҠ收Cl2еҗҺпјҢжә¶ж¶Ізҡ„й…ёжҖ§еўһејәгҖӮеҶҷеҮәиҜҘеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸ______гҖӮ |
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
еҸҚеә”A(g)+ B(g)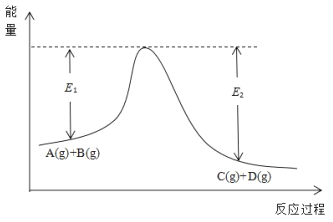 е®ҢжҲҗдёӢеҲ—еЎ«з©ә: пјҲ1пјүиҜҘеҸҚеә”жҳҜ__________еҸҚеә”(йҖүеЎ«вҖңеҗёзғӯвҖқгҖҒвҖңж”ҫзғӯвҖқ)пјҢиҜҘеҸҚеә”еҢ–еӯҰе№іиЎЎеёёж•°иЎЁиҫҫејҸдёәK=____гҖӮ пјҲ2пјүеңЁжҒ’жё©жҒ’е®№жқЎд»¶дёӢпјҢиғҪеҲӨж–ӯиҜҘеҸҚеә”иҫҫеҲ°е№іиЎЎзҠ¶жҖҒзҡ„дҫқжҚ®жҳҜ____________гҖӮ(з”Ёж–Үеӯ—иЎЁзӨә) пјҲ3пјүиӢҘеңЁдҪ“зі»дёӯеҠ е…ҘеҗҲйҖӮзҡ„еӮ¬еҢ–еүӮпјҢеҲҷиҜҘеҸҚеә”зҡ„еҢ–еӯҰеҸҚйҖҹзҺҮ_________пјҢеҸҚеә”зҡ„зғӯж•Ҳеә”_____ (еқҮйҖүеЎ«вҖңеўһеӨ§вҖқгҖҒвҖңеҮҸе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқ)гҖӮ пјҲ4пјүиҫҫеҲ°е№іиЎЎж—¶пјҢж”№еҸҳдёҖдёӘжқЎд»¶пјҢеҢ–еӯҰе№іиЎЎеёёж•°дёҚеҸҳпјҢAзҡ„иҪ¬еҢ–зҺҮеўһеӨ§пјҢеҲҷиҜҘжқЎд»¶жҳҜ_______гҖӮ пјҲ5пјүFeCl3еӣәдҪ“жә¶дәҺи’ёйҰҸж°ҙеёёдјҡеҮәи§Ғжө‘жөҠпјҢеҫ—дёҚеҲ°жҫ„жё…зҡ„ж°§еҢ–й“Ғжә¶ж¶ІгҖӮе…¶еҺҹеӣ жҳҜ_________пјҢеҰӮжһңиҰҒеҫ—еҲ°жҫ„жё…зҡ„ж°ҜеҢ–й“Ғжә¶ж¶ІпјҢеҸҜйҮҮеҸ–зҡ„жҺӘж–ҪжҳҜ____________гҖӮ |
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
жҳҺзҹҫзҹіжҳҜеҲ¶еҸ–й’ҫиӮҘе’Ңж°ўж°§еҢ–й“қзҡ„йҮҚиҰҒеҺҹж–ҷпјҢжҳҺзҹҫзҹізҡ„з»„жҲҗе’ҢжҳҺзҹҫзӣёдјјпјҢжӯӨеӨ–иҝҳеҗ«жңүж°§еҢ–й“қе’Ңе°‘йҮҸж°§еҢ–й“ҒжқӮиҙЁгҖӮе…·дҪ“е®һйӘҢжӯҘйӘӨеҰӮдёӢеӣҫжүҖзӨә(жҳҺзҹҫзҹіз„ҷзғ§еҗҺжҲҗеҲҶдёҚеҸҳ):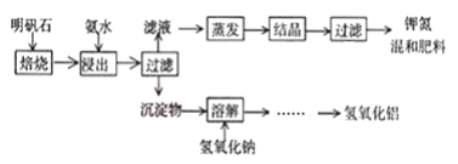 е®ҢжҲҗдёӢеҲ—еЎ«з©ә: пјҲ1пјүвҖңжөёеҮәвҖқеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә_______гҖӮвҖңжөёеҮәвҖқжүҖз”ЁзЁҖж°Ёж°ҙжө“еәҰдёә39.20g/LпјҢй…ҚеҲ¶500mL иҜҘж°Ёж°ҙйңҖ251.28g/L зҡ„жө“ж°Ёж°ҙ________mLгҖӮ пјҲ2пјүвҖңиҝҮж»ӨвҖқжүҖйңҖзҡ„зҺ»з’ғд»ӘеҷЁжңү______________гҖӮ пјҲ3пјүеҶҷеҮәвҖңжә¶и§ЈвҖқиҝҮзЁӢдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ_________гҖҒ________гҖӮ пјҲ4пјүжЈҖйӘҢж»Өж¶ІдёӯжҳҜеҗҰеҗ«жңүSO42- зҡ„е®һйӘҢж–№жі•__________гҖӮ пјҲ5пјүдёәжөӢе®ҡй’ҫж°ЁеӨҚеҗҲиӮҘK2SO4гҖҒ(NH4)2SO4дёӯSO42-зҡ„иҙЁйҮҸеҲҶж•°пјҢи®ҫи®Ўе®һйӘҢжӯҘйӘӨеҰӮдёӢ: в‘ _____________________гҖӮ в‘Ўжә¶дәҺж°ҙпјҢеҠ е…Ҙи¶ійҮҸBaCl2жә¶ж¶ІпјҢеҫ…зҷҪиүІжІүж·ҖдёҚеҶҚдә§з”ҹдёәжӯўгҖӮ в‘ўиҝҮж»ӨгҖҒ______гҖҒ________ (дҫқж¬ЎеЎ«еҶҷе®һйӘҢж“ҚдҪңеҗҚз§°) гҖӮ в‘ЈеҶ·еҚҙгҖҒз§°йҮҸжүҖеҫ—жІүж·Җзҡ„иҙЁйҮҸгҖӮ пјҲ6пјүиӢҘжүҖеҸ–иҜ•ж ·е’ҢжүҖеҫ—жІүж·Җзҡ„иҙЁйҮҸеҲҶеҲ«дёәmgгҖҒng,иҜ•з”Ёеҗ«жңүmгҖҒnзҡ„д»Јж•°ејҸиЎЁзӨәиҜҘй’ҫж°®еӨҚеҗҲиӮҘдёӯSO42-зҡ„иҙЁйҮҸеҲҶж•°дёә________гҖӮ |
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
жңүжңәзү©GжҳҜдёҖз§Қй«ҳеҲҶеӯҗеҢ–еҗҲзү©пјҢеёёз”ЁдҪңжңүжңәеҗҲжҲҗзҡ„дёӯй—ҙдҪ“пјҢ并еҸҜз”ЁдҪңд№іиғ¶жјҶзӯүгҖӮеҸҜд»ҘйҖҡиҝҮд»ҘдёӢйҖ”еҫ„еҗҲжҲҗ: е·ІзҹҘжңүжңәзү©A дёӯеҗ«жңүCгҖҒHгҖҒOгҖҒClеӣӣз§Қе…ғзҙ дё”еҗҢдёҖдёӘзўіеҺҹеӯҗдёҠдёҚзӣҙжҺҘиҝһжҺҘдёӨдёӘе®ҳиғҪеӣўпјҢEжҳҜд№ҷйҶҮзҡ„еҗҢзі»зү©пјҢFзҡ„еҲҶеӯҗејҸдёәC4H6O2гҖӮ е®ҢжҲҗдёӢеҲ—еЎ«з©ә: пјҲ1пјүA зҡ„з»“жһ„з®ҖејҸдёә______жҲ–_________пјҢеҸҚеә”в‘ўзҡ„еҸҚеә”зұ»еһӢ________гҖӮ пјҲ2пјүеҶҷеҮәеҸҚеә”в‘Өе’ҢеҸҚеә”в‘Ҙзҡ„еҢ–еӯҰж–№зЁӢејҸ: еҸҚеә”в‘Ө___________________пјӣеҸҚеә”в‘Ҙ_____________гҖӮ пјҲ3пјүеҶҷеҮәдёӨз§ҚдёҺFеҗ«жңүзӣёеҗҢе®ҳиғҪеӣўзҡ„еҗҢеҲҶејӮжһ„дҪ“зҡ„з»“жһ„з®ҖејҸ_______гҖҒ_______гҖӮ пјҲ4пјүиҜ•и®ҫи®ЎдёҖжқЎд»Ҙ 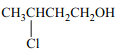 дёәеҺҹж–ҷеҗҲжҲҗ дёәеҺҹж–ҷеҗҲжҲҗ |
|
й«ҳдёӯеҢ–еӯҰ иҜ•еҚ·жҺЁиҚҗ
- з”ҳиӮғзңҒйқҷе®ҒеҺҝ第дёҖдёӯеӯҰ2021еұҠй«ҳдёүдёҠеҶҢ第еӣӣж¬ЎжЁЎжӢҹиҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- ж»•е·һеёӮй«ҳдәҢеҢ–еӯҰдёӢеҶҢжңҲиҖғиҜ•еҚ·иҖғйўҳеҗҢжӯҘи®ӯз»ғ
- иЎЎйҳіеёӮй«ҳдёүеҢ–еӯҰ2019е№ҙдёҠеҚҠжңҹй«ҳиҖғжЁЎжӢҹе®Ңж•ҙиҜ•еҚ·
- жұҹиӢҸй«ҳдәҢеҢ–еӯҰжңҲиҖғжөӢйӘҢпјҲ2019е№ҙдёҠжңҹпјүеёҰеҸӮиҖғзӯ”жЎҲдёҺи§Јжһҗ
- 2018-2019е№ҙй«ҳдәҢдёӢеҚҠе№ҙејҖеӯҰиҖғиҜ•еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·пјҲеҗүжһ—зңҒй•ҝжҳҘеӨ–еӣҪиҜӯеӯҰж Ўпјү
- жӯҰйӮ‘дёӯеӯҰ2019е№ҙй«ҳдәҢеҢ–еӯҰдёҠеӯҰжңҹжңҲиҖғжөӢйӘҢеңЁзәҝеҒҡйўҳ
- жІӘ科зүҲеҢ–еӯҰжӢ“еұ•жҖ§иҜҫзЁӢ4гҖҠзҰ»еӯҗдә’жҚўеҸҚеә”е’Ңж°§еҢ–иҝҳеҺҹеҸҚеә”гҖӢжөӢиҜ•еҚ·
- еҗҲиӮҘеёӮй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•йўҳеёҰзӯ”жЎҲе’Ңи§Јжһҗ
жңҖиҝ‘жӣҙж–°