华宁一中2019年高二化学上学期开学考试试卷完整版
| 1. 选择题 | 详细信息 |
|
下列物质中不属于糖类的是( ) A. 酶 B. 蔗糖 C. 淀粉 D. 葡萄糖 |
|
| 2. 选择题 | 详细信息 |
|
下列是有关生活中的醋酸,其中主要利用了醋酸酸性的是( )。 ①醋酸不小心滴到大理石桌面上,桌面失去光泽 ②熏醋可一定程度上防止流行性感冒 ③醋可以除去水壶上的水垢 ④用醋烹饪鱼,除去鱼的腥味 A.①③ B.②④ C.①④ D.②③ |
|
| 3. 选择题 | 详细信息 |
|
下列关于甲烷、乙烷、丙烷的说法正确的是( ) A. 它们的分子空间结构都是正四面体 B. 都能使酸性高锰酸钾溶液褪色 C. 光照条件下,都能与氯气发生取代反应 D. 乙烷的熔、沸点比丙烷高 |
|
| 4. 选择题 | 详细信息 |
|
决定气体体积的因素:①气体分子的直径、②气体的物质的量多少、③气体分子间的平均距离、④气体分子的相对分子质量,则决定气体体积的因素主要为( ) A. ①② B. ①③ C. ②③ D. ②④ |
|
| 5. 选择题 | 详细信息 |
|
分类是化学学习与研究的常用方法,下列分类正确的是( ) A. Na2O、MgO、Al2O3均属于碱性氧化物 B. 石灰石、生石灰、熟石灰均属于碱 C. 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 D. 根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
|
| 6. 选择题 | 详细信息 |
用如图所示装置进行如下实验,能达到实验目的是 A. 瓶中盛满水,从A口进气,用排水法收集氢气 B. 瓶中盛适量浓硫酸,从A口进气来干燥氨气 C. 从B口进气,用排空气法收集二氧化碳 D. 瓶中装满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
|
| 7. 选择题 | 详细信息 |
|
实验中需2 mol·L-1的碳酸钠溶液950 mL,配制时应选用的容量瓶的规格是 A. 1 000 mL B. 950 mL C. 900 mL D. 500 mL |
|
| 8. 选择题 | 详细信息 |
有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3,试管中各有10mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是 A. 甲装置的气球膨胀速率大 B. 若最终两气球体积相同,则一定有c(HCl)≥2 mol/L C. 若最终两气球体积不同,则一定有c(HCl)≤1 mol/L D. 最终两溶液中Na+、Cl﹣的物质的量相同 |
|
| 9. 选择题 | 详细信息 |
|
除去铁粉中混有的少量铝粉,可选用的试剂是( ) A. H2O B. 浓H2SO4 C. NaCl D. NaOH |
|
| 10. 选择题 | 详细信息 |
|
能用铝作原料来冶炼难熔的金属是因为( ) A.铝的密度小,熔点较低 B.铝在空气中燃烧放出大量的热 C.铝在金属活动性顺序表中排在较前面 D.铝具有还原性,发生铝热反应时放出大量热 |
|
| 11. 选择题 | 详细信息 |
|
下列说法不正确的是( ) A. 烷烃分子中一定含有极性键 B. 烷烃分子中不一定含有非极性键 C. 烷烃分子中可能含有离子键 D. 烷烃分子中的化学键都为共价单键 |
|
| 12. 选择题 | 详细信息 |
|
根据成键元素判断下列化合物中含有离子键的是( ) A. HF B. H2O C. H2SO4 D. MgO |
|
| 13. 选择题 | 详细信息 |
|
1919年,科学家第一次实现了人类多年的梦想——人工转变元素。这个核反应如下: A. B. C. O2和O3互为同位素 D. 通常情况下,He和N2化学性质都很稳定 |
|
| 14. 选择题 | 详细信息 |
|
一般检验SO42-的试剂是 A. BaCl2、稀硝酸 B. AgNO3、稀硝酸 C. 稀盐酸、BaCl2 D. AgNO3、稀盐酸 |
|
| 15. 选择题 | 详细信息 |
|
用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”字,放置片刻,用少量水将铜片上的溶液冲到小烧杯中,下列说法正确的是( ) A. 烧杯中的溶液呈棕黄色 B. 铜片无任何变化 C. 铜片上的凹凸陷的“Cu”字 D. 发生发应:Fe3++Cu==Cu3++Fe2+ |
|
| 16. 选择题 | 详细信息 |
|
下列变化不属于化学变化的是( ), A. 煤的干馏 B. 石油分馏 C. 由乙烯制聚乙烯 D. 重油裂化 |
|
| 17. 选择题 | 详细信息 |
|
下列物质中不能电离出酸根离子的是( ) A. Ca(OH)2 B. KMnO4 C. KClO3 D. NaHSO4 |
|
| 18. 选择题 | 详细信息 |
|
氰(CN)2、硫氰(SCN)2等称为拟卤素,它们与卤素单质性质相似,它们的阴离子也与卤素阴离子性质相似。例如:2Fe+3(SCN)2==2Fe(SCN)3、Ag++CN-== AgCN↓(白)。拟卤素形成的无氧酸和含氧酸一般比氢卤酸和次卤酸弱,阴离子的还原性一般比Br-强。下列反应中,不正确的是( ) A. 2CN-+Cl2= 2Cl-+(CN)2 B. (CN)2+2OH-=CN-+CNO-+H2O C. (SCN)2+H2O = 2H++SCN-+SCNO- D. MnO2+4HSCN(浓) |
|
| 19. 选择题 | 详细信息 |
如图表示一个化学反应过程,图中的黑球表示两个相同的单糖或其单元。 则图中的a、b、c分别表示( ) A. 麦芽糖 麦芽糖酶 葡萄糖 B. 蔗糖 蔗糖酶 果糖 C. 乳糖 乳糖酶 葡萄糖 D. 淀粉 淀粉酶 葡萄糖 |
|
| 20. 选择题 | 详细信息 |
|
有下列实验:①过滤、②蒸发结晶、③固体溶解、④取用液体、⑤取用固体,其中都需要使用玻璃棒的是( ) A. ①②③ B. ④⑤ C. ①④ D. ①③⑤ |
|
| 21. 选择题 | 详细信息 |
一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( ) A. 电池工作时,电子由a流向b B. 微生物所在电极区放电时发生还原反应 C. 放电过程中,H+从正极区移向负极区 D. 正极反应式为:MnO2+4H++2e-===Mn2++2H2O |
|
| 22. 选择题 | 详细信息 |
|
氰[(CN)2]、硫氰[(SCN)2]等称为拟卤素,它们与卤素单质性质相似,它们的阴离子也与卤素阴离子性质相似。例如:2Fe+3(SCN)2===2Fe(SCN)3、Ag++CN-===AgCN↓(白)。拟卤素形成的无氧酸和含氧酸一般比氢卤酸和次卤酸弱,阴离子的还原性一般比Br-强。下列反应中,不正确的是( ) A. 2CN-+Cl2=2Cl-+(CN)2 B. (CN)2+2OH-=CN-+CNO-+H2O C. (OCN)2+H2O =2H++OCN-+OCNO- D. MnO2+4HSCN |
|
| 23. 选择题 | 详细信息 |
|
阴离子和阳离子都为稀有气体元素原子结构,且阳离子比阴离子少两个电子层的离子化合物是( ) A. MgCl2 B. BaF2 C. NaBr D. NaI |
|
| 24. 选择题 | 详细信息 |
|
关于三氧化硫的下列说法中,不正确的是 ( ) A. 常温下是一种易溶于水的气体 B. 能与碱反应生成硫酸盐和水 C. 能与氯化钡溶液反应产生沉淀 D. 能使石蕊试液变红色 |
|
| 25. 选择题 | 详细信息 |
|
已知NA为阿伏加德罗常数的数值,Vm为气体摩尔体积,下列说法中正确的是( ) A. 2.4g 镁离子所含电子数目为1.2NA B. 标准状况下,22.4L汞所含分子数目为NA C. Vm体积甲烷所含质子数目为10NA D. 18g铵根离子所含电子数目为11NA |
|
| 26. 选择题 | 详细信息 |
|
下列各组物质中,按酸、碱、盐、碱性氧化物、酸性氧化物的顺序排列正确的是( ) A. 盐酸、纯碱、氯酸钾、氧化镁、二氧化硅 B. 硝酸、烧碱、次氯酸钠、氧化钙、二氧化硫 C. 碳酸、消石灰、硫酸铵、一氧化碳、三氧化硫 D. 醋酸、烧碱、生石灰、氧化铁、二氧化碳 |
|
| 27. 推断题 | 详细信息 |
(1)将红热的固体单质甲放入显黄色的浓乙溶液中,剧烈反应,产生混合气体A,A在常温下不与空气作用,发生如下图所示的变化。 则:①写出下列物质的化学式: 丙__________,B____________,C__________, D____________。 ②写出甲跟乙反应的化学方程式:__________________________。 ③单质丙与溶液乙反应生成气体B的离子方程式:___________________。 (2)如图是各物质的反应关系图:已知A和E都是黄色粉末,F有刺激性气味且有漂白性。请据此回答下列问题: 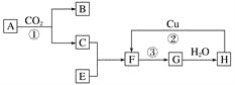 写出图中编号的化学方程式: ①_______________________; ②_______________________; ③______________________。 |
|
| 28. 综合题 | 详细信息 |
海水中溴元素以Br﹣形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图: 请回答下列问题. (1)将海水浓缩的方法是__; (2)步骤①反应的离子方程式是__,1molCl2参加反应,转移电子__mol; (3)步骤②通入热空气吹出Br2,利用了Br2的__(填序号); A.氧化性 B.还原性 C.挥发性 D.腐蚀性 (4)步骤③中用SO2的水溶液吸收Br2,吸收率可达95%,该反应的氧化剂是__,在工业生产中此步骤应解决的问题是__. |
|
| 29. 实验题 | 详细信息 |
某课外小组同学设计如图实验装置(部分夹持仪器未画出)探究氨气的还原性并检验部分产物。 (1)若A中使用装置Ⅰ制取氨气,则化学方程式为__,发生装置试管口略向下倾斜的原因_____;若A中使用装置Ⅱ制取氨气,则分液漏斗中的试剂为__,圆底烧瓶中的固体可以为__。 (2)B中碱石灰的作用是__。 (3)氨气还原炽热氧化铜的化学方程式为__,装置C中的实验现象为__,装置D中的实验现象为__。 (4)①该装置存在明显的缺陷是__。 ②请画出改进后需要增加连接的实验装置图________。 |
|
| 30. 综合题 | 详细信息 |
已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2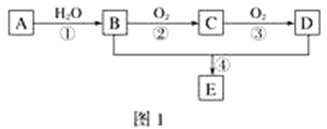 (1)写出下列物质的官能团名称:B:____________________;D:____________________。 (2)反应④的化学方程式为________________________________________________,反应类型:________。 (3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。 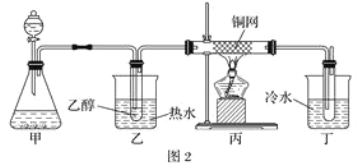 ①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。 A.Na2O2 B.KClC.Na2CO3 D.MnO2 ②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。 ③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。 |
|
| 31. 推断题 | 详细信息 |
已知:①R-NO2 (1)A转化为B的化学方程式是______________________________。 (2)图中“苯→①→②”省略了反应条件,请写出①②物质的结构简式:①__________,②_______。 (3)苯的二氯代物有________种同分异构体。 (4)有机物  的所有原子________(填“是”或“不是”)在同一平面上。 的所有原子________(填“是”或“不是”)在同一平面上。 |
|
最近更新



