辽宁2019年九年级下半期化学中考模拟试卷带答案和解析
| 1. | 详细信息 |
|
下列说法正确的是( ) A. 在化学变化中往往会伴随能量变化 B. 通过化学变化可以改变原子的种类和个数 C. 改变物质的性质一定要通过化学变化 D. 在化学变化中原子中的电子数不会发生变化 |
|
| 2. | 详细信息 |
|
分类法是学习化学的重要方法之一。从组成角度分析,下列四种物质中有一种与另外三种明显不同,该物质是( ) A. 二氧化碳 B. 氯化钠 C. 氧化钙 D. 水 |
|
| 3. | 详细信息 |
|
从图所示的两种微粒结构示意图中,所获取信息正确的个数是( ) (1)它们属于同种元素 (2)它们的核外电子层数相同 (3)它们的原子的核外电子数相同 (4)①表示阳离子,②表示原子 (5)它们均达到稳定结构 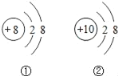 A. 1 B. 2 C. 3 D. 4 |
|
| 4. | 详细信息 |
|
在AgNO3、Mg(NO3)2和Cu(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子是( ) A. Cu2+ B. 只有Fe2+ C. Fe2+和Fe3+ D. Mg2+和Fe2+ |
|
| 5. | 详细信息 |
|
鉴别下列各组物质,选用的试剂(括号内)不合理的是( ) A. CO2和N2(澄清石灰水) B. Ca(OH)2溶液和NaOH溶液(稀盐酸) C. NaOH溶液和稀H2SO4(pH试纸) D. 蒸馏水和海水(硝酸银溶液) |
|
| 6. | 详细信息 |
|
在化学反应A+2B=C+D中,若5.6g A和7.3g B恰好完全反应,生成12.7g C,现在要得到0.4g D,需要A的质量为( ) A. 5.6g B. 11.2g C. 14.6g D. 无法计算 |
|
| 7. | 详细信息 | |||||||||||||||
丰富的化学知识能帮助我们识别伪劣商品,下列鉴别伪劣商品的方法中错误的是( )
|
||||||||||||||||
| 8. | 详细信息 |
|
汽车轮胎的主要成分是( ) A. 合成橡胶 B. 合成纤维 C. 塑料 D. 合金钢 |
|
| 9. | 详细信息 |
|
下列各组物质的溶液不用其他试剂无法鉴别的是( ) A. HCl、NaOH、MgSO4、CuSO4 B. NaNO3、HCl、CaCl2、KOH C. Na2CO3、K2SO4、BaC12,HCl D. H2SO4、NaCl、Na2CO3、CaCl2 |
|
| 10. | 详细信息 |
甲乙两种物质的溶解度曲线如图所示,下列说法正确的是( )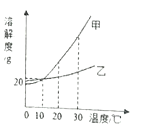 A. 常温下,乙易溶于水 B. 10℃时,甲和乙的饱和溶液各100g,其溶质质量都是20g C. 将等质量的甲乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙 D. 20℃时,甲的不饱和溶液变为饱和溶液,可采取升温的方法 |
|
| 11. | 详细信息 |
|
下列物质分别与100g 36.5%的盐酸恰好完全反应,反应后所得溶液中溶质的质量分数最小的是( ) A. Mg B. MgO C. Mg(OH)2 D. MgCO3 |
|
| 12. | 详细信息 |
|
请用化学用语填空: (1)两个铁离子_____。 (2)标出氧化铝中铝元素的化合价_____。 (3)最简单的有机物_____。 (4)空气中含量最多的气体_____。 |
|
| 13. | 详细信息 |
|
请将下列物质进行分类(填序号): ①苛性钠 ②过氧化氢溶液 ③冰水混合物 ④纯碱 ⑤甲烷 ⑥金刚石 属于有机物的是_____,属于单质的是_____,属于碱的是_____,属于盐的是_____,属于混合物的是_____. |
|
| 14. | 详细信息 |
|
请用所学的化学知识填空 (1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具有_____性; (2)Ca(OH)2和NaOH化学性质相似,是因为它们的溶液中都含有_____(填符号) (3)酸和碱能发生中和反应,生成_____和水,这一性质在日常生活和工农业生产中有广泛的应用,如_____(举一实例) |
|
| 15. | 详细信息 |
“他已褪去少年的青涩,淋漓尽致的表演充满了成长的力量。”20岁的哈尔滨小伙博洋,自2018年年初的四大洲花样滑冰锦标赛自由滑比赛中完美发挥,全场零失误,一举夺得冠军。 (1)运动员每日饮食需要营养的严格配比,牛肉炖柿子是运动员比较喜爱的一道美食,其中西红柿富含的营养素可以起到调节新陈代谢,______和维持身体健康的作用。而牛肉中富含的营养素(除水外)主要是______。 (2)大米是由水稻磨制而成的,水稻在种植过程中需施加钾肥,其主要作用是保证各种代谢过程的顺利进行,促进植物生长,增强_________能力等功能,若还需使水稻叶色浓绿,则能同时提供这两种营养元素的复合肥是______(填化学式)。 (3)如果运动员穿的衣服面料是由一种纤维材料制成的,具有强度高、弹性好、耐磨、耐化学腐蚀的性能,则制作该面料的纤维种类为_____(填字母)。 A.羊毛纤维 B.棉纤维 C.合成纤维 |
|
| 16. | 详细信息 |
|
通过一年化学课的学习,我们知道,除了催化剂可以改变化学反应速率外,下列因素都会影响化学反应的速率,请你说明发生了什么影响,并各举一例. (1)反应物的浓度_____; (2)反应物的接触面积_____; (3)温度_____. |
|
| 17. | 详细信息 |
某同学欲用如图所示的五个实验来验证复分解反应发生的条件,分析并回答问题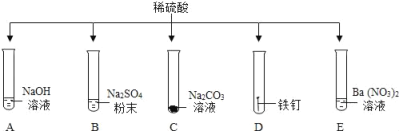 (1)从物质类别和构成的角度分析,铁钉、_____与稀H2SO4混合的实验没有必要做。 (2)上述_____(填序号)实验能发生复分解反应,但没有明显现象,为证明两者能够反应,你的操作是_____。 (3)写出上述实验中有沉淀生成的反应的化学方程式_____。 |
|
| 18. | 详细信息 |
|
请用“<”、“>”或“﹦”填空. (1)相同条件下在水中的溶解性:氢氧化钙_____氢氧化钠; (2)pH:蒸馏水_____酸雨; (3)氮元素的化合价:亚硝酸钠_____ 氯化铵; (4)溶液的质量:100g硫酸铜溶液_____ 100g硫酸铜溶液与足量铁充分反应后的溶液. |
|
| 19. | 详细信息 |
|
有一包白色固体粉末,可能由Na2CO3、Na2SO4、CuSO4、NaNO3中的一种或几种物质组成,为检验其组成,做了以下实验:①取少量固体混合物溶于水,搅拌后得无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀盐酸中,发现沉淀全部溶解。 (1)试判断:白色固体中肯定含有_____,肯定没有_____,可能有_____。 (2)实验步骤③反应的化学方程式为_____。 |
|
| 20. | 详细信息 |
图为实验室制取气体的常用装置及改进装置。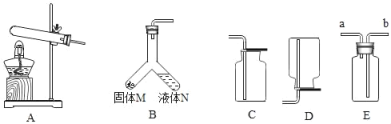 (1)用A装置制取气体时,试管口常低于试管底部,目的是_____。 (2)将改进装置B向左或右倾斜,使两种药品混合,即可制得气体。用装置B不能制取的气体有_____。 A加热KClO3和MnO2制取O2 B用大理石与稀盐酸反应制取CO2 C用锌与稀硫酸反应制取H2 DCO2与炽热的碳反应制取CO (3)张明同学认为,实验室也可用B装置制取O2,若能,发生反应的化学方程式为_____,固体M的作用是_____。 (4)用装置E收集CO2,验满时将燃着的木条放在_____(填“a”或“b”)处。 (5)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(已知氨气密度比空气小,易溶于水)。若图中装置均从左至右连接,则制取氨气可选用实验装置为_____(填序号)。 A A和C B A和D C B和D D A和E |
|
| 21. | 详细信息 |
鉴别稀盐酸、稀硫酸、Ba(OH)2溶液、Na2CO3溶液和NaCl溶液五瓶无标签的溶液时,将它们随意编号为A、B、C、D、E后进行如下实验: (1)根据以上实验过程,确定C溶液是_____,B、E混合时的现象为_____; (2)鉴别后把所有物质混合倒入同一烧杯中,发现混合物呈浑浊状,过滤后,滤液呈红色。说明滤液呈_____性,则滤渣的成分是_____; (3)为了防止滤液污染环境,向滤液中逐滴加入过量的Na2CO3溶液时,发现先有气泡产生,后有白色沉淀生成。综合以上实验过程判断,加入Na2CO3溶液前,滤液中含有的溶质除石蕊外,一定还有_____。 |
|
| 22. | 详细信息 | ||||||
|
二氧化碳的过度排放会引起系列环境问题。某化学兴趣小组的同学设计了如下图的方法来吸收转化工业废气中的二氧化碳(部分产物已略)。 (1)下列环境问题与CO2有关的是_____(填字母序号)。 A酸雨 B温室效应 C臭氧空洞 D白色污染 (2)第Ⅰ步中不用价格更低的Ca(OH)2来直接吸收CO2的主要原因是_____。 (3)第Ⅱ步反应的化学方程式是_____。 (4)CaCO3在医疗上可用作_____。 (5)已知部分原料的价格如下表所示。
|
|||||||
| 23. | 详细信息 |
锌是人体健康所必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫力功能底下。市售的葡萄糖酸锌口服液对治疗锌缺乏症具有较好的疗效。如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息通过计算回答以下问题: (1)葡萄糖酸锌是由_____种元素组成的; (2)葡萄糖酸锌中碳、氢元素质量比为_____; (3)葡萄糖酸锌中锌元素的质量分数为_____;(精确到0.01%) (4)某患者除正常饮食吸收锌元素外,还需服用该品牌葡萄糖酸锌口服液。若治疗时每天还需要补充13mg锌元素,则此患者每天需要服用该口服液_____支。 |
|
| 24. | 详细信息 |
某粗盐中除NaCl以外还含有少量杂质MgCl2,为了测定粗盐中MgCl2的质量分数。取固体样品50.0g完全溶解于150.0g水中,并向其中逐渐加入一定浓度的NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如图所示: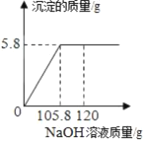 注:发生反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl 请根据相关信息完成下列计算: (1)反应完全时,生成氢氧化镁的质量为_____g; (2)在粗盐中氯化镁的质量分数;_____ (3)恰好完全反应时得到的溶液中溶质的质量分数。_____ |
|
最近更新



