广东高三化学月考测验(2019年上学期)完整试卷
| 1. 选择题 | 详细信息 |
|
《新修本草》中关于“青矾”的描述:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中说:“青矾厂气熏人,衣服当之易烂,栽木不茂”,下列相关叙述不正确的是 A. 赤色固体可能是Fe2O3 B. 青矾宜密闭保存,防止氧化变质 C. 青矾燃烧过程中发生了电子转移 D. “青矾厂气”可能是CO和CO2 |
|
| 2. 选择题 | 详细信息 |
|
NA代表阿伏加德罗常数的值。下列说法正确的是 A.1 mol CH3COOC2H5在稀硫酸中水解可得到的乙醇分子数为NA B.pH=1的H2SO3溶液中,含有0.1 NA个H+ C.1 mol Fe分别与足量的稀硫酸和稀硝酸反应转移电子数均为3NA D.常温常压下,56g丙烯与环丁烷的混合气体中含有4NA个碳原子 |
|
| 3. 选择题 | 详细信息 |
|
化学与生活、生产密切相关,下列说法正确的是 A.常用于染料、医药、农药等的酚类物质可来源于煤的干馏 B.大豆中含有丰富的蛋白质,豆浆煮沸后蛋白质全部变为了氨基酸 C.可以用酸性高锰酸钾溶液鉴别苯和直馏汽油 D.涤纶、有机玻璃、光导纤维都是有机高分子化合物 |
|
| 4. 选择题 | 详细信息 |
|
KIO3可作为食盐中的补碘剂。利用“KIO3氧化法”制备KIO3包括以下两个反应:①11KClO3+6I2+3H2O=6KH(IO3)2+3Cl2↑+5KCl ② 2KH(IO3)2+KOH=2KIO3+H2O下列说法正确的是 A.反应①表明氧化性:KH(IO3)2>KClO3 B.反应①中每转移4mol电子生成2.24L Cl2 C.向淀粉溶液中加入少量碘盐,溶液会变蓝 D.可用焰色反应实验证明碘盐中含有钾元素 |
|
| 5. 选择题 | 详细信息 |
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在 pH=5时沉淀完全).其中分析错误的是 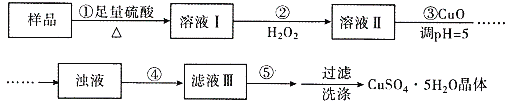 A. 步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O B. 步骤②不能用氯水、硝酸等强氧化剂代替H2O2 C. 步骤④为过滤,步骤⑤蒸发结晶 D. 步骤③用 CuCO3代替CuO也可调节溶液的pH |
|
| 6. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
|
|||||||||||||||||||||
| 7. 选择题 | 详细信息 | ||||||||||||
实验室处理含FeBr3废催化剂的溶液,可得到溴的苯溶液和无水FeCl3。下列做法能达到相应实验目的的是
|
|||||||||||||
| 8. 实验题 | 详细信息 |
四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置略去)。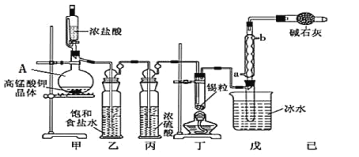 有关信息如下表  回答下列问题: (1)甲装置中仪器A的名称为_________。 (2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为_____________。 (3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到______(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是: ①促进氯气与锡反应; ②_________。 (4)乙装置的作用 __________,如果缺少乙装置,可能发生的副反应的化学方程式为___________;己装置的作用是__________(填序号) A.防止空气中CO2气体进入戊装置 B.除去未反应的氯气,防止污染空气 C.防止水蒸气进入戊装置的试管中使产物水解 D.防止空气中O2进入戊装置的试管中使产物氧化 (5)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.04g SnCl4,则SnCl4的产率为________。(保留2位有效数字) |
|
| 9. | 详细信息 |
从海水中提取溴的工业流程如图: (1)步骤I中将卤水酸化,再通入Cl2,是为了防止Cl2与碱反应,写出Cl2与碱反应的离子方程式_____。 (2)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是__________。 (3)实验室保存液溴时,通常在盛液溴的试剂瓶中加少量的水,这与液溴的_____性质有关(填写序号)。 A.氧化性 B.还原性 C.挥发性 D.密度比水大 (4)步骤II中将吹出的溴蒸汽用纯碱溶液吸收时还有CO2生成,写出吸收时发生反应的离子方程式:___。 (5)步骤II中通入热空气吹出的Br2用纯碱溶液吸收前先经过NaBr溶液,其目的是______________。 (6)步骤III中蒸馏出工业溴后残留液的主要溶质是_______________。 (7)步骤III中若使用硝酸酸化,缺点是_________。 |
|
| 10. | 详细信息 | ||||||||
铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工业流程如下: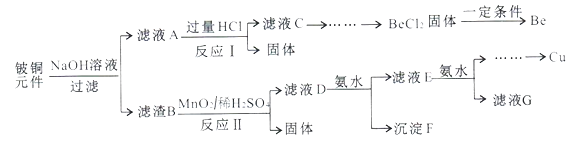 已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
|
|||||||||
| 11. 推断题 | 详细信息 |
氨甲环酸(G)别名止血环酸,是一种已被广泛使用半个世纪的止血药,它的一种合成路线如下(部分反应条件和试剂略):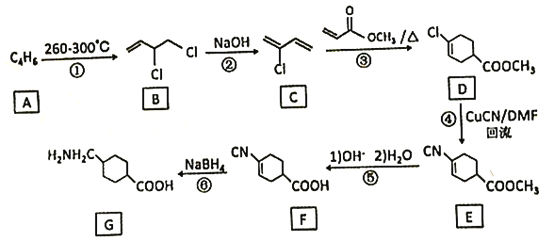 回答下列问题: (1)A的结构简式是____。C的化学名称是_______。 (2)G在NaOH催化下发生双分子脱水形成仅含两个环的有机物,写出该反应的化学反应方程式____。 (3)①~⑥中属于取代反应的是_________。 (4)E中不含N原子的官能团名称为___________。 (5)氨甲环酸(G)的分子式为__________。 (6)满足以下条件的所有E的同分异构体有_____种。 a.含苯环 b.含硝基 c.苯环上只有两个取代基 (7)写出以  的合成路线:_______(无机试剂任性) 的合成路线:_______(无机试剂任性) |
|
- 2019届高三上册一模检测理科综合化学题带答案和解析(安徽省黄山市)
- 江苏省常州市第二中学2020-2021年高二上册期中联合调研考试化学网上检测无纸试卷带答案和解析
- 广西岑溪市2020-2021年高一上学期期中考试化学免费试题带答案和解析
- 2019-2020年高一上学期期中联考化学试卷带参考答案和解析(江西省南昌市八一中学、洪都中学、十七中、实验中学、南师附
- 清远市高三化学下册月考试卷题带答案和解析
- 吉林高一化学期中考试(2018年前半期)试卷带答案和解析
- 广西壮族自治区南宁市育才实验中学2020-2021年高一前半期期中考试化学在线考试题免费练习
- 2018至2019年高二后半期期中考试化学试卷(江苏省启东中学)