2019-2020年九年级上册期中化学考题(山东省淄博市临淄区边河乡中学)
| 1. 选择题 | 详细信息 |
|
即食即热型快餐的内层是用铝箔真空包装的食物,外层则分别包装两包物质,使用时拉动预留在外的拉线,使这两种物质反应,便可对食物进行加热,这两包物质最适合的选择是( ) A.浓硫酸与水 B.生石灰与水 C.熟石灰与水 D.锌与稀硫酸 |
|
| 2. 选择题 | 详细信息 |
|
如图是硫酸试剂瓶标签上的部分内容,认真观察此标签,从中不能获取的信息是( ) 硫酸化学纯(CR)(500mL) 品名:硫酸 化学式H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% A.硫酸的化学性质 B.硫酸的物理性质 C.硫酸中各元素的质量比 D.硫酸中硫元素的质量分数 |
|
| 3. 选择题 | 详细信息 |
|
下列质量增加的变化有一种与其他三种存在着本质的区别,这种变化是 A. 长期放置在空气中的氢氧化钠质量增加 B. 久置在潮湿空气中的铁钉质量增加 C. 久置在空气中的生石灰质量增加 D. 长期敞口放置的浓硫酸质量增加 |
|
| 4. 选择题 | 详细信息 |
|
下列各组物质的名称或俗名与化学式表示的是同一种物质( ) A.消石灰 生石灰 CaO B.铁锈 氢氧化铁 Fe(OH)3 C.氯化钠 食盐 NaCl D.烧碱 纯碱 Na2CO3 |
|
| 5. 选择题 | 详细信息 |
|
逻辑推理是化学学习常用的思维方法。下列推理正确的是( ) A.酸性溶液的pH都小于7,所以酸溶液pH一定小于7 B.氧化物都含氧元素,所以含氧元素的化合物都是氧化物 C.水是纯净物,所以海水也是纯净物 D.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
|
| 6. 选择题 | 详细信息 |
|
一些食物的近似pH如下:牛奶6.3~6.6;鸡蛋清7.6~8.0;柠檬2.2~2.4;番茄4.0-4.4。其中碱性最强的是( ) A. 牛奶 B. 柠檬 C. 鸡蛋清 D. 番茄 |
|
| 7. 选择题 | 详细信息 |
|
下图X、Y、Z表示的是水、石灰水、稀盐酸的近似pH。下列判断错误的是: A. X是稀盐酸 B. Y是水 C. Z是石灰水 D. 无法确定X、Y、Z |
|
| 8. 选择题 | 详细信息 |
如图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中导管口有较多气泡产生,则液体A和固体B的组合不可能是 A.双氧水和二氧化锰 B.水和生石灰 C.水和氢氧化钠 D.水和硝酸铵 |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
为了除去下列物质中的杂质(括号内为杂质),选用的试剂和操作方法都正确的是( )
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
|
生活中的洗涤问题大都与化学知识有关.下列说法中不正确的是 ( ) A.洗涤剂能够除去油污的原因是因为洗涤剂具有乳化作用 B.汽油能够除去油污的原因是汽油能够溶解油污从而挥发除去 C.食醋能够除去热水瓶中水垢的原因是二者发生了化学反应 D.盐酸能够除去铁制品表面上的铁锈的原因是二者发生了物理变化 |
|
| 11. 选择题 | 详细信息 |
|
下列溶液仍然是饱和溶液的是( ) A.饱和石灰水降温 B.饱和石灰水表面结了一层膜 C.室温下的饱和硝酸钾溶液放进冰箱 D.向饱和蔗糖水里加水 |
|
| 12. 选择题 | 详细信息 |
|
化学是以实验为基础的自然科学,通过实验可以得知物质的组成 、结构、性质及其变化规律。下列通过实验得出的结论正确的是( ) A.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液一定是碱溶液 B.白磷可以在氧气中燃烧,说明氧气具有可燃性 C.把燃着的木条插入某无色气体中,火焰熄灭,该气体可能是二氧化碳 D.向某无色溶液中滴入BaCl2溶液,产生白色沉淀,证明该溶液一定是稀硫酸 |
|
| 13. 选择题 | 详细信息 |
|
下列能发生中和反应的是( ) A.氢氧化钠与二氧化碳 B.石灰水与稀盐酸 C.稀硫酸与氧化铜 D.二氧化碳与氧化钠 |
|
| 14. 选择题 | 详细信息 |
|
为了区别海水和雨水,可分别加入下列哪种试剂( ) A.盐酸 B.硝酸银溶液 C.酚酞试液 D.PH试纸 |
|
| 15. 选择题 | 详细信息 |
|
20℃时,将100g某物质的溶液蒸干,得到30g固体,则下列说法正确的是( ) A.20℃时,该物质溶解度为30g B.该溶液的溶质的质量分数为30% C.20℃时,该物质为饱和溶液 D.无法计算该溶液的溶质的质量分数 |
|
| 16. 选择题 | 详细信息 |
|
溶液与我们的生活息息相关。下列叙述正确的是( ) A.溶液一定是均一、稳定、无色透明的液体 B.溶剂体积加溶质休积等于溶液的休积 C.配制100g 10%的氯化钠溶液的操作步骤:计算、称量、溶解、装瓶存放 D.溶液中只能有一种溶质 |
|
| 17. | 详细信息 |
|
将100g25%的硝酸钾溶液稀释,取10g稀释后的溶液,经测定得知其溶质质量分数为10%,则稀释原溶液时所用水的质量是 A. 50g B. 100g C. 150g D. 200g |
|
| 18. 选择题 | 详细信息 |
(09年恩施)右图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是 ( ) A.t1℃时甲、乙、丙三者的溶解度相等 B.t1℃时甲、乙、丙三者饱和溶液的溶质质量分数相等 C.要使t1℃时甲的饱和溶液变成不饱和溶液可以采取升高温度的方法 D.t2℃ 时,往100g水中加入90g甲,充分搅拌后得到190g甲的溶液 |
|
| 19. 填空题 | 详细信息 |
|
从下列物质选择填空(填写物质的化学式): ①氢氧化铝②熟石灰③生石灰④氧气⑤稀硫酸 (1)供急救病人呼吸的是_____; (2)用于治疗胃酸过多的是_____; (3)用于改良酸性土壤的是_____; (4)用作干燥剂的是_____; (5)用于金属表面除锈的是_____。 |
|
| 20. 填空题 | 详细信息 |
| 将一枚生锈的铁钉放入足量的稀硫酸中,你首先观察到的现象是_____,化学方程式_____,过一会儿,你还可以观察到的现象是_____、_____,请写出有关反应的化学方程式_____。 | |
| 21. 填空题 | 详细信息 | |||||||||||||||
请根据下表回答有关问题:(各小题均用序号填空)
|
||||||||||||||||
| 22. 填空题 | 详细信息 | ||||
右图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题: (1)氯化钠溶液中的溶剂是 ; (2)10℃时,碳酸钠的溶解度为 g; (3)30℃时,氯化钠的溶解度 碳酸钠的溶解度(填写“>”、“<”或“=”); (4)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是 溶液(填化学式); (5)如右图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是________(填字母序号)。 
|
|||||
| 23. 填空题 | 详细信息 |
按照组成和性质对物质进行分类是化学学习的一种方法,下图中虚线圈内是对应类别的物质的具体实例。请仿例在空白实线圈内填上相应的内容: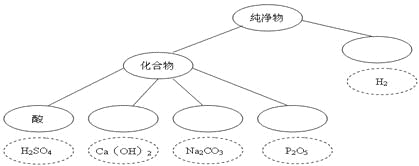 任选虚线圈中的物质作为反应物,写出一个能发生复分解反应的方程式 。 |
|
| 24. 填空题 | 详细信息 |
| 久盛石灰水的试剂瓶内壁常附有一层白膜,其形成的原因是_____(用化学方程式表示),要洗去这层白膜的最好方法是加入_____,化学方程式_____。 | |
| 25. 填空题 | 详细信息 |
| 决定溶液酸性强弱的是溶液中_____,10%的稀硫酸pH_____(填“大于、小于或等于”)5%的稀硫酸。如果想要使氢氧化钙溶液的pH降低,你采用不发生化学变化的方法是加_____,发生化学变化的方法是加_____、_____(所选物质的类别不同)。 | |
| 26. 推断题 | 详细信息 |
|
某同学在A、B两只盛有无色溶液的玻璃杯中,分别倒入一种液体(盐溶液),同学们看到下列奇特现象:A杯变成了“汽水”(产生大量的气泡);B杯中变成了“牛奶”(有白色沉淀)。请你回答:A杯中原来的无色溶液可能是_____(化学式),B杯中原来的无色溶液可能是_____(化学式),倒入盐溶液可能是_____(化学式), A杯中发生的化学方程式_____, B杯中发生的化学方程式_____。 |
|
| 27. 填空题 | 详细信息 |
实验室中要配制一定溶质质量分数的氯化钠溶液,请你帮助完成。 (1)甲图中缺少一种必须用到的玻璃仪器是_____(填写名称)作用是_____。 (2)准确称量18g氯化钠,量取蒸馏水的体积如乙图所示,氯化钠完全溶解后所配制的溶液中溶质的质量分数是_____(水的密度为1g/cm3)。如果量取水读数时仰视,溶质的质量分数会_____(填“偏大”或“偏小”)。 (3)配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、_____、装瓶并贴上标签。请你把丙图中试剂瓶上的标签填写完整_____。 |
|
| 28. 科学探究题 | 详细信息 |
国家环保总局已规定将各类实验室纳入环保监管范围。某中学九年级甲、乙两个班的同学分别做常见酸和碱与指示剂反应的实验,所做的实验和使用的试剂如图所示。实验后废液分别集中到各班的废液缸中,甲班废液呈红色,乙班废液呈蓝色。 (1)请你分析废液的成分:甲班废液含有_____;乙班废液中含有_____。 (2)目前许多高校、中学以及科研单位的化学实验室排放的各类废液大都未经严格处理便进入了下水道。甲班的废液若直接排入铁管下水道,会腐蚀下水道,你建议可用_____试剂来处理,原理:_____。(用化学方程式表示) |
|
| 29. 填空题 | 详细信息 | ||||||||||
|
小明同学做了下列四个实验:①在白色点滴板上加入少量的稀盐酸,然后滴入紫色的石蕊试液;②在白色点滴板上加入少量的氢氧化钠溶液,然后滴入紫色的石蕊试液;③在试管中放入一颗生锈的铁钉,然后加入适量的稀盐酸;④在试管中放入一颗生锈的铁钉,然后加入适量的氢氧化钠溶液。 小明记录了以下实验现象:a.溶液呈红色;b.没有任何现象;c.溶液呈蓝色;d.溶液呈黄色并伴有少量气泡产生。请你帮助小明完成实验报告: (1)将实验现象的序号(a、b、c、d)填在相应的表格内。
|
|||||||||||
| 30. 计算题 | 详细信息 |
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示。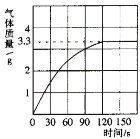 (1)从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是多少__________g。 (2)水垢中碳酸钙的质量分数是多少___________? |
|
最近更新



