2017届九年级上学期第一次模拟测试化学试卷(广东省广州市天河新蕾五星学校)
| 1. | 详细信息 |
|
下列过程中发生了化学变化的是 A. 石油分馏得到多种产品 B. 打开浓盐酸瓶盖,从瓶口涌出白雾 C. 铜片在酒精灯上加热变黑 D. 用干冰做制冷剂进行人工降雨 |
|
| 2. | 详细信息 |
|
下列实验能达到目的的是 A. 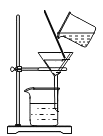 分离溶液中的NaCl和CuSO4 分离溶液中的NaCl和CuSO4B. 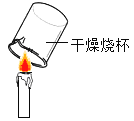 检验蜡烛燃烧生成的水 检验蜡烛燃烧生成的水C. 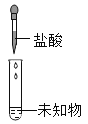 检验CO32- 的存在 检验CO32- 的存在D. 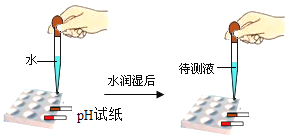 测溶液pH 测溶液pH |
|
| 3. | 详细信息 |
|
下列物质:①空气、②硫酸、③氧气、④硫酸钠、⑤水、⑥氢氧化钠、⑦天然气、⑧生铁、⑨碳酸钙,对其分类完全正确的一组是: A.混合物:①⑥⑦⑧ B.酸:②④ C.氧化物:③⑤ D.盐:④⑨ |
|
| 4. | 详细信息 |
|
空气是一种宝贵的资源,下列关于空气的用途不正确的是 A. 稀有气体可制成多种用途的光源 B. 氮气是制造硝酸和磷肥的重要原料 C. 氧气用于医疗急救 D. 二氧化碳可作气体肥料 |
|
| 5. | 详细信息 |
|
下列化学用语中,数字“2”的说法正确的是 ① 2H ② 2NH3 ③ SO2 ④ A. 表示分子中原子个数的是③⑦ B. 表示分子个数的是①② C. 表示离子个数的是⑤⑥ D. 表示离子所带电荷数的是④⑤ |
|
| 6. | 详细信息 |
|
下列事实与对应的解释相符合的是 A. 空气能被压缩 分子体积可以变小 B. 甘蔗甜,苦瓜苦 不同分子性质不同 C. 结冰的水不能流动 0℃以下,水分子不再运动 D. 50mL水和50mL酒精混合后的总体积小于l00mL 分子的质量和体积都很小 |
|
| 7. | 详细信息 |
|
水是地球上最普通、最常见的物质之一,下列关于水的说法正确的是 A. 水是所有溶液中的溶剂 B. 水蒸发后,水分子间的间隔增大 C. 水的蒸发和水的电解都生成气体,它们都是化学变化 D. 水电解生成氢气和氧气,说明水中含氢分子和氧分子 |
|
| 8. | 详细信息 |
|
下列关于碳和碳的氧化物的说法中,不正确的是 A. 将CO2通入CaCl2溶液中,有白色沉淀生成 B. 金刚石、石墨和C60都是碳元素的单质 C. 在一定条件下CO2能够转变成CO D. 将CO2通入紫色石蕊溶液中,可看到溶液变红 |
|
| 9. | 详细信息 |
|
物质的性质决定用途。下列有关说法正确的是 A. 稀有气体化学性质很不活泼,所以可制成多种电光源 B. 火碱具有碱性,故可用于改良酸性土壤 C. 一氧化碳具有还原性,故可用于治金工业 D. 高锰酸钾受热分解生成氧气,故工业上常用此方法制取氧气 |
|
| 10. | 详细信息 |
|
下列有关燃烧的说法不正确的是 A. 发生森林火灾要开辟隔离带,目的是清除可燃物 B. 白磷保存在冷水中目的是为了隔绝氧气 C. 将煤块制成蜂窝煤是为了使其燃烧更充分 D. 用水灭火目的是为了降低可燃物的着火点 |
|
| 11. | 详细信息 |
|
下列有关实验操作的“先”与“后”的说法中,正确的是 A. 制取气体时,先装药品,后检查装置的气密性 B. 用托盘天平称量10g固体药品时,先放砝码,后放药品 C. 用滴管取细口瓶内的液体时,先将其伸入液体内,后挤压取液 D. 加热KMnO4并用排水法收集O2的实验结束时,先熄灭酒精灯,后移出导管 |
|
| 12. | 详细信息 |
|
有关化学性质推断正确的是( ) A.两种物质相互反应生成盐和水,证明该反应是中和反应 B.在同一化合物中,金属元素一定显正价,非金属元素一定显负价 C.一定温度下,往氢氧化钙饱和溶液中加入氧化钙,溶质、溶剂的质量一定改变 D.某物质在空气中燃烧生成二氧化碳和水,证明该物质含碳、氢、氧三种元素 |
|
| 13. | 详细信息 |
X、Y是两种粒子的结构示意图,下列说法不正确的是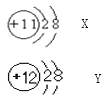 A. X、Y都是阳离子 B. Y粒子可表示为Y2+ C. X、Y属于不同种元素 D. X、Y都属于稀有气体元素 |
|
| 14. | 详细信息 |
|
下列各组物质分别加入足量水中,得到无色透明溶液的是 A.CuSO4? KCl? HCl B.Na2SO4? HCl? BaCl2 C.FeCl3 NaOH? NaCl D.Na2CO3? NaCl? Na2SO4 |
|
| 15. | 详细信息 |
|
近来,多种知名品牌白酒陷入塑化剂风波。邻苯二甲酸二丁酯是一种工业上常用的塑化剂,化学式为C16H22O4。则下列说法正确的是 A.C16H22O4的相对分子质量278g B.C16H22O4由C、H、O三个元素组成 C.C16H22O4中碳元素的质量分数为69.1% D.C16H22O4由16个碳原子、22个氢原子、4个氧原子构成 |
|
| 16. | 详细信息 |
如图所示,在小烧杯乙和丙中分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙。下列有关现象或结论的说法错误的是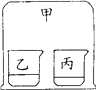 A. 乙:浓氨水 丙:紫色石蕊试液。 现象:丙中石蕊试液变蓝 B. 乙:浓盐酸 丙:无色酚酞试液。 现象:丙中酚酞试液不变色 C. 乙:浓硫酸 丙:硝酸钡溶液。? 现象:丙中产生白色沉淀 D. 乙:水 丙:浓硫酸。 结论:丙中溶质质量分数会减小 |
|
| 17. | 详细信息 |
已知反应前后分子变化的微观示意图如下所示,下列说法错误的是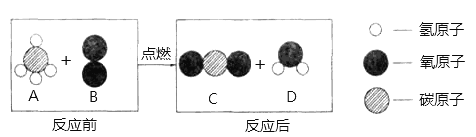 A. 反应前后元素种类不变 B. A是有机物,C、D是无机物 C. 点燃前要先检验A的纯度,防止爆炸 D. 此反应中A和B的化学计量数之比等于1:1 |
|
| 18. | 详细信息 |
现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的反应和转化关系。图中“?”表示两端物质间可发生化学反应,“→”表示物质间存在相应的转化关系。下列判断合理的是 A. X、Y、M两两间都可以发生复分解反应 B. X一定是碳酸钠溶液 C. Y可能是稀盐酸 D. N转化为铁的反应属于置换反应 |
|
| 19. | 详细信息 | ||||||||||||||||||||
除去下列物质中含有的杂质所选用试剂或操作方法不正确的一组是
|
|||||||||||||||||||||
| 20. | 详细信息 | ||||||||||||||||||||||
下列各组对比实验,能达到实验目的的是:
|
|||||||||||||||||||||||
| 21. | 详细信息 |
用下图装置分别进行下列实验,认识物质变化中的能量变化。 ①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______。写出生石灰与水反应的化学方程式_________________________。 ②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是________ (填标号)。 A. 氯化钠 B. 硝酸铵 C. 浓硫酸 D. 氢氧化钠 |
|
| 22. | 详细信息 | ||||||||||||||||
|
随着对“火”的认识和使用,人类能够更好地改造自然、改善生活。 (1)古人“钻木取火”过程中,快速搓动木棍使底部的干草着火。从“燃烧条件”分析:“钻木”为干草燃烧提供的条件是______________________; (2)某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。物质燃烧产生火焰的根本原因是什么? 【查阅资料】
|
|||||||||||||||||
| 23. | 详细信息 | ||||||||||||
下图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。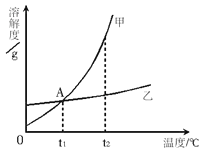 (1)A点的含义是_____________________________________。 (2)当甲中含有少量乙时,可采用__________________的方法提纯甲。 (3)小明说“t2℃时甲溶液的溶质质最分数一定大于乙溶液的溶质质量分数”,请判断该说法是否正确(填“正确”或“不正确)__________ , 其理由是_____________________________ 。 (4)t1℃时,100g水中溶解20g甲时溶液刚好达到饱和; 那么在t1℃时,向50g水中溶解_____g乙,溶液可以达到饱和。 (5)硫酸钠在不同温度下的溶解度如下表所示:
|
|||||||||||||
| 24. | 详细信息 |
|
金属材料在我国建设中起着重要的作用。 ⑴ 铜可以做导线,主要利用了金属铜的延展性和_______________。 ⑵ 回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下。  已知: Fe + Fe2(SO4) 3 == 3FeSO4 ① 过程Ⅰ中氧化铁发生反应的化学方程式是___________________________。 ② 过程Ⅱ、Ⅲ充分反应后,还应有的实验操作是_______。 ③ 过程Ⅲ的反应观察到的现象有___________________________________。 ④ A~F中含铁元素的有______________(填序号)。 ⑤ 若最后得到铜128克,则原工业废料中含氧化铜的质量是_____________。 |
|
最近更新