黄金30题系列 高二化学 大题好拿分
| 1. | 详细信息 |
|
化学反应原理对生产有重大的指导意义。回答下列问题: (1)有两个温度相同的密闭容器A和B,容器A保持容积不变,容器B保持压强不变,起始时向容积相等的A、B中分别充入等量的C(碳)和H2O(g),发生反应:C(s)+H2O(g) ①H2O的体积分数:V(A)%_____V(B)%。(填“>”、“<” “=”) ②达到平衡后,在两容器中分别通入等量的氦气,则A中H2O的转化率_______(填“ 增大” “减小”、“不变”);B中化学平衡_________移动(填“不”“向正反应方向”“向逆反应方向”)。 (2)某温度下,测得0.01mol?L-1 NaOH溶液的pH=10,则在该温度下Kw=______;在此温度下,将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得溶液为中性,则a:b=_______(假设混合时体积不变)。 |
|
| 2. | 详细信息 |
|
沉淀的生成、溶解和转化在无机物制备和提纯以及科研等领域有广泛应用。 Ⅰ.汽车尾气中的SO2可用石灰水来吸收,生成CaSO3浊液。已知常温下Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9 常温下测得某纯CaSO3与水形成的浊液pH=9,忽略SO32-的第二步水解,则Ksp(CaSO3)=__________ 。CaSO3易变质为CaSO4,水垢中含有较多的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。CaSO4转化为CaCO3的离子方程式为:_________; Ⅱ.已知25℃时,NH3?H2O电离常数Kb=1.8×10-5,Ksp[Mg(OH)2]=1.0×10-11,向0.4mol/L的氨水中加入等体积浓度为6×10-4mol/L MgCl2 溶液,________沉淀生成(填“无”或“有”),并简述理由______ ;若某溶液中C(Mg2+)=1.2×10-3mol/L,需向其中加入等体积的NaOH溶液浓度为_____ mol/L时,可使Mg2+恰好沉淀完全(忽略溶液体积变化)。 Ⅲ.工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为: CrO42- 其中第①步存在平衡:2CrO42-(黄色)+2H+ ①若平衡体系的pH=2,则溶液显____________色。 ②能说明第①步反应达平衡状态的是_____________。 A.Cr2O72-和CrO42-的浓度相同 B.2v (Cr2O72-) =v (CrO42-) C.溶液的颜色不变 ③第②步中,还原1mol Cr2O72-离子,需要________mol的FeSO4?7H2O。 ④第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) |
|
| 3. | 详细信息 | ||||||||||
已知25℃、101kPa时,一些物质的燃烧热为,回答下列问题:
|
|||||||||||
| 4. | 详细信息 |
下图一所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液,足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。 (1)图一中的直流电源为一种性能优良的Al-Ag2O电池,其原理如图二所示。该电池中铝是负极,试写出电池工作时的正极反应式__________________和电池的总化学反应方程式______________。 (2)接通电源后,经过一段时间后,测得丙中K2SO4质量分数为10.47%,乙中c电极质量增加。据此回答问题: ①电源的N端为_______极;c电极上发生______反应(“氧化”或“还原”); ②电极b上发生的电极反应为___________________; ③列式计算电极b上生产的气体在标准状况下的体积_______; ④电极c的质量变化是_____g; ⑤电解前后各溶液的pH是否发生变化(“增大”、“减小”或“不变”) 甲溶液_________;乙溶液_________;丙溶液______________。 |
|
| 5. | 详细信息 |
|
(1)为除去CuSO4溶液中少量的Fe3+杂质,可加入某物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3而除去,调整溶液pH可选用下列物质中的________。 A. NaOH B. Cu C. Cu(OH)2 D. NH3?H2O (2)在恒温、恒容条件下,将1molA和2molB充入一个密闭容器中,在一定条件下发生反应:A(g)+2B(g) (3)25℃时,物质的量浓度相同的下列六种溶液:①NH3?H2O? ②NH4HSO4? ③(NH4)2CO3 ④NH4Cl? ⑤NH4Al(SO4)2? ⑥(NH4)2SO4 ,其中c(NH4+)从大到小的排列顺序为______________(填序号)。 (4)已知下列四组溶液中:①Na2S? ② H2S 和NaHS ③H2S? ④NaHS ,每种溶质的物质的量浓度均为0.4 mol?L-1,回答下列问题: c(H2S)从大到小的顺序为____________________________(填序号) c(S2-)从大到小的顺序为_____________________________(填序号) |
|
| 6. | 详细信息 | ||||||||||||||||
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
|||||||||||||||||
| 7. | 详细信息 |
已知:①25 ℃时,弱电解质的电离平衡常数:K(CH3COOH)=1.8×10-5,K(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=6×10-10。②25 ℃时,2.0×10-3 mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:  请根据以上信息回答下列问题: (1)25 ℃时,将20 mL 0.10 mol/L CH3COOH溶液和20 mL 0.10 mol/L HSCN溶液分别与20 mL 0.10 mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是__________,反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)。 (2)25 ℃时,HF电离平衡常数的数值Ka≈______。 (3)4.0×10-3 mol/L HF溶液与4.0×10-4mol/L CaCl2溶液等体积混合,调节混合液pH为4.0后(忽略调节时混合液体积的变化),_______沉淀产生。(填“有”或“无”)。 |
|
| 8. | 详细信息 | |||||||||||||||
蛋壳的主要成分是CaCO3,含有少量的SiO2、MgCO3及色素等杂质,测定蛋壳中钙含量的操作步骤如图所示: 已知:CaC2O4、MgC2O4都难溶于水。 回答下列问题: (1)样品溶于盐酸后得到的滤渣主要是________________________________。 (2)①②操作时,加入饱和(NH4)2C2O4溶液和氨水的作用是_______________________。 (3)洗涤最好选用_____(填“冰水”或“0. lmol/L草酸铵溶液”),其目的是____________________。 (4)在一定温度下,向2L的密闭容器中放入足量的草酸钙(固体所占体积忽略不计)发生反应: CaC204(s) (5)滴定操作是用标准酸性高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,可间接求出钙的含量。 步骤1:将溶液A加蒸馏水稀释至250mL。 步骤2:取稀释后的溶液25.00mL于锥形瓶中,加稀H2SO4酸化。 步骤3:用0.0190 mol?L-1KMnO4溶液滴定步骤2所得溶液至终点,消?KMnO4溶液V1mL。 步骤4:重复步骤2、步骤3的操作3次,记录数据如下表:
|
||||||||||||||||
| 9. | 详细信息 | ||||||||||
|
在T℃时,发生反应C(s)+H2O(g) (1)T℃时,在一个2L的密闭容器中加入4molC和1molH2O(g),5min后反应达到平衡,C的转化率为20%。 ①0~5min内,用H2O(g)表示的平均反应速率为____________。 ②该反应达到平衡的标志是______。 a.气体的平均相对分子质量不变 b.气体的密度不变 c.H2O(g)、CO(g)、H2(g)的物质的量之比为1:1: 1 d.气体的总物质的量不变 (2)T℃时,在下列密闭容器中加入相应的物质进行实验,中间的隔板可以自由滑动。  ①若左室中气体的平均相对分子质量一直保持不变,则反应开始前H2O(g)、H2(g)的物质的量之比是__________。 ②反应在达到平衡时,中间的隔板所处的位置是________。 a.1~1.5之间 b.1.5处 c.1.5~2之间 (3)已知: I.破坏1mol 共价键所需要的能量如下表:
|
|||||||||||
| 10. | 详细信息 |
氨气有广泛用途,工业上利用反应N2(g)+3H2(g)  (1)某小组为了探究外界条件对反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。 ①a条件下,0~t0的平均反应速率v(N2)=___________mol?L-1?min-1。 ②相对a而言,b可能改变的条件是______________________________。 ③在a条件下t1时刻将容器体积压缩至原来的1/2,t2时刻重新建立平衡状态。请在答题卡相应位置画出t1~t2时刻c(H2)的变化曲线________。  (2)某小组往一恒温恒压容器充入9 mol N2和23 mol H2模拟合成氨反应,图B为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。 ① 此时N2的平衡分压为__________MPa,H2的平衡分压为___________MPa。(分压=总压×物质的量分数) ② 列式计算此时的平衡常数Kp=____。(用平衡分压代替平衡浓度计算,结果保留2位有效数字) (3)分离器中的过程对整个工业合成氨的意义是_____________________。 |
|
| 11. | 详细信息 |
工业上用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2,在500℃下发生发应,CO2(g)+3H2(g) (1)从反应开始到平衡,氢气的平均反应速率v(H2)= ______ 。图2是改变温度时化学反应速率随时间变化的示意图,则该反应的正反应为 _____ 反应(填“放热”或“吸热”)。 (2)下列各项能作为判断该反应达到平衡标志的是____(填序号字母)。 A.容器内压强保持不变 B.v正(CO2)=3v逆(H2) C.容器内CO2的体积分数不变 D.混合气体的密度保持不变 (3)500℃该反应的平衡常数为 ______ (保留两位小数),若提高温度到 800℃进行,达平衡时,K值 ______ (填“增大”“减小”或“不变”). (4)下列措施中不能使CO2的转化率增大的是 ______ 。 A.在原容器中再充入1mol H2 B.在原容器中再充入1molCO2 C.缩小容器的容积 D.使用更有效的催化剂? E.将水蒸气从体系中分离 (5)500℃,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。 (6)下列措施能使n(CH3OH)/n(CO2)增大的是 ______ 。 A.升高温度 B.在原容器中充入1molHe C.将水蒸气从体系中分离出 D.缩小容器容积,增大压强 |
|
| 12. | 详细信息 |
|
氢气是一种新型的绿色能源,又是一种重要的化工原料。以生物材质(以C计)与水蒸气反应制取H2是一种低耗能,高效率的制H2方法。该方法由气化炉制造H2和燃烧炉再生CaO两步构成。气化炉中涉及的反应有: Ⅰ.C(s)+H2O(g) Ⅱ.CO(g)+H2O(g) Ⅲ.CaO(s)+CO2(g) 燃烧炉中涉及的反应为 Ⅳ.C(s)+O2(g)===CO2; Ⅴ.CaCO3(s)===CaO(s)+CO2(g)。 (1)该工艺制H2总反应可表示为C(s)+2H2O(g)+CaO(s) (2)在一容积可变的密闭容器中进行反应Ⅰ,恒温恒压条件下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),达到平衡时,容器的体积变为原来的1.25倍,平衡时水蒸气的平衡转化率为________;向该容器中补充a mol炭,水蒸气的转化率将________(填“增大”、“减小”或“不变”),再补充a mol水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为__________。 (3)已知反应Ⅱ的ΔH=-41.1 kJ/mol,C≡O 、O?H、H?H键的键能分别为1072.9 kJ/mol,464 kJ/mol、436 kJ/mol,则C=O的键能为________ kJ/mol。 (4)对于反应Ⅲ,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡________移动(填“向右”、“向左”或“不”);当重新平衡后,CO2浓度________(填“变大”、“变小”或“不变”)。 |
|
| 13. | 详细信息 |
|
已知:乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;碳酸(H2CO3)的电离平衡常数为K1=4.5×10-7,K2=4.7×10-11。草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题: (1)写出水溶液中草酸的电离方程式_____________________________________ 。 (2)相同条件下物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH比Na2CO3溶液的pH______________? (填“大”、“小”或“相等”) 。 (3)常温下将0.4mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中阴离子浓度的大小顺序为_____________________________________ 。 (4)往Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为________________。 (5)25℃时,向20mL碳酸钙的饱和溶液中逐滴加入c mol/L的草酸钾溶液20mL后,有草酸钙沉淀生成,则c的最小值为__________________________。 |
|
| 14. | 详细信息 |
某课外活动小组用如图装置进行实验,试回答下列问题: (1)若开始时开关K与a连接,则B极的电极反应为____________________。 (2)若开始时开关K与b连接,则B极的电极反应为____________________,总反应的离子方程式为____________________。 (3)有关上述实验,下列说法正确的是______。 A.溶液中Na+向A极移动 B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝 C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子 (4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。 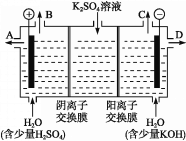 ①该电解槽的阳极反应为______________。 此时通过阴离子交换膜的离子数_____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。 ②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________导出。 ③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因__________________________。 |
|
| 15. | 详细信息 |
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4?H2O):CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl。 实验一:制备NaClO溶液(实验装置如图1所示) (1)锥形瓶中发生反应的离子方程式是________________________________________________。 实验二:制取水合肼.(实验装置如图2所示) 已知水合肼具有还原性,被氧化生成氮气。 控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。 (2)分液漏斗中的溶液是______(填标号). A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液 选择的理由是____________________________________________________。 实验三:测定馏分中水合肼的质量分数。采用下列步骤: a.称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液。 b.移取25.00mL溶液于锥形瓶中,加入10 mL水,摇匀。 c.用0.2000 mol?L-1的I2溶液滴定,至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右,记录消耗碘的标准溶液的体积。 d.进一步操作与数据处理。 (3)水合肼与碘溶液反应的化学方程式为:_______________________; (4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_______________。 (5)滴定时,碘的标准溶液盛放在___________(填“酸式”或“碱式”)滴定管中;若三次滴定消耗碘的标准溶液的平均体积为18.00 mL,则馏分中水合肼(N2H4?H2O)的质量分数为____________________(保留三位有效数字)。 |
|
| 16. | 详细信息 | ||||||||||||||||||||||||||
H2O2是一种常见试剂,在实验室、工业生产上有广泛用途 Ⅰ.实验室用H2O2快速制氧,其分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如甲乙丙丁四图所示: (1)下列说法正确的是:________(填字母序号) A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越慢 B.图乙表明,其他条件相同时,溶液碱性越弱,H2O2分解速率越快 C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快 D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 (2)催化剂Mn2+在反应中,改变了____________________ (填字母序号) A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数 Ⅱ. H2O2在工业上作为Fenton法主要试剂,常用于处理含难降解有机物的工业废水。在调节好pH(溶液的酸碱性)和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。 【实验设计】控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验,并将实验结果绘制时间-p-CP浓度图如下。  (3)电中性的羟基自由基的电子式为:______________ (4)请完成以下实验设计表(表中不要留空格)。
|
|||||||||||||||||||||||||||
| 17. | 详细信息 |
|
硫酰氯(SO2Cl2) 和亚硫酰氯(SOCl2) 均是重要的化工试剂,遇水发生剧烈反应,常用作脱水剂。 已知:①SO2Cl2 (g) ②SO2(g) +Cl2(g) +SCl2(g) (1)反应2SOCl2(g) (2)若在绝热、恒容的密闭容器中,投入一定量的SO2Cl2(g)和SCl2(g),发生反应SO2Cl2(g)+SCl2(g)  (3)为研究不同条件对反应①的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molSO2Cl2,10min后反应①达到平衡。测得10min内v(SO2)= 8.0×10-3mo1?L-1?min-1,则平衡时SO2Cl2的转化率α1=_______。若其它条件保持不变,反应①在恒压条件下进行,平衡时SO2Cl2的转化率α2_____α1(填“>”、“<”或“=”)。若要增大SO2Cl2的转化率,可以采取的措施有______(列举一种)。 (4)锂亚硫酰氯(Li/SOCl2) 电池是一种大容量电池,该电池用锂与石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4) 溶解在亚硫酰?(SOCl2)中形成的,其电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S。 ①写出电池工作时正极的电极反应式_____________; ②若用此电池做电源,以铂作电极电解200mL 0.2mol.L-1CuSO4溶液,当两极各产生标准状况下896mL的气体时,电池负极消耗锂的质量是______g。 |
|
| 18. | 详细信息 |
|
科学家积极探索新技术对CO2进行综合利用。 Ⅰ.CO2可用来合成低碳烯烃:2CO2(g)+6H2(g) 请回答: (1)已知:H2和CH2=CH的燃烧热分别是285.8kJ/mol和1411.0kJ/mol,且H2O(g) (2)上述由CO2合成CH2=CH2的反应在________下自发进行(填“高温”或“低温”)。 (3)在体积为1L的恒容密闭容器中,充入3molH2和1molCO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示。下列说法正确的是________。 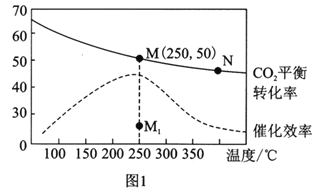 A.平衡常数大小:KMN B.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于点M1 C.图1中M点时,乙烯的体积分数为7.7% D.当压强或n(H2)/n(CO2)不变时均可证明化学反应已达到平衡状态 (4)保持温度不变,在体积为V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反应物,t0时达到化学平衡。请在图2中作出容器内混合气体的平均相对分子质量 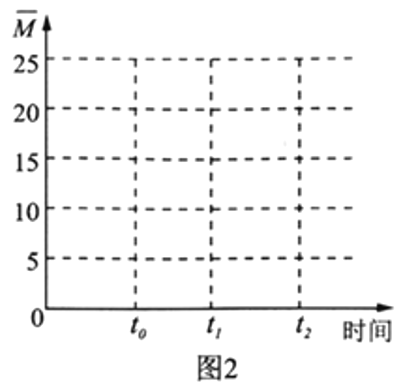 Ⅱ.利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2  (5)放电时,正极的电极反应式为__________________。 (6)若生成的Na2CO3和C全部沉积在正极表面,当转移0.2mole-时,正极增加的质量为_______g。 (7)选用高氯酸钠四甘醇二甲醚做电解液的优点是_____________________。 |
|





