2018届九年级上半期期中考试化学试卷带参考答案和解析(江苏省苏州市景城中学)
| 1. | 详细信息 |
下列食品、调味品的制作过程中,主要发生物理变化的是 A.水果榨果汁 B.黄豆酿酱油 C.糯米酿甜酒 D.鲜奶制酸奶 |
|
| 2. | 详细信息 |
|
人体中化学元素含量的多少会直接影响人体健康.下列说法不正确的是( ) A. 食用加铁酱油防止贫血 B. 缺锌会使儿童发育停滞智力低下 C. 缺碘和碘过量均会导致甲状腺疾病 D. 人体补充的钙、吸收的钙越多越好 |
|
| 3. | 详细信息 |
|
下列有关氧气的说法正确的是( ) A. 因为氧气能支持燃烧,所以可用作燃料 B. 氧气化学性质比较活泼,能与许多物质发生氧化反应 C. 空气中的氧气来源于绿色植物的呼吸作用 D. 氧气只有点燃条件下才能与其他物质发生化学反应 |
|
| 4. | 详细信息 |
|
下列有关二氧化碳的说法错误的是( ) A. 二氧化碳能溶于水,所以二氧化碳气体不能用排水法收集 B. 二氧化碳是能加快绿色植物光合作用,可用作温室气体肥料 C. 液态二氧化碳用于灭火,利用了CO2不助燃、不可燃、密度大于空气的性质 D. 干冰气化时要吸收大量的热,可用作制冷剂 |
|
| 5. | 详细信息 |
|
下列实验操作或说法中,不正确的是( ) A. 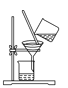 用于分离二氧化锰和水 用于分离二氧化锰和水B.  说明该装置气密性良好 说明该装置气密性良好C.  滴管用毕插回 滴管用毕插回D.  用于做反应容器 用于做反应容器 |
|
| 6. | 详细信息 |
|
下列说法正确的是( ) A. O2、CO2、SO2三种物质中,都含有氧分子 B. 相对原子质量就是原子的实际质量 C. 分子和原子的质量都很小,分子质量大于原子质量 D. 由分子构成的物质发生化学变化时,分子发生改变 |
|
| 7. | 详细信息 |
|
水是生命之源,下列有关水的说法正确的是( ) A. 水中加入明矾能杀菌消毒 B. 为了加快过滤速率,可用玻璃棒搅拌浊液 C. 生活中通过煮沸的方法可以降低水的硬度 D. 将长江水过滤可以除去水中所有的杂质 |
|
| 8. | 详细信息 |
|
下列物质名称对应的化学式正确的是 A.氧化镁 MgO2 B.氢氧化钠 NaOH C.氯化锌 ZnCl D.碳酸钠 NaCO3 |
|
| 9. | 详细信息 |
|
下列叙述正确的是 A. 不同元素的根本区别在于其相对原子质量的不同 B. 元素化学性质与其原子的最外层电子数目关系非常密切 C. 一种元素只能组成一种单质 D. 含氧元素的化合物一定是氧化物 |
|
| 10. | 详细信息 |
|
用微粒的相关知识解释下列生活中的现象,不正确的是 A.墙内开花墙外香——微粒在不断运动 B.热胀冷缩——微粒的大小随温度的升降而改变 C.10mL酒精与10mL水混合后,体积小于20mL——微粒间有间隔 D.湿衣服在阳光下容易晾干——微粒的运动速率随温度升高而加快 |
|
| 11. | 详细信息 |
|
下列说法中,正确的是( ) A. 在空气中不燃烧的物质,在氧气里也一定不燃烧 B. 使用催化剂可使双氧水分解出比理论值更多的氧气 C. 只有使用二氧化锰才能催化双氧水分解放出氧气 D. 食物的腐败是缓慢氧化的结果 |
|
| 12. | 详细信息 |
|
下列一些实验现象的描述正确的是( ) A. 镁条在空气中燃烧,发出耀眼的白光,生成白色的固体 B. 硫在氧气中燃烧,发出淡蓝色的火焰 C. 碳在氧气中燃烧发出白光,产生黑色气体 D. 铁丝在氧气中燃烧,火星四射,生成黑色的四氧化三铁 |
|
| 13. | 详细信息 |
|
括号内是区别下列各组常见物质的方法,其中错误的是( ) A. 面粉和食盐(加水,振荡) B. 硬水与软水(加肥皂水,振荡) C. 蒸馏水与食盐水(过滤) D. 白酒和食醋(闻气味) |
|
| 14. | 详细信息 |
|
下列对实验过程中出现的问题的处理方法不正确的是 A. 添加液体时,倒入的液体过多可将多余的液体倒回原试剂瓶 B. 实验中不慎打翻酒精灯,可用湿抹布盖灭 C. 用火柴梗迅速平放蜡烛火焰中,约1S后取出,比较火焰各层温度 D. 用高锰酸钾制取氧气并用排水法收集后出现倒吸现象,可立刻松开试管上的橡皮塞 |
|
| 15. | 详细信息 |
右图装置常用来测定空气中氧气的含量。下列对该实验的认识中正确的是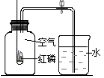 A. 红磷燃烧产生大量白色烟雾 B. 燃烧匙中的红磷可以换成细铁丝 C. 该实验可说明N2难溶于水 D. 红磷的量不足会导致进入集气瓶中水的体积大于1/5 |
|
| 16. | 详细信息 |
|
下列计算正确的是( ) A. 在Cl-中,质子数为17,电子数为17 B. Mr[CO(NH2)2]=12+16+14+2×2 C. 化工颜料普鲁士蓝Fe4[Fe(CN)6]中,Fe、C、N三原子个数比为5∶6∶6 D. 抗癌药物顺铂[Pt(NH3)2Cl2]中,氢元素和氯元素质量比为3∶71 |
|
| 17. | 详细信息 |
|
下列化学符号中数字“2”的意义正确的是( ) A. 3H2O:3个水分子中共含有2个氢原子 B. O2-:1个氧离子带2个单位负电荷 C. 2O:2个氧元素 D. MgO:氧化镁的化合价为-2价 |
|
| 18. | 详细信息 |
如图是实验室加热高锰酸钾制取氧气的装置图,下列有关实验操作的分析错误的是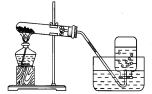 A.连接装置:先检查装置气密性,再加药品;先放酒精灯,再固定试管 B.试管口略向下倾斜:防止水倒流入试管底部,导致试管炸裂 C.收集:加热前将导管伸入装满水的集气瓶口 D.停止加热:先把导管移出水面,再熄灭酒精灯 |
|
| 19. | 详细信息 |
虾青素(C40H52O4)是从河虾外壳,牡蛎,藻类中发现的一种红色类胡萝卜素,如下图,是一种高效的纯天然抗氧化剂(能与氧气反应),最主要的功能是清除自由基,提高人体抗衰老能力。下列有关它的说法正确的是 A.虾青素长期露置在空气中会与氧气反应而变质 B.虾青素中碳、氢、氧元素质量比为40∶52∶4 C.虾青素中共含有96个原子 D.虾青素属于氧化物 |
|
| 20. | 详细信息 |
|
下列CO2的制备装置,不能控制反应的发生和停止的是( ) A. 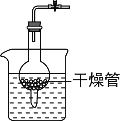 B. B. 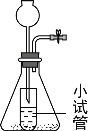 C.  D. D.  |
|
| 21. | 详细信息 |
|
请用化学符号填空: (1)2个硫原子________; (2)2个铵根离子________; (3)氧化铁________; (4)氧化钙中钙元素显+2价________。 |
|
| 22. | 详细信息 |
|
用下列物质的序号填空 (1)①高锰酸钾②石灰水③液氧④四氧化三铁⑤清新的空气⑥碱式碳酸铜⑦水银⑧冰水共存物⑨氧化铜⑩五氧化二磷 其中属于混合物的是___,属于单质的是___,属于氧化物的是___,含有氧分子________。 (2)如图所示,用○表示氧原子,用●表示氢原子,请按要求回答下列问题。  ①图A表示的一个分子由________个原子构成; ②图________可以用来表示水这种物质; ③图________表示的物质是混合物。(填字母) |
|
| 23. | 详细信息 |
|
写出下列反应的符号表达式,并回答有关问题。 (1)实验室用双氧水和少量二氧化锰混合物制取氧气:________,其中二氧化锰的作用是________。 (2)加热碱式碳酸铜固体:________,固体的颜色变化为________。 (3)碳酸氢铵常温下易分解:________,该反应属于________反应(填基本反应类型)。 (4)镁条在空气中燃烧,________,燃烧的镁条应用________夹持置于石棉网上。 (5)盛放石灰水的试剂瓶上会形成一层白膜:________,该白膜最方便的除去方法是先加入________浸泡再用清水冲洗。 |
|
| 24. | 详细信息 |
10月4日中秋夜,一颗流星体划破了云南西北的夜空.图1是某陨石样品中各种元素含量的比例图: (1)该陨石中含________种非金属元素; (2)钠离子的结构示意图如图2,则X=________; (3)此陨石样品中不可能含有的化合物是________。 A.CaCO3 B.K2SO4 C.Al2O3 D.SiO2 |
|
| 25. | 详细信息 |
请你根据所学知识并结合下图所示装置回答有关问题:(提示:F中盛放的液体是浓硫酸,浓硫酸具有强吸水性,能用来除去某些气体中的水蒸气。) (1)指出标号仪器的名称:①________;②________。 (2)用高锰酸钾制取氧气的符号表达式为________,应选择的发生装置是________,可以用E装置收集氧气的原因是________,当观察到________现象时,说明氧气已收满,集满氧气的集气瓶应________(填“正”或“倒”)放在桌面上。 (3)某老师带领学生进行上述实验时,发现一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃;于是,老师让该同学重新做实验;先往集气瓶中装入半瓶水,再用排水法收集1/2集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃。  ①用下列方案收集“1/2集气瓶的氧气”,其中最合理的是________(填字母)。 ②空气中氧气的体积分数约为21%,本实验中,该同学收集的氧气约占总体积的________%(保留1位小数),所以用“使带火星的木条复燃”来检验集气瓶中充满氧气的方法并不能保证收集到的氧气很纯净。 (4)实验室制取并收集一定量的二氧化碳,应选择的发生装置是________,写出反应的符号表达式为________,如果用F装置干燥二氧化碳,气体应该从________导管(填“左”或“右”)进入。 (5)用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是________,H中喷有紫色石蕊溶液的纸花显________色,写出纸花变色的反应符号表达式________。 |
|
| 26. | 详细信息 |
|
每年的3月22日是“世界水日”,中国水周主题是“节约保护水资源,大力建设生态文明用所学知识回答下列问题。 (一)生活中的水. (资料在线)我国生活饮用水的标准(摘录部分)。 感官指标:水质无色无味且澄清透明。 化学指标:pH6.5~8.5;总硬度<250mg/L(以碳酸钙计);铜<1.0mg/L,铝<0.2mg/L。 细菌学指标:细菌总数<100个/mL等. (1)自来水厂用过滤的方法使水澄清透明,再用一种物质来吸附色素和异味,从而达到感官指标.而化学指标中的铜、铝等指的是________(选填“原子”或“元素”)。 (2)漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。试计算: ①Ca(ClO)2中钙:氯:氧元素的质量比________; ②143gCa(ClO)2中钙元素的质量是________。 (二)探究水的组成 某校化学兴趣小组想亲自感受科学家的探究历程,他们选择了“水的组成粗略测定”为探究内容。 (查阅资料) 水难导电,在水中可加入少量氢氧化钠可以增强导电性。 (进行试验)如图装置进行实验并记录数据。  (实验分析)两个电极附近产生很多气泡,a管内气泡产生较b管快,小组成员用燃着的木条分别在两个玻璃尖嘴导管口检验产生的气体,观察到:放在b端管口燃着的木条________。分析得出:水通电的符号表达式为________,进而推出水是由________组成的。 (定量研究)小组经过多次试验后发现:氢气和氧气的体积比几乎都是2∶1。同学们还想进一步认识水的组成.查阅资料:氢气的密度是0.09g/L,氧气的密度是1.43g/L。同学们经过计算得出水中氢元素与氧元素的质量比为:________。 |
|
| 27. | 详细信息 |
|
在现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用。如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明。 碘盐 配料:氯化钠、碘酸钾(KIO3) 含碘量:(20~30)mg/kg 保质期:18个月 食用方法:勿长时间炖炒 贮藏指南:避光、避热、密封防潮 碘盐 配料:氯化钠、碘酸钾(KIO3) 含碘量:(20~30)mg/kg 保质期:18个月 食用方法:勿长时间炖炒 贮藏指南:避光、避热、密封防潮 请回答下列问题: (1)碘酸钾的相对分子质量________; (2)碘酸钾(KIO3)中碘元素的化合价为________; (3)碘酸钾中,碘元素的质量分数是________;(写出计算过程,计算结果精确到0.1%) (4)若成人每天摄入5g这样的“碘盐”,在5g这样的“碘盐”中至少需要加入________mg碘酸钾。(写出计算过程,计算结果精确到0.01) |
|
最近更新



