2017-2018年高二上半期期中考试化学考卷带参考答案和解析(内蒙古巴彦淖尔市第一中学)
| 1. | 详细信息 |
|
已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+ 根据以上热化学方程式判断,下列说法正确的是 A. CO的燃烧热为283 kJ B. 如图可表示由CO生成CO2的反应过程和能量关系 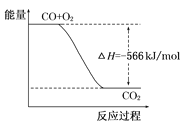 C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
|
| 2. | 详细信息 |
|
已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ /mol;HCl(aq)与NaOH(aq)反应的△H =-55.6kJ/ mol。则HCN在水溶液中电离的ΔH等于 A. -67.7 kJ /mol B. -43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol |
|
| 3. | 详细信息 |
|
下列说法正确的是( ) A. 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 B. 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 C. 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 D. 催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
|
| 4. | 详细信息 |
|
α1和α2分别为A、B在两个恒容容器中平衡体系A(g) A. α1、α2均减小 B. α1、α2均增大 C. α1减小,α2增大 D. α1增大,α2减小 |
|
| 5. | 详细信息 |
|
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是(? ) A. 该溶液的pH=4 B. 升高温度,溶液的pH和电离平衡常数均减小 C. 此酸的电离平衡常数约为1×10-7 D. 加入少量纯HA,电离程度减小电离平衡常数不变 |
|
| 6. | 详细信息 |
|
下列事实不能证明CH3COOH是弱酸的是( ) A. CH3COOH溶液能使石蕊试液变红 B. 0.1 mol/L的CH3COOH,H+浓度为0.01 mol/L C. 等物质的量浓度的CH3COOH导电能力比盐酸弱 D. 0.01 mol/L的CH3COOH溶液中有两种分子存在 |
|
| 7. | 详细信息 |
|
已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( ) A. 该温度高于25℃ B. 由水电离出来的H+的浓度是1.0×10-10mol?L-1 C. NaHSO4晶体的加入抑制了水的电离 D. 该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性 |
|
| 8. | 详细信息 | ||||||||||||||||||||
|
乙醇是重要的化工原料和液体燃料,可以利用下列反应制取乙醇:2CO2(g) + 6H2(g) (1)写出该反应的平衡常数表达式:K=_________________________。 (2)请说明以CO2为原料合成乙醇的优点是_____________________(只要求写出一条)。 (3)在一定压强下,测得该反应的实验数据如下表:
|
|||||||||||||||||||||
| 9. | 详细信息 |
在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答: (1)写出醋酸的电离方程式___________________________________________。 (2)a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。 (3)a、b、c三点中醋酸的电离程度最大的是_________。 (4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:c(H+)甲_____ 10c(H+)乙(填“大于”、“小于”或 “等于”) |
|
最近更新




