2019届高三9月月考化学题开卷有益(山西省朔州市应县第一中学)
| 1. | 详细信息 | ||||||||||||
中华文化源远流长、博大精深。从化学的视角看,下列理解不正确的是( )
|
|||||||||||||
| 2. | 详细信息 |
|
已知氧化还原反应: 2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O。则有关该反应的说法正确的是( ) A. 当1molCu(IO3)2发生反应共转移的电子为10mol B. 反应中KI被氧化 C. I2是氧化产物CuI是还原产物 D. 当1molCu(IO3)2发生反应被Cu2+氧化的I—为2mol |
|
| 3. | 详细信息 |
|
下列关于阿伏伽德罗常数说法正确的是( ) A. 20gH218O和20gTHO中含有的中子数均为10NA B. 25℃时,pH=2的CH3COOH溶液中水电离出的OH-的数目为10-12NA C. 标况下,22.4L HF含HF分子数目为NA D. 3.4gH2O2参加氧化还原反应时转移电子数为0.1 NA |
|
| 4. | 详细信息 | |||||||||||||||
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如图,符合图中情况的一组物质是( ) 
|
||||||||||||||||
| 5. | 详细信息 |
|
Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx 与NaClO的物质的量之比为1:16,则x的值是 ( ) A. 2 B. 3 C. 4 D. 5 |
|
| 6. | 详细信息 |
|
下列离子方程式书写正确是( ) A. 1mol•L﹣1的NaAlO2溶液和2.5mol•L﹣1的HCl溶液等体积互相均匀混合:2AlO2﹣+5H+═Al3++Al(OH)3↓+H2O B. 向Mg(HC03)2溶液中加入足量澄清石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O C. 已知:酸性Ka1(H2SO3)>Ka2(H2SO3)>Ka(HClO),过量SO2通入到NaClO溶液中:SO2+H2O+ClO﹣═HClO+HSO3﹣ D. 向Fe(OH)2中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
|
| 7. | 详细信息 |
|
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关说法正确的是 A. NF3是氧化剂,H2O是还原剂 B. 还原剂与氧化剂的物质的量之比为2∶1 C. 若生成0.2 mol HNO3,则转移0.2 mol电子 D. NF3在潮湿的空气中泄漏会产生红棕色气体 |
|
| 8. | 详细信息 |
|
对于某酸性溶液(可能含有Br–、SO42 –、H2SO3、NH4+),分别进行如下实验: ①加热时放出的气体可使品红溶液褪色;②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略呈橙红色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀。对于下列物质不能确定其在原溶液中是否存在的是 A. Br– B. SO42– C. H2SO3 D. NH4+ |
|
| 9. | 详细信息 |
|
在复杂的体系中,确认化学反应先后顺序有利于解决问题。下列化学反应先后顺序判断正确的是( ) A. 在含有等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:OH-、CO32-、 AlO2- B. 在含等物质的量的FeBr2、FeI2溶液中,缓慢通人氯气:I-、Fe2+、 Br- C. 在含等物质的量的KOH、Ba(OH)2溶液中,缓慢通入CO2: KOH、Ba(OH)2、K2CO3、BaCO3 D. 在含等物质的量的Fe3+、Cu2+、H+溶液中加入锌粉:Cu2+、Fe3+、H+ |
|
| 10. | 详细信息 |
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )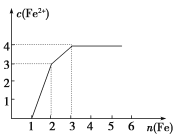 A. 1∶1∶1 B. 1∶3∶1 C. 3∶3∶8 D. 1∶1∶4 |
|
| 11. | 详细信息 |
|
下列各组离子在指定溶液中能大量共存的是( ) ①无色溶液中K+、Na+、MnO4-、SO42- ②pH=1的溶液CO32 -、Na+、AlO2-、NO3- ③加入Al能放出H2的溶液中Cl-、HCO3-、SO42-、NH4+ ④由水电离的C(OH-)= 10-13 mol/L的溶液中,Na+、Ba2+、Cl-、Br- ⑤有较多的Fe3+的溶液中,Na+、NH4+、SCN-、HCO3- ⑥酸性溶液中Fe3+、Al3+、NO3-、I-、Cl- A. ④ B. ③⑥ C. ①② D. ③⑤ |
|
| 12. | 详细信息 |
|
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( ) A. 2.24LCO2中含有的原子数为0.3×6.02×1023 B. 0.1L 3mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 C. 4.5g SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023 D. 5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023 |
|
| 13. | 详细信息 |
|
将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100 mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度约为( ) A. 0.011 mol/L B. 0.22 mol/L C. 0.022 mol/L D. 0.11 mol/L |
|
| 14. | 详细信息 |
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化,则X为( ) A. Fe B. Cu C. S D. C |
|
| 15. | 详细信息 |
|
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42—的总物质的量浓度为6 mol/L,则此溶液最多可溶解铁粉的质量为( ) A. 5.6 g B. 11.2 g C. 22.4 g D. 33.6 g |
|
| 16. | 详细信息 |
|
A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去),下列推断不正确的是( ) A. 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 B. 若D是一种强碱,则A、B、C均可与X反应生成D C. 若D为NaCl,且A可与C生成B,则E可能是CO2 D. 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可能与铜反应生成B或C |
|
| 17. | 详细信息 |
|
在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为pg•cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( ) A. B. C. 上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5 D. 上述溶液中再加入同体积同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c (Cl-)>c(NH4+)>c (OH-)>c(H+) |
|
| 18. | 详细信息 |
二氧化氯(ClO2)是一种广谱、高效的消毒剂,易溶于水,尤其在水处理等方面有广泛应用。以下是某校化学研究小组设计实验室制取ClO2的工艺流程图。下列有关说法正确的是 ( ) A. 电解时发生反应的化学方程式为2HCl B. 由NaClO2溶液制取0.6 mol ClO2时,至少消耗0.1 mol NCl3 C. 将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的NH3 D. 溶液X的主要成分为NaClO2和NaOH |
|
| 19. | 详细信息 |
|
己知Li2Ti5O15和Na202中都含有过氧键,Ti的化合价为+4,Na202中含一个过氧键,则Li2Ti5O15中过氧键的数目为( ) A. 2个 B. 4个 C. 6个 D. 8个 |
|
| 20. | 详细信息 |
如右图所示,集气瓶内充满某气体,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体可能是 ①NH3 ②N2、H2 ③NO2、O2 ④SO2 ⑤SO2、Cl2 A. ①②③④⑤ B. ①②④ C. ①③④⑤ D. ②③④ |
|
| 21. | 详细信息 | ||||||||||||||||||||
下列各物质中,不能满足“
|
|||||||||||||||||||||
| 22. | 详细信息 |
|
向Fe2O3和Fe粉组成的混合物中加入适量的稀H2SO4,各物质均恰好完全反应,测得所得溶液中不含Fe3+,且Fe2+与H2的物质的量之比为4:1,那么在反应中Fe2O3、Fe、H2SO4之间的物质的量之比为( ) A. 1:1:1 B. 1:2:4 C. 1:2:3 D. 2:3:5 |
|
| 23. | 详细信息 |
|
(1)用KClO3在H2SO4存在下与SO2反应制得ClO2。请写出反应的离子方程式:______。 (2)把ag固体NaHCO3加热分解一段时间后,固体质量变为b g。 ①尚未分解的NaHCO3质量为________g。 ②当b为________g时,表明NaHCO3完全分解。 (3)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。 ①上述反应中氧化剂是__________________。 ②根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、 ③淀粉、④白酒、⑤食醋,你认为必须选用的物质有___________(填序号)。 ③某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________(填编号)。 A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4 ④请配平以下化学方程式:________□Al+□NaNO3+□NaOH===□NaAlO2+□N2↑+2H2O。若反应过程中转移5 mole-,则生成标准状况下N2的体积为________L。 |
|
| 24. | 详细信息 |
高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿制高锰酸钾的流程如下(部分条件和产物省略): 请回答下列问题: (1)提高锰酸钾浸出率(浸出锰酸钾质量与固体总质量之比)的措施有______ (任答一项即可) (2)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式:______。 (3)从经济性考虑试剂X宜选择(填名称):___________。上述流程中,设计步骤IV和V的目的是___。 (4)以惰性材料为电极,采用电解锰酸钾溶液的方法完成步骤III转化。 ①阳极反应式为______。 ②电解过程中,阴极附近电解质溶液的pH将________(填:增大、减小或不变)。 (5)测定高锰酸钾样品纯度:向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀。当溶液由紫红色刚好褪色且半分钟不变色,表明达到滴定终点。写出离子方程式:________ |
|
| 25. | 详细信息 |
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。请回答下列问题: (1)B中所含元素位于周期表中第____周期____族。 (2)A在B中燃烧的现象是_______________。 (3)D+E→B的反应中,被氧化与被还原的物质的物质的量比是________。 (4)G+J→M的离子方程式是 _________________。 (5)Y受热分解的化学方程式是 ___________________。 |
|
| 26. | 详细信息 |
现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L−1硫酸、6 mol·L−1盐酸和蒸馏水) 回答下列问题: (1)装置A中发生反应的化学方程式是______________________________________。 (2)装置B的作用是______________,装置C的作用是______________,装置E的作用是_____________。 (3)装置D中发生反应的化学方程式是______________________________________。 (4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。 |
|
| 27. | 详细信息 |
|
铅的单质、氧化物、铅盐在现代工业中有着重要的用途。 (1)工业利用锌冶炼过程中的铅浮渣生产硫酸铅的流程如下[已知铅浮渣的主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。  ①生产过程中,必须使浸出渣中仍含少量的铅单质,其目的是_________,废液中存在可循环利用于的物质,该物质是_______ , 加40%硫酸的目的是 _______ ②写出酸浸过程中单质铅反应的化学方程式:______,若沉淀物含有极少量CaSO4,则洗涤剂最好使用____ a.水 b.10%硫酸、水 c.Pb(NO3)2溶液、水 (2)已知铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2以及Pb3O4。Pb3O4能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出反应的化学方程式______________________。 |
|
最近更新






