北京高二化学期末考试(2018年下期)试卷带答案和解析
| 1. | 详细信息 | ||||||||||||
下列能量的转化过程中,由化学能转化为电能的是
|
|||||||||||||
| 2. | 详细信息 |
|
下列化学用语正确的是 A. HSO3-+ H2O C. NaHCO3 == Na+ + HCO3- D. H2S |
|
| 3. | 详细信息 |
下列关于金属腐蚀与防护的说法不正确的是 图① 图② 图③ A. 图①,放置于干燥空气中的铁钉不易生锈 B. 图②,若断开电源,钢闸门将发生吸氧腐蚀 C. 图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀 D. 图③,若金属M比Fe活泼,可防止输水管腐蚀 |
|
| 4. | 详细信息 |
|
下列溶液一定呈中性的是( ) A. pH=7的溶液 B. c(H+)=c(OH-)=10-6mol/L的溶液 C. 使酚酞试液呈无色的溶液 D. 酸与碱恰好完全反应生成正盐的溶液 |
|
| 5. | 详细信息 |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述不正确的是 A. 在温度、体积一定的条件下,通入1mol N2和3mol H2 反应后放出的热量为92kJ B. a曲线是加入催化剂时的能量变化曲线 C. 加入催化剂,也不能提高N2的转化率 D. 该反应的热化学方程式为:N2(g)+3H2(g) |
|
| 6. | 详细信息 |
|
下列实验事实不能用平衡移动原理解释的是 A. pH=11的氨水稀释10倍后溶液pH>10 B. 将氯化铝溶液加热蒸干并灼烧,最终得氧化铝固体 C. 对2HI(g) D. 水垢中含有CaSO4,可先用Na2CO3溶液浸泡处理,而后用盐酸去除 |
|
| 7. | 详细信息 | ||||||
以下是常温下几种弱酸的电离平衡常数:
|
|||||||
| 8. | 详细信息 | ||||||||||||
下列说法正确的是
|
|||||||||||||
| 9. | 详细信息 |
为研究沉淀的生成及其转化,某小组进行如下实验。关于该实验的分析不正确的是 A.①浊液中存在平衡:AgSCN(s) B.②中颜色变化说明上层清液中含有SCN- C.③中颜色变化说明有AgI生成 D.该实验可以证明AgI比AgSCN更难溶 |
|
| 10. | 详细信息 |
K2FeO4在水中不稳定,发生反应:4FeO42-+10H2O A. 由图Ⅰ可知K2FeO4的稳定性随温度的升高而减弱 B. 由图Ⅱ可知图中a>c C. 由图Ⅰ可知温度:T1>T2>T3 D. 由图Ⅰ可知上述反应△H>0 |
|
| 11. | 详细信息 | |||||||||||||||
|
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下: 电池: Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l); 电解池:2Al+3O2
|
||||||||||||||||
| 12. | 详细信息 |
常温下,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L HCl溶液,滴定曲线如图所示,下列说法不正确的是 A. a=20.00 B. 滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-) C. 若将盐酸换成相同浓度的醋酸,则滴定到pH=7时,a<20.00 D. 若用酚酞作指示剂,当滴定到溶液明显由无色变为浅红色时立即停止滴定 |
|
| 13. | 详细信息 |
|
下列选项中,微粒的物质的量浓度关系正确的是 A. 0.1 mol/L K2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) B. 0.1 mol/L NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) C. 等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:2c(K+)= c(HX)+c(X-) D. 浓度均为0.1 mol/L的NaHCO3溶液和NaOH溶液等体积混合:c(Na+)+ c(H+)=c(CO32-)+c(OH-)+c(HCO3-) |
|
| 14. | 详细信息 |
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是 A. 该过程是将太阳能转化为化学能的过程 B. 催化剂a表面发生氧化反应,有O2产生 C. 催化剂a附近酸性减弱,催化剂b附近酸性增强 D. 催化剂b表面的反应是CO2+2H++2e一=HCOOH |
|
| 15. | 详细信息 | ||||||||||||||||
(题文)氯碱工业中电解饱和食盐水流程及原理示意图如下图所示。 (1)生成H2的电极反应式是_________________________________________。 (2)Na+向________(填“E”或“F”)方向移动,溶液A的溶质是______________。 (3)电解饱和食盐水总反应的离子方程式是_____________________________。 (4)常温下,将氯碱工业的附属产品盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表。
|
|||||||||||||||||
| 16. | 详细信息 | |||||||||||||||||||||||||||||||||
|
工业上由N2、H2合成NH3。制备H2需经多步完成,其中“水煤气(CO、H2)变换”是纯化H2的关键一步。 (1)水煤气变换:CO(g)+ H2O(g) ① 平衡常数K随温度变化如下:
|
||||||||||||||||||||||||||||||||||
| 17. | 详细信息 | |||||||||||||||||||||||
近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下: (1)反应Ⅰ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) ΔH=+550 kJ·mol-1 它由两步反应组成:i. H2SO4(l)=SO3(g)+H2O(g) ΔH=+177 kJ·mol-1 ii. SO3(g)分解。 L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。  ① X代表的物理量是_____________________。 ② 判断L1、L2的大小关系是______________。 (2)反应Ⅱ:I-可以作为催化剂,可能的催化过程如下。 i. SO2+4I-+4H+=S↓+2I2+2H2O; ii. I2+2H2O+ SO2= SO42-+4H++2I-; 探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
|
||||||||||||||||||||||||
| 18. | 详细信息 | ||||||||||
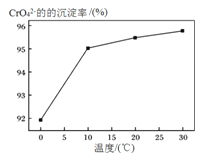
含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有K2Cr2O7的废水并回收重铬酸,具体的流程如下: 已知:i. CaCr2O7、BaCr2O7易溶于水,其它几种盐在常温下的溶度积如下表所示。
|
|||||||||||
| 19. | 详细信息 | ||||||||||||||||||||||||||
|
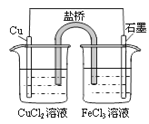
某小组同学利用原电池装置探究物质的性质。 资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。 (1)同学们利用下表中装置进行实验并记录。
|
|||||||||||||||||||||||||||