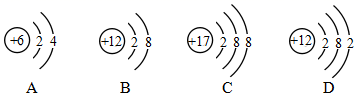2020天津九年级下学期人教版初中化学中考模拟
| 1. | 详细信息 |
|
下列变化,属于化学变化的是 A.石蜡熔化 B.盐酸挥发 C.粮食酿酒 D.海水晒盐
|
|
| 2. | 详细信息 |
|
地壳中含量最多的元素是( ) A.Si B.Al C.O D.Fe
|
|
| 3. | 详细信息 |
|
下列物质属于盐的是 A.盐酸 B.纯碱 C.生石灰 D.消石灰
|
|
| 4. | 详细信息 |
|
有关空气中主要成分的说法不正确的是 A.氮气可作保护气 B.稀有气体可用于制作霓虹灯 C.氧气可与多种物质发生反应 D.二氧化碳是一种空气污染物
|
|
| 5. | 详细信息 |
|
下列化肥属于复合肥料的是 A.氯化钾 B.磷矿粉 C.硝酸钠 D.磷酸氢二铵
|
|
| 6. | 详细信息 |
|
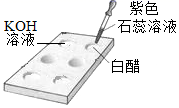
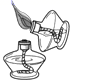
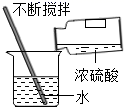
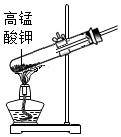
下列化学实验操作正确的是 A.
|
|
| 7. | 详细信息 |
|
厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生,这种气体是( ) A.二氧化碳 B.氧气 C.氢气 D.二氧化硫
|
|
| 8. | 详细信息 |
|
下列叙述正确的是 A.生铁和钢含碳量相同 B.木炭和一氧化碳都可以作燃料 C.一氧化碳和二氧化碳都有毒 D.棉花和塑料都属于天然纤维
|
|
| 9. | 详细信息 |
|
下列叙述正确的是 A.钢的性能优良,所以钢是很纯的铁 B.服用含氢氧化铝的药物可以治疗胃酸过多症 C.饱和溶液一定比不饱和溶液含溶质多 D.利用汽油的乳化作用可以除去衣服上的油污
|
|
| 10. | 详细信息 |
|
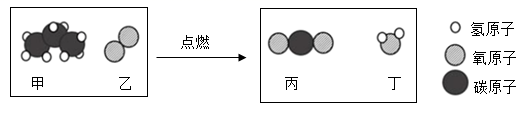
丙烷(C3H8)是液化石油气的主要成分之一,燃烧前后分子种类变化的微观示意图如下。下列说法正确的是( )
A.甲中碳、氢元素质量比为3:8 B.乙和丙的元素组成相同 C.44g甲完全燃烧至少需160g乙 D.生成的丙与丁的分子个数比为1:1
|
|
| 11. | 详细信息 |
|
推理是化学学习中常见的思维方法,下列推理正确的是 A.因为氧化物都含有氧元素,所以含有氧元素的物质一定是氧化物 B.如果两种化合物发生反应生成水,则该反应一定是复分解反应 C.金属与盐酸反应放出气体,与盐酸反应放出气体的物质不一定是金属 D.燃烧需要三个条件同时具备,灭火也必须同时破环这三个条件才能完成
|
|
| 12. | 详细信息 | |||||||||||||||
|
为达到以下实验目的,下列相应实验方案合理的是
A.A B.B C.C D.D
|
||||||||||||||||
| 13. | 详细信息 |
|
下列说法不正确的是 A.稀盐酸和稀硫酸都可用于除铁锈 B.铝比铁活泼,因而铝的抗腐蚀性能比铁差 C.固体氢氧化钠不可用作二氧化碳气体的干燥剂 D.金属与盐酸溶液发生置换反应后,溶液的质量一定增加
|
|
| 14. | 详细信息 | |||||||||||||||||||||||||
|
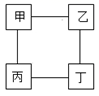
甲、乙、丙、丁四种物质间的反应如图所示,“一”表示相连的物质间在一定条件下可以反应,下列选项符合图示反应关系的是
A.A B.B C.C D.D
|
||||||||||||||||||||||||||
| 15. | 详细信息 |
|
向质量为10 g的碳酸镁、碳酸氢钠和氯化钠的混合物中,加入100g稀盐酸,恰好完全反应后,得到二氧化碳气体的质量是4.4 g。下列说法正确的是 A.混合物中氯化钠的质量一定为 1.6 g B.所加稀盐酸溶质的质量分数一定为 7.3% C.反应后溶液中氯化镁的质量一定大于氯化钠的质量 D.碳酸镁和碳酸氢钠无论以任何比例混合,得到二氧化碳的总质量均为4.4 g
|
|
| 16. | 详细信息 |
|
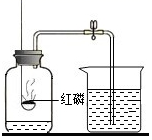
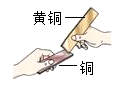
下列实验不涉及化学变化的是( ) A. C.
|
|
| 17. | 详细信息 |
|
人类生存需要清新的空气。下列一般不会造成空气污染的是( ) A.人工降雨 B.燃放烟花 C.焚烧垃圾 D.汽车尾气
|
|
| 18. | 详细信息 |
|
下列图示的实验操作中正确的是( ) A. C.
|
|
| 19. | 详细信息 |
|
认识燃烧原理可以利用和控制燃烧。下列说法不正确的是 A.空气中混有可燃性气体,在有限空间里遇明火可能发生爆炸 B.用煤炭烧锅炉时不断鼓入空气,可使煤炭燃烧更剧烈、更充分 C.实验桌上少量酒精着火时可用湿布盖灭,是因为降低了酒精的着火点 D.森林起火时,可在大火蔓延线路前砍掉一片树木,建立隔离带灭火
|
|
| 20. | 详细信息 |
|
下列说法不正确的是( ) A.细铁丝在氧气中燃烧时,火星四射,生成黑色固体 B.红磷在空气中燃烧产生大量的白雾 C.硫在氧气中燃烧生成有刺激性气味的气体 D.少量氯化铵与少量熟石灰粉末混合、研磨,放出刺激性气味气体
|
|
| 21. | 详细信息 |
|
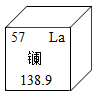
近期,英国《自然》杂志刊发了材料领域的最新研宄成果---一科学家找到了接近常温的超导材料“超氢化镧”。下列有关镧的说法错误的是( )
A.镧是金属元素 B.元素符号是La C.中子数是57 D.相对原子质量是138.9
|
|
| 22. | 详细信息 |
|
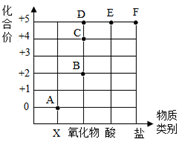
如图表示元素的化合价与物质类别关系,若它表示氮元素的部分关系图,则下列说法错误的是( )
A.A点对应的物质类别是单质 B.B点表示物质的化学式为NO C.某化合物的化学式为KNO3,它代表的点是F D.写出由D点表示的物质与水发生反应生成E的化学方程式:3NO2+H2O=2HNO3+NO
|
|
| 23. | 详细信息 |
|
下列课本实验中,说法正确的是( ) A.测定空气中氧气含量的实验中,可以用硫粉替代红磷 B.过滤时,滤纸要紧贴漏斗内壁 C.蒸发食盐水时,待蒸发皿内水分蒸干后,才停止加热 D.电解水实验中,加入的CuSO4做为催化剂
|
|
| 24. | 详细信息 |
|
下列图像分别对应四个变化过程,不能正确反映对应变化关系的是 A. B. C. D.
|
|
| 25. | 详细信息 |
|
在2A+3B=C+2D反应中,36gA与56gB恰好完全反应生成28gC和一定量的D,若C的化学式量为14,则C和D的化学式量之比为( ) A.7:1 B.7:8 C.7:16 D.7:32
|
|
| 26. | 详细信息 |
|
以下推理合理的是( ) A.分子可以构成物质,所以物质都是由分子构成的 B.碱溶液一定显碱性,所以显碱性的溶液一定是碱溶液 C.阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子 D.由不同种元素组成的纯净物是化合物,所以化合物一定含有不同种元素
|
|
| 27. | 详细信息 | |||||||||||||||
|
下列实验操作不能达到实验目的的是( )
A.A B.B C.C D.D
|
||||||||||||||||
| 28. | 详细信息 |
|
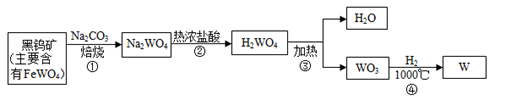
金属钨(W)可做白炽灯泡的灯丝。用黑钨矿主要含有钨酸亚铁(FeWO4)得金属钨(W)的工艺流程如下图所示:
其主要反应原理是: ① ② ③ ④ 下列说法不正确的是() A.反应③属于分解反应 B.反应①②③④的产物都有氧化物 C.反应①④中有元素的化合价发生改变 D.为加快反应的速率,可将黑钨矿石碾成粉末
|
|
| 29. | 详细信息 |
|
某混合气中可能有CO、水蒸气、CO2和N2中的两种或多种。为测定其组成,现将混合气依次通过浓硫酸、灼热的Fe2O3、澄清石灰水。一段时间后,浓硫酸质量增加,Fe2O3固体由红变黑,澄清石灰水变浑浊且有剩余气体。下列说法正确的是( ) A.该混合气体中一定有CO、水蒸气和N2,可能有CO2 B.该混合气体中一定有水蒸气、CO和CO2,可能有N2 C.该混合气体中一定有CO2和N2,可能有CO或水蒸气 D.该混合气体中一定有水蒸气和CO,可能有CO2或N2
|
|
| 30. | 详细信息 |
|
某K2CO3样品,可能含有Na2CO3、NaHCO3、CuCl2、NaCl中的几种杂质。取该样品6.9g,加入50g稀盐酸中,恰好完全反应得到无色溶液,同时产生2.2g气体。下列判断正确的是( ) A.反应后得到无色溶液,说明样品中一定没有CuCl2 B.NaCl不与盐酸反应,说明样品中一定没有NaCl C.所加稀盐酸中溶质的质量分数为3.65%≤w≤7.3% D.Na2CO3和NaHCO3都能和稀盐酸反应生成气体,说明样品中Na2CO3和NaHCO3至少有一种
|
|
| 31. | 详细信息 |
|
现有①维生素A②浓硫酸③甲烷④金刚石⑤二氧化氮⑥氯化钠,选择适当的物质填空(填序号)。 (1)可用来裁玻璃的是________________________。 (2)可用作干燥剂的是_______________________。 (3)可治疗夜盲症的是_______________________。 (4)可用作气体燃料的是_______________________。 (5)可造成酸雨的气体是_______________________。 (6)可用作厨房调味品的是_______________________。
|
|
| 32. | 详细信息 |
|
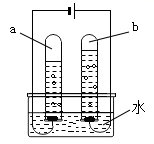
人类生产、生活离不开化学,用所学的知识填空。 (1)空气中O2所占的体积分数约为____。 (2)硬水是指含有较多可溶性___化合物的水。 (3)如图所示为电解水的实验,该实验证明水是由__组成的,若试管b中产生气体体积为6 mL,则试管a中产生气体体积为___mL,该反应的化学方程式是___。分解高氯酸钾(KClO4)也可制得氧气,高氯酸钾中氯元素的化合价是___。
(4)过滤器中的活性炭可除去有气味的物质,这是利用了活性炭的____性。
|
|
| 33. | 详细信息 |
|
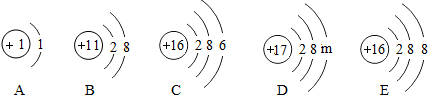
化学是从微观角度研究物质性质、组成、结构及其变化规律的科学。根据图示填空:
(1)图中A、B、C、D粒子共表示__________种元素。 (2)B与C所形成的化合物的化学式为______。 (3)晶体硅是制造半导体芯片的原料,如右图E是硅原子的结构示意图,图中x的值是__。
(4)硅元素的化学性质与A、B、C、D中__(填字母序号)元素的化学性质相似。 (5)“84消毒液”的成分为次氯酸钠(NaClO)、 氯化钠和水,其中NaClO为有效成分,写出氯气与氢氧化钠溶液反应制备“84消毒液”的化学方程式______。
|
|
| 34. | 详细信息 |
|
写出下列反应的化学方程式。 (1)镁在氧气中燃烧______________。 (2)高温煅烧石灰石______________。 (3)金属锌与稀硫酸反应______________。
|
|
| 35. | 详细信息 |
|
金属与我们生活息息相关。 (1)铸造硬币不需要考虑金属的_____ (填字母序号)。 A 硬度 B 抗腐蚀性 C 导电性 (2)铁制品锈蚀的过程,实际上是铁与空气中的__(填化学式)、水蒸气等发生化学反应的过程;铁锈的主要成分为___(填化学式)。 (3)写出氧化铁与一氧化碳在高温条件下发生反应的化学方程式_____。 (4)某钢铁厂每天需消耗5000t含Fe3O4 76%的磁铁矿石,该厂理论上可日产含Fe98%的生铁的质量是___t (结果精确到0.1)。
|
|
| 36. | 详细信息 |
|
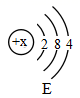
溶液与人们的生产、生活密切相关。 (1)将少量下列物质分别加入足量水中搅拌,可以得到溶液的是___(填字母序号)。 A 面粉 B 汽油 C 蔗糖 (2)在盛有水的烧杯中加入以下某种物质,在形成溶液的过程中,溶液温度明显降低的是_ (填字母序号)。 A 烧碱 B 硝酸铵 C 氯化钠 (3)固体物质甲和乙的溶解度曲线如图所示:
①t2°C时,甲的溶解度为____。 ②现有t1°C时甲的饱和溶液m1g和乙的饱和溶液m2g,下列关系一定成立的是__ (填字母序号) 。 A 两溶液中溶质的质量分数相等 B 分别升温至t2°C,所得溶液中溶质的质量分数相等 C 保持t1°C不变,分别加入等质量的水,所得溶液中溶质的质量分数相等 (4)将t1°C时乙的饱和溶液118 g稀释成质量分数为10%的乙溶液,需加水__g.
|
|
| 37. | 详细信息 |
|
根据所学化学知识回答问题。 (1)在粗盐提纯的实验中其主要的操作步骤顺序是__(填数字序号)。 ①过滤 ②溶解 ③蒸发 ④计算产率 (2)在蒸发加热过程中,应用玻璃棒不断搅拌,防止因局部温度过高,造成___;当蒸发皿中出现_时,应停止加热。 (3)欲除去粗盐中可溶性杂质Na2SO4、MgCl2、 CaCl2 得到纯净的NaCl,所加试剂为稍过量的BaCl2溶液、稍过量的___ (填化学式) 溶液、稍过量的Na2CO3溶液和适量的稀盐酸。 (4)纯净的氯化钠是重要的化工产品,熔融态的氯化钠通电可生成金属钠和氯气,写出该反应的化学方程式__。
|
|
| 38. | 详细信息 |
|
从下列选项中,选择一种合适物质的序号填空。 ①氦气 ②氧气 ③酒精 ④干冰 ⑤小苏打 ⑥大理石 (1)常用于人工降雨的是_____。 (2)常用于制作霓虹灯的是_____。 (3)常用于建筑材料的是_____。 (4)可用于面粉发酵的是_____。 (5)可用于急救病人的气体是_____。 (6)可用于配制医用消毒剂的是_____。
|
|
| 39. | 详细信息 |
|
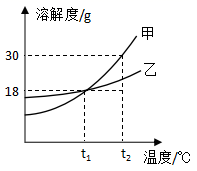
水是生命之源!“珍惜水、节约水、爱护水”是每个公民应尽的义务和责任。
(1)用如图1所示装置进行电解水的实验,a、b两玻璃管中收集到的气体质量比为_____,反应的化学方程式为_____,该实验证明水是由_____组成的; (2)饮用硬度过大的水不利于人体健康,在生活中可用_____区分硬水和软水; (3)如图2是自来水厂净化水的主要步骤。有关说法错误的是_____(填字母); A 步骤①中可加入明矾作絮凝剂 B X试剂可以是活性炭 C 步骤④的作用是消毒杀菌 D 净化后的水为纯净物 (4)下列做法会造成水体污染的是_____(填序号)。 ①工业废水处理达标后排放 ②随意丢弃废旧电池 ③提倡使用无磷洗衣粉 ④合理使用化肥和农药 (5)现有6.4g某种铁的氧化物,用足量的CO将其完全反应,将生成的气体通过足量澄清石灰水,得到沉淀10.0g,则这种铁的氧化物可能是_____。 A FeO B Fe2O3和Fe3O4 C FeO和Fe3O4 D Fe3O4
|
|
| 40. | 详细信息 |
|
按要求写出下列反应的化学方程式。 (1)磷燃烧的反应_____。 (2)工业制二氧化碳的反应_____。 (3)湿法炼铜的反应_____。
|
|
| 41. | 详细信息 |
|
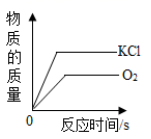
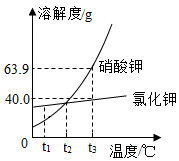
KNO3和KCl的溶解度曲线如下图所示:
(1)t3℃时,KNO3的溶解度为________。 (2)将t3℃时KCl的饱和溶液70.0g稀释成质量分数为20.0%的KCl溶液,需加水________g(精确到0.1g)。查阅相关物质的密度后,在实验室完成该实验通常需要的仪器有烧杯、量筒、________ (填字母标号)。 A托盘天平 B药匙 C胶头滴管 D玻璃棒 (3)现有t2℃时KNO3的饱和溶液m1g和KCl的饱和溶液m2g。不考虑水的蒸发,下列关系一定成立的是_______(填字母标号)。 A两溶液中溶质的质量分数相等 B分别降温到t1℃,析出KNO3的质量大于析出KCl的质量 C分别升温至t3℃,所得溶液中溶质的质量分数相等 D保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
|
|
| 42. | 详细信息 |
|
2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。 (1)建造航母用到了钛合金,构成金属钛的粒子是_____(填“原子”“分子”或“离子”),工业制钛有一种反应为: (2)航母外壳用涂料覆盖,是为了防止钢铁材料与_____接触而锈蚀。 (3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_____(填序号)。 A 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉 B ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液 C ZnCl2溶液中加入足量铜粉后,再加入铁粉 (4)铝制品形成致密保护膜的化学方程式是_____。 (5)氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是_____。
|
|
| 43. | 详细信息 |
|
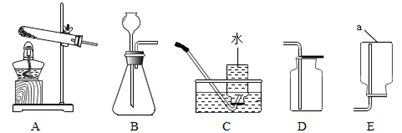
根据下列装置图回答问题:
(1)写出仪器a的名称:_____。 (2)实验室用氯酸钾和二氧化锰制氧气,该反应的化学方程式为_________。反应中二氧化锰所起的作用为__作用。 (3)实验室用石灰石和稀盐酸反应制取并收集二氧化碳,应选用的装置为___(填字母序号),该反应的化学方程式为____。
|
|
| 44. | 详细信息 |
|
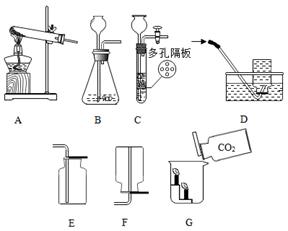
请根据下列各图中提供的信息回答问题:
(1)写出仪器a的名称:_____。 (2)请写出用装置B制取二氧化碳的化学方程式:_____。证明二氧化碳收集满的方法是_____。 (3)比较用过氧化氢溶液和用氯酸钾固体制取O2的方法,两者的共同点是_____。 A发生装置相同 B都可用MnO2做催化剂 C完全反应后剩余的固体成分相同 (4)装置B、C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是_____。 (5)用大理石和稀盐酸制取一瓶二氧化碳气体,将这瓶气体按G所示慢慢倒入烧杯中,观察到_____,说明二氧化碳具有的性质是_____。 (6)实验室用装置A制取氧气的化学方程式为_____;若用D装置收集氧气,实验操作中当等到_____再收集。
|
|
| 45. | 详细信息 |
|
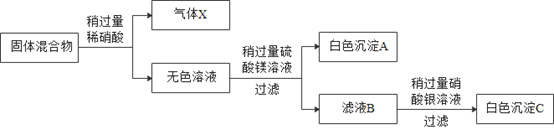
有一包白色固体,可能含氯化钠、碳酸钠、硫酸钠、氢氧化钠、氢氧化钡中的一种或几种。 为了研究该混合物的成分,某同学按下列流程进行了实验( 各步均恰好完全反应);
回答下列问题: (1)气体X的化学式____,白色沉淀C的化学式__。 (2)生成白色沉淀A的化学方程式为____。 (3)通过流程图分析原固体中一定不含有的物质是____。 (4)为探究固体混合物中是否含有氢氧化钠及质量,某研究性学习小组取固体混合物样品40.0g,按上述流程图进行实验,结果产生白色沉淀A23.3g,白色沉淀C28.7g,气体X2.2g。通过以上数据计算确定固体混合物中___ (填字母序号)。 A 含有氢氧化钠 B 不含氢氧化钠 C 氢氧化钠为4.0g D 氢氧化钠为5.9g
|
|
| 46. | 详细信息 |
|
维生素C (C6H8O6),主要存在于蔬菜、水果中。根据维生素C的化学式计算: (1)维生素C由 种元素组成; (2)一个维生素C分子中含有 个原子; (3)维生素C的相对分子质量为 ; (4)维生素C中氧元素的质量分数为 (结果精确到0.1%)。
|
|
| 47. | 详细信息 |
|
现有碳酸钙和氯化钙的固体混合物16g,其中含碳元素1.2g,将该混合物加入到100 g稀盐酸中,恰好完全反应。计算: (1)原固体混合物中碳酸钙的质量分数为多少? (2)所得溶液溶质的质量分数(结果保留至0.1%)。
|
|
| 48. | 详细信息 |
|
车用防冻液“冬天防冻、夏天防沸、全年防水垢、防腐蚀”的优良性能被爱车族广泛使用,现国际上普遍使用的是乙二醇 (1)乙二醇的相对分子质量为_____。 (2)乙二醇中C、H、O元素的质量比为_____。 (3)乙二醇中氧元素质量分数为_____。 (4)_____g乙二醇中氢元素质量与81g中水氢元素质量相等。
|
|
| 49. | 详细信息 |
|
现有一包含有氯化钠固体的纯碱样品,为测定其成分,同学们取一定质量的这种“纯碱”样品于试管中,加入103g稀盐酸,恰好完全反应,得到4.4g气体。将所得溶液冷却至t℃,恰好成为该温度下的饱和溶液,经测定溶液中的溶质含钠元素的质量为13.8g。求反应后所得溶液中溶质的质量分数。
|
|
| 50. | 详细信息 |
|
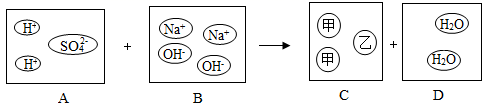
“宏观辨识与微观探析”是化学学科的核心素养之一。在宏观、微观和符号之间建立联系是化学学科的重要思维方式。 (1)根据下列粒子结构示意图,回答问题: ①上述示意图中,共包含_____种元素。 ②A、B、C、E中属于阴离子的是_____(填离子符号)。 ③若D表示某元素的原子,则该粒子在化学变化中容易_____(选填“得到”或“失去”)电子。 ④若D为离子,则BD构成的化合物的化学式为_____。 (2)根据氢氧化钠溶液和稀硫酸反应的微观示意图,回答问题:
①写出氢氧化钠溶液和稀硫酸反应的化学方程式_____。 ②从微观的角度分析,上述反应的实质是_____。
|
|
| 51. | 详细信息 |
|
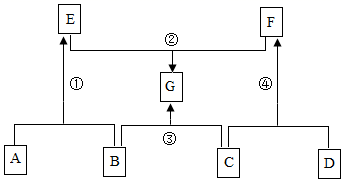
A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去)。其中A、B、C中均含有同一种元素,D是温室气体,G是重要调味品。请回答下列问题:
(1)G的化学式为_____。 (2)反应①的基本反应类型为:_____。 (3)反应③的化学方程式为:_____。 (4)F的一种用途是:_____。
|
|
- 济南市2019年九年级上半期化学期末考试试卷带解析及答案
- 江苏省兴化市板桥初级中学、泰兴市济川中学、泰州市第二中学附属初中、.泰州市口岸实验初级中学2020届初三4月四校联考化学
- 甘肃九年级化学中考真题(2018年下学期)附答案与解析
- 2019届初三上半年段考化学考题同步训练(山东省滨州市邹平县礼参中学)
- 甘肃省庆阳市西峰区北师大庆阳附校2020-2021年初三上半年期末化学题免费试卷在线检测
- 2019届九年级下学期期中考试化学题带答案和解析(广东省广州大学附属东江中学)
- 福建省泉州市丰泽区泉州九中2020-2021年初三上半期期中化学题免费在线检测
- 山西省临汾市襄汾县五校联考2020-2021年九年级上期期末化学题同步训练免费试卷
 B
B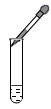 C
C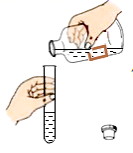 D
D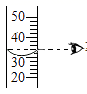
 B
B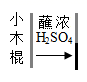
 D
D