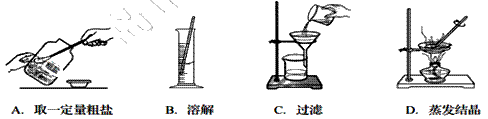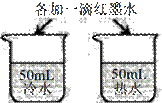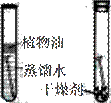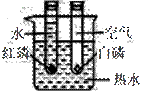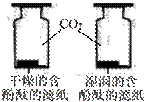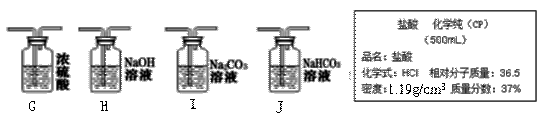江苏省南通市崇川区2019届九年级化学下学期阶段性调研试题及答案
| 1. | 详细信息 |
|
绿水青山就是金山银山。关于化学、物质、人类活动和环境问题的认识,合理的是 A.化学是环境污染的主因,没有化学,就不会产生环境问题 B.有毒的化学物质是环境污染的主因,应禁止使用 C.解决环境问题,应从源头禁止排放污染物,而不应先排放后治理 D.化工生产是环境污染的主因,化工生产一定会导致环境污染
|
|
| 2. | 详细信息 |
|
某兴趣小组的同学进行“粗盐中难溶性杂质的去除”实验。下图是实验过程中的部分操作其中正确的是
|
|
| 3. | 详细信息 |
|
我国古代科技高度发达,对中国古代著作涉及化学的叙述,下列解读不正确的是 A.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 B.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的“碱”是K2CO3 C.“青蒿一握,以水二升渍,绞取汁”,该过程属于化学变化 D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
|
|
| 4. | 详细信息 |
|
右图为铁元素在元素周期表中的信息,下列有关铁的说法结论正确的是 A.Fe3+中含有29个电子 B.铁的相对原子质量为55.85g C.铁原子、铁离子和亚铁离子的质量相差很小 D.人体缺铁会引起甲亢
|
|
| 5. | 详细信息 |
|
下列实验现象描述正确的是( ) A.在加热的条件下,一氧化碳还原氧化铜时,黑色粉末逐渐变为红色 B.电解水一段时间后,正负极产生气体的体积比约为2:1 C.红磷在空气中燃烧生成五氧化二磷 D.氨气能使干燥的蓝色石蕊纸花变红
|
|
| 6. | 详细信息 | |||||||||||||||
|
.对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
|
||||||||||||||||
| 7. | 详细信息 |
|
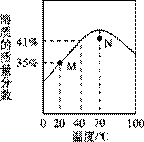
ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是 A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体 B. M点对应的ZnSO4溶液是不饱和溶液 C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大 D.40℃时,ZnSO4的溶解度为41g
|
|
| 8. | 详细信息 | ||||||||
|
化学学习让我们有很多收获,下列归纳总结不完全正确的一组是( )
|
|||||||||
| 9. | 详细信息 |
|
.推理是学习化学的一种重要方法。下列推理合理的是 A. 离子是带电的粒子,带电的粒子一定是离子, B. 单质是由同种元素组成的,则由同种元素组成的纯净物,一定是单质 C. 中和反应有盐和水生成,则有盐和水生成的反应,一定是中和反应 D. 溶液具有均一性和稳定性,则有均一性和稳定性的液体一定是溶液
|
|
| 10. | 详细信息 |
|
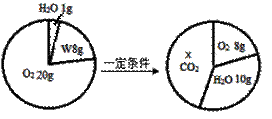
一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示,下列说法正确的是
A.X的值为22 B.该反应属于置换反应 C.W由碳、氢两种元素组成 D.W中碳、氢元素原子个数比为1:4
|
|
| 11. | 详细信息 |
|
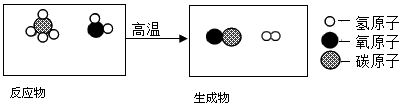
能源问题一直受到社会高度关注。 (1)煤、石油和天然气是三大化石燃料,不仅可以作燃料,还是重要的化工原料。 ①化石燃料的大量使用,带来了环境的污染和资源的枯竭等。某市自2018年开始推广车用乙醇汽油,到2019年实现全市全覆盖。乙醇(C2H5OH)燃烧的化学方程式是 ▲ ; ②天然气重整可以得到合成气,其反应的微观示意图如下: 写出上述反应的化学方程式 ▲ ;用不同催化剂可使合成气合成不同的物质。下列物质仅以合成气为原料不可能得到的是 ▲ (填序号)。 A.甲醛(CH2O) B.甲醇(CH3OH) C.尿素【CO(NH2)2】 (2)氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。 I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为: 6ZnFe2O4 ①制氢过程中,ZnFe2O4是反应的 ▲ ,其中Fe的化合价为 ▲ 。 ②该循环制氢中不断消耗的物质是 ▲ (填化学式) ,产生的氢气和氧气质量比是 ▲ 。 Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:2Mg2Cu+3H2 ③熔炼制备Mg2Cu合金时,通入氩气的目的是 ▲ 。 ④氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为 ▲ 。
|
|
| 12. | 详细信息 |
|
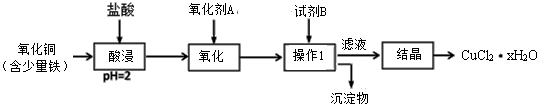
用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
已知:①在pH为4~5时,Fe3+几乎完全水解而转化为Fe(OH)3沉淀,Cu2+却不水解。 ②含Fe3+溶液遇到硫氰化钾(KSCN)溶液能够很灵敏显现出红色。 (1)在“酸浸”步骤中为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是 ▲ ,酸溶过程中发生反应的化学方程式: ▲ 。(写一个) (2)氧化剂A是为了将Fe2+转变为Fe3+,以便在后续操作中将溶液中的铁元素除去。从产品的纯度考虑,可选用下列氧化剂中的 ▲ (填编号)。 A.KMnO4 B.HNO3 C.Cl2 D.H2O2 (3)在实验室进行“操作1”所需的玻璃仪器有烧杯、玻璃棒和 ▲ ,在此过程中造成滤液浑浊可能的原因 ▲ 。 (4)设计最简实验证明滤液中Fe3+已沉淀完全(写出操作、现象及结论,试剂任选) ▲ 。 (5)用试剂B调节溶液 pH至5,从产品的纯度考虑,试剂B最好选用 ▲ (填编号) A.NaOH B.CuO C.Fe2O3 D.Fe (6)从滤液经过结晶得到氯化铜晶体的方法是: ▲ 、冷却结晶、过滤、洗涤、低温烘干。
|
|
| 13. | 详细信息 |
|
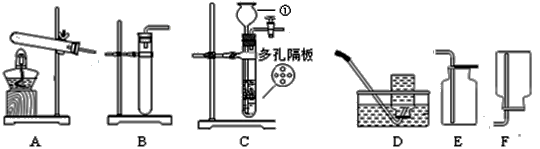
实验室现有高锰酸钾、大理石和37%的浓盐酸,及下列仪器,请回答有关问题: (1)指出图中仪器的名称:① ▲
(2)利用上述仪器和药品可以制取氧气,该反应的化学方程式为 ▲ ; (3)与装置B相比,C装置的优点是 ▲ (写一个),小明用C装置,取浓盐酸与石灰石反应制取气体,反应的化学方程式为 ▲ ; 【查阅资料】①碳酸钠溶液中通入二氧化碳发生反应: Na2CO3 + CO2 + H2O = 2NaHCO3 ②碳酸氢钠不与二氧化碳反应。如果小明想制的纯净的二氧化碳气体,可将气体依次通过下列试剂 ▲ ,并用上图中 ▲ 收集。
|
|
| 14. | 详细信息 |
|
)南南同学学完了溶质质量分数后与小组同学到实验室练习配制一定溶质质量分数的溶液。先用托盘天平称取纯净的氢氧化钠于洁净烧杯中,再用量筒量取自来水倒入烧杯中,搅拌后发现溶液中有白色浑浊物。对此现象小组同学都感到疑惑,于是进行了如下探究。【提出问题】白色浑浊物是什么物质? 【查阅资料】①自来水是硬水,常常含有Ca(HCO3)2和Mg(HCO3)2。 ②Ca(HCO3)2与足量的氢氧化钠反应方程式:Ca(HCO3)2+2NaOH = CaCO3↓+2H2O+ Na2CO3 Mg(HCO3)2与足量的氢氧化钠反应方程式: Mg (HCO3)2+2NaOH = Mg(OH)2↓+2H2O+ Na2CO3 ③Mg(OH)2在热水中溶解度增大,可形成稀碱溶液。 【作出猜想】猜想一:白色浑浊物是CaCO3 猜想二:白色浑浊物是Mg(OH)2 猜想三:白色浑浊物是 ▲ 【实验探究】 ①取氢氧化钠于烧杯中,加自来水水搅拌,杯壁发烫,原因是 ▲ 。静置冷却、过滤。 ②取①滤渣加稀盐酸,有气泡冒出。 ③另取①滤渣加热的蒸馏水,在上层清夜中再加 ▲ 试液,液体变红 【得出结论】猜想 ▲ 正确 【拓展延伸】南南认为实验探究①过滤后的滤液是纯净的氢氧化钠溶液,对吗?你的证明方法是取少量滤液于试管中,向其中滴加 ▲ ,若有 ▲ ,则不是纯净的氢氧化钠溶液。 【实验反思】①实验室在配制溶液时应该使用 ▲ 水。 ②用 ▲ 来判断自来水是否是硬水。
|
|
| 15. | 详细信息 |
|
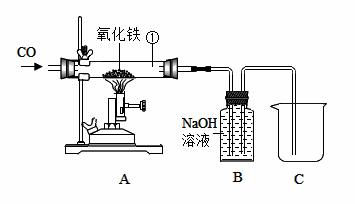
早在春秋战国时期,我国就开始生产和使用铁器。从1世纪起,铁成了一种最主要的金属材料,工业上可利用一氧化碳还原赤铁矿制得金属铁。 (1)如下图回答问题:
①加热一段时间后玻璃管内的现象是 ▲ ,反应的化学方程式为 ▲ ②你认为B装置的优点是 ▲
|
|