江苏省无锡市2018届九年级化学下学期考前适应性练习试题及答案
| 1. | 详细信息 |
|
改善环境质量是我们共同的责任,下列做法不利于保护环境的是 A.节能减排,利用太阳能光伏发电 B.绿色出行,提倡乘坐公共交通工具 C.方便生活,点外卖用一次性塑料餐盒 D.变废为宝,回收秸秆加工为生物柴油
|
|
| 2. | 详细信息 |
|
下列过程仅包含物理变化的是 A.干冰升华 B.钢铁生锈 C.食物变质 D.葡萄酿酒
|
|
| 3. | 详细信息 |
|
下列食物的近似pH如下,其中酸性最强的是 A.鸡蛋清7.6-8.0 B.柠檬2.2-2.4 C.西红柿4.0-4.4 D.牛奶6.3-6.6
|
|
| 4. | 详细信息 |
|
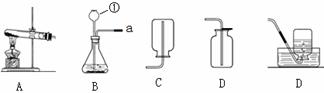
下列实验操作的图示正确的是
A B C D
|
|
| 5. | 详细信息 |
|
下列有关物质燃烧现象的叙述中,不正确的是 A.铁丝插入硫酸铜溶液:铁丝表面红色固体析出 B.硫粉在空气中燃烧:生成刺激性气味的气体 C.氯化铵与熟石灰研磨:有刺激性氨味放出 D.红磷在空气中燃烧:生成大量的白色烟雾
|
|
| 6. | 详细信息 |
|
铬酸钾(K2CrO4)是印染、电焊等工业的原料。铬酸钾中铬元素(Cr)的化合价为 A.+3 B.+4 C.+5 D.+6
|
|
| 7. | 详细信息 |
|
下列有关物质性质与用途的说法均正确的是 A.洗涤剂有乳化作用,可用于洗去油污 B.金属铝难与氧气反应,常用与制作炊具 C.氢氧化钠能与酸反应,常用于治疗胃酸过多 D.活性炭具有吸附性,常用于自来水杀菌消毒
|
|
| 8. | 详细信息 |
|
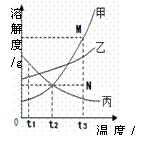
A.t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲 B.t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 C.若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲 D.若要将组成在N点的甲溶液转变为M点的甲溶液 可以采用恒温蒸发溶剂的方法
|
|
| 9. | 详细信息 |
|
大蒜中含有的一种有效成分“硫化丙烯”(C3H6S)具有一定的杀菌食疗作用。下列有关硫化丙烯的说法正确的是 A.硫化丙烯的相对分子质量为74 B.硫化丙烯中硫元素的质量分数最大 C.硫化丙烯分子中碳、氢、硫元素质量比为3:6:1 D.硫化丙烯由3个碳原子、6个氢原子和1个硫原子构成
|
|
| 10. | 详细信息 | |||||||||||||||
|
除杂是化学实验的重要环节,下列实验方法能达到实验目的是
|
||||||||||||||||
| 11. | 详细信息 | ||||
|
化学学习让我们有了很多收获,下列归纳总结完全正确的一组是
|
|||||
| 12. | 详细信息 |
|
铜在氯化铁溶液中发生反应:Cu+2FeCl3 = 2FeCl2+CuCl2。一定质量的铁与氧化铜的混合物在高温条件下恰好完全反应.将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后过滤,得到固体甲和滤液乙。取适量滤液乙于试管中,加入一定质量的锌粉,充分反应。 ①固体甲中一定含Cu,一定不含Fe ②滤液乙中一定含有FeCl2、CuCl2,一定不含FeCl3 ③若充分反应后Zn无剩余,溶液中若有CuCl2,则一定有FeCl2 ④若充分反应后Zn无剩余,溶液中若无CuCl2,则可能有FeCl2 ⑤若充分反应后Zn有剩余,则溶液中有ZnCl2,无CuCl2,可能有FeCl2 其中正确的个数有 A.2个 B.3个 C.4个 D.5个
|
|
| 13. | 详细信息 |
|
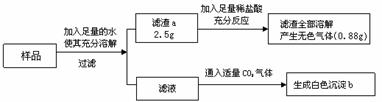
.有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。下列说法正确的是
A. 滤渣a一定有碳酸钙,一定没有硫酸钡、可能有氢氧化镁 B. 沉淀b是由氯化钡与二氧化碳反应生成 C.滤液中溶质一定有氯化钡、氯化钠,一定没有氢氧化钠 D.若“滤渣全部溶解”变为“部分溶解”,其它现象不变,则原样品中不能确定是否存在的物质是氯化镁
|
|
| 14. | 详细信息 |
|
下列是探究灭火原理的四个实验,其中说法不正确的是
A.实验Ⅰ中蜡烛熄灭、实验Ⅱ中蜡烛不熄灭,说明隔绝空气可以灭火 B.实验Ⅲ中蜡烛熄灭,因为稀盐酸与小苏打反应生成二氧化碳使温度降到着火点以下 C.实验Ⅳ中蜡烛熄灭,说明二氧化碳的密度比空气大且不能燃烧不支持燃烧 D.通过上述四个实验不能得出灭火的三个原理
|
|
| 15. | 详细信息 |
|
从“丝绸之路”到“一带一路”的倡议,促进了东西方经济、文化的交流. (1)“丝绸之路”把中国的丝绸、茶叶等传入西方,将西方的宝石等传入中国。 ①丝绸的主要成分是 。 A.纤维素 B.蛋白质 C.糖类 D.维生素 ②新鲜茶叶中含维生素C,缺乏会得 病。 ③宝石的成分复杂,其中所含的Al2O3 金属材料(选填“是”或“否”)。 写出铝离子的符号 。 (2)能源合作是“一带一路”的重要内容,中缅油气管道将石油和天然气输入中国。 ①将石油分离得到汽油、煤油等不同产品是 (选填“物理变化”或“化学变化”)。 ②写出天然气燃烧的方程式 ;做饭时,燃气灶的火焰呈黄色,锅底出现黑色,则需要调大炉具进风口,其原理: 。 ③温室效应是由CO2、CO、SO2气体中的 气体造成的。
|
|
| 16. | 详细信息 |
|
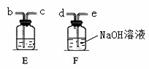
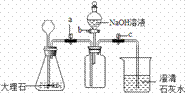
我们已经学习过实验室制取一些气体的反应原理、发生装置及收集方法,请根据下列实验装置图回答问题:
(2)如选用装置A作为制取氧气的发生装置,其化学方程式可以为 。 (3)实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为__________________,这种方法制得的氢气往往含有少量杂质气体,若用B、E、F等装置制取并收集纯净的氢气,则装置的接口顺序为:a→( ) ( ) →( ) ( ) →收集,其中E中所放的药品为 。
①打开止水夹a和c,关闭活塞b,从长颈漏斗向锥形瓶 中注入稀盐酸,使长颈漏斗下端管口浸没在液面下的原因 是 。 ②当观察 (填实验现象)时,说明集气瓶中已集满二氧化碳气体。再向集气瓶中加入适量的NaOH溶液后,关闭活塞a、b,轻轻振 荡集气瓶。一段时间后可观察到 ,证明二氧化碳与氢氧化钠发生了化学反应。 二氧化碳与氢氧化钠反应的化学方程式为: 。 ③有同学认为仅做上述实验不严密,应利用上图装置做一个对比实验。该对比实验所选的试剂是 ,产生的现象与上述实验不同的是 。
|
|
| 17. | 详细信息 | |||||||||||||||||||||||||||||
|
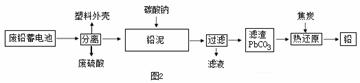
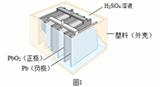
铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:
(1)图1铅蓄电池放电过程中,反应的化学方程式为 Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_____(填“增大”、“减小”或“不变”)。 (2)如图2是回收废铅蓄电池的一种工艺流程。 ①写出焦炭热还原生成铅的化学方程式: ②将流程图中的废硫酸和滤液按一定比例混合,再将所得的混合液经____、降温结晶、过滤等操作,可以析出Na2SO4·10H2O晶体。 ③如表是一些金属熔点的数据:
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 。
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
已知:2NH3+H2SO4═(NH4)2SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择___________ 。
|
||||||||||||||||||||||||||||||
| 18. | 详细信息 | ||||||||||||
|
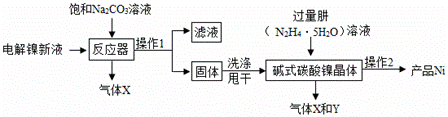
镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。 I.【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:
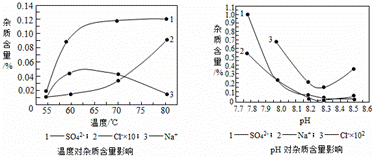
(1)反应器中一个重要反应为: 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2↓+3Na2SO4+2X,X的化学式为 。 (2)操作1名称是 , 洗涤操作1所得固体时,需用纯水洗涤,检验其洗净的方法(写出步骤、现象) 。 (3)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中95%酒精浸泡的目的 。 (4)物料在反应器中反应时需控制反应条件。分析下图,反应器中最适合的温度及pH分别为 。
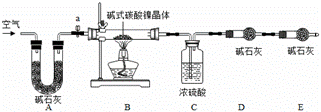
(5)生产中,pH逐渐增加,生成Ni(OH)2量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将 (填“升高”、“降低”或“不变”)。 Ⅱ.【测定碱式碳酸镍晶体的组成】 为测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O组成,某小组设计了如下实验方案及装置: 【资料卡片】 1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O 2、400℃左右,NiO会氧化生成Ni2O3.
【实验步骤】: ① 连接装置, ;②准确称取3.77g xNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,缓缓鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤ ;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表)
【实验分析及数据处理】: (1)完善实验步骤中的填空:① 连接装置, ;⑤ 。 (2)装置A的作用是 (3)计算 xNiCO3•yNi(OH)2•zH2O中x:y:z 的值。(写出计算过程)
|
|||||||||||||