2019广东九年级下学期人教版初中化学中考模拟
| 1. | 详细信息 |
|
下列变化属于化学变化的是 A.铁钉生锈 B.衣服晾干 C.干冰升华 D.剪纸成花
|
|
| 2. | 详细信息 |
|
人们常把金、银、铜、铁、锡等五种金属统称为“五金”。下列相关叙述错误的是( ) A.铁锅应用了铁的导热性 B.金属银可与硝酸铜溶液发生置换反应 C.金的化学性质最不活泼 D.焊锡(锡铅合金)比锡熔点要低
|
|
| 3. | 详细信息 |
|
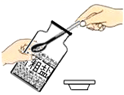
某兴趣小组的同学进行“粗盐中难溶性杂质的去除”实验。下图是实验过程中的部分操作其中正确的是( ) A. C.
|
|
| 4. | 详细信息 |
|
下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( ) A.蔗糖 B.花生油 C.面粉 D.冰块
|
|
| 5. | 详细信息 |
|
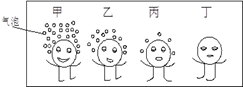
把甲、乙、丙三种金属分别加入稀硫酸中,甲、乙表面有气泡产生,丙无变化;再把甲放到乙的硫酸盐溶液中,甲表面析出乙。则三种金属的活动性顺序是 A.甲>乙>丙 B.乙>甲>丙 C.丙>甲>乙 D.丙>乙>甲
|
|
| 6. | 详细信息 |
|
下图为某粒子的结构示意图,下列说法正确的是
A.该粒子有12个质子 B.该粒子有2个电子层 C.该粒子属于非金属元素 D.该粒子已达到相对稳定结构
|
|
| 7. | 详细信息 |
|
如图是稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是
A.该反应是NaOH溶液滴入稀盐酸 B.a克是指加入NaOH溶液的质量 C.A点时,溶液的溶质为NaOH、NaCl D.B点表示稀盐酸和加入的NaOH溶液质量一定相同
|
|
| 8. | 详细信息 | ||||||||||
|
生活中一些食物和饮料的pH 如下表所示,若某位病患者的胃酸过多,你提出建议他在空腹时最适宜食用的是( )
A.葡萄 B.糖水 C.牛奶 D.玉米粥
|
|||||||||||
| 9. | 详细信息 |
|
下列物质的用途利用其物理性质的是 A.生石灰用作干燥剂 B.铁粉用作食品保鲜吸氧剂 C.铜用于制作导线 D.小苏打用于治疗胃酸过多
|
|
| 10. | 详细信息 |
|
下图是甲.乙.丙.丁四种常见金属与盐酸反应的比较示意图。以下说法错误的是( )
A.如乙金属为Fe,则乙与盐酸反应的化学方程式为:2Fe+6HCl=2FeCl3+3H2↑ B.金属甲.乙.丙与盐酸反应属于置换反应 C.若乙是金属Al,则丙可能是Zn和Fe D.四种金属的活动性强弱顺序为:甲、乙、丙、丁
|
|
| 11. | 详细信息 |
|
下列各组气体中既能用浓硫酸干燥,又能用苛性钠干燥的是 ( ) A.H2、O2 B.CO 2、N2 C.SO 2、CO D.SO 2、CO 2
|
|
| 12. | 详细信息 | ||||||||||||||||||||
|
除去下列物质中的少量杂质,所选试剂或方法正确的是( )
A.A B.B C.C D.D
|
|||||||||||||||||||||
| 13. | 详细信息 |
|
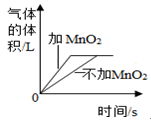
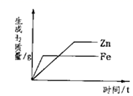
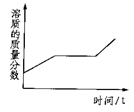
下列四个图象分别对应四种操作过程,其中正确的是( ) A.双氧水分解 B.向饱和氯化钠溶液中加水稀释 C.常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 D.将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直至有少量晶体析出
|
|
| 14. | 详细信息 |
|
实验室里有三瓶失去标签的无色溶液,只知道分别是澄清石灰水、氢氧化钠溶液和稀盐酸中的一种,下列四种试剂能将无色溶液只需要一次性鉴别开来的是( ) A.碳酸钠溶液 B.稀硫酸 C.氢氧化钡溶液 D.无色酚酞溶液
|
|
| 15. | 详细信息 |
|
化学与我们的生产、生活息息相关。现有四种物质: ①活性炭 ②熟石灰 ③氮气④小苏打。请选择以上相应物质的化学式填空。 (1)空气中含量最多的气体是______。 (2)食品工业中发酵粉的主要成分是______。 (3)常用于除去冰箱中异味的是______。 (4)农业上用于改良酸性土壤的是______。
|
|
| 16. | 详细信息 |
|
化学与生活息息相关。 (1)蒸鸡蛋是一道非常适合考生的补脑食品,鸡蛋中的鸡蛋清主要含有的基本营养素是_____。 (2)碘元素是人体必需的微量元素,缺乏碘元素会引起_____。 (3)炒菜完毕,关闭煤气罐阀门,燃着的煤气熄灭,其灭火的原理是_____。 (4)洗涤剂可用来洗碗,是因为它对油污具有______功能。 (5)常温下,铝制品耐腐蚀不易生锈的原因是______。(用化学方程式表示)
|
|
| 17. | 详细信息 |
|
在分子、原子的微观层面上研究物质及其化学反应是化学学科的特点。请回答:
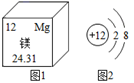
(1)如图1,镁的相对原子质量为___。 (2)如图2,表示的粒子属于 ___(填“原子”、“阳离子”或“阴离子”)。 (3)某反应的化学方程式为4X+11O2
|
|
| 18. | 详细信息 |
|
物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻。传接球“队员”间的物质在一定条件下必须能相互反应,场上“队员”位置及传球路线如图。
(友情提示:图示中连线间物质相互反应) (1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质名称是_____; (2)B位置“队员”所代表的物质的一种用途是______; (3)写出连线④代表的物质间发生反应的化学方程式____,连线①代表的物质间发生反应的化学反应的基本类型是____反应; (4)为实现“快速进攻”,氯化铜除传球给A位置“队员”外,还能直接传球给___“队员”(填物质名称)。
|
|
| 19. | 详细信息 |
|
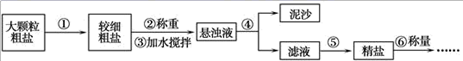
氯化钠在生活、生产中有广泛的用途。 Ⅰ.在农业生产上,常需要用质量分数为16%的氯化钠溶液选种。某同学配制100g质量分数为16%的氯化钠溶液,需要氯化钠的质量为___g;水的体积为____mL(水的密度近似看作1g/mL)。 Ⅱ.海水中提取氯化钠。利用风吹日晒可以从海水中提取粗盐,粗盐中一般含有少量泥沙等杂质。以下是 制备纯净氯化钠的实验流程,请据图回答问题。
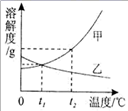
(1)操作⑤中用到的仪器有铁架台、玻璃棒、酒精灯、坩埚钳、_____。其中玻璃棒的作用是_____。 (2)实验结束后称量获得的精盐,并计算精盐的产率,发现产率偏低,其可能的原因是____(填序号)。 A 食盐没有全部溶解即过滤 B 蒸发时食盐飞溅剧烈 C 蒸发后,所得精盐很潮湿 D 过滤时滤纸有破损 (3)如图是甲、乙两种固体物质的溶解度曲线。
①_____℃时,甲、乙两种物质的溶解度相等。 ②t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲___乙(填“>”、“<”或“=”)。 Ⅲ.家庭制备氯化钠: 将洁厕灵(含有盐酸)与炉具清洁剂(含有氢氧化钠)混合,如下图甲所示。
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)__,此时溶液可用图乙中___(选填 A、B、C)点处表示。 ②若反应后溶液pH为7,图丙中a微粒的化学式为____。
|
|
| 20. | 详细信息 |
|
某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。
(1)生成二氧化碳的质量是 g; (2)加入60g稀盐酸后所得溶液中含有的溶质是 、 (填化学式); (3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%).
|
|
| 21. | 详细信息 |
|
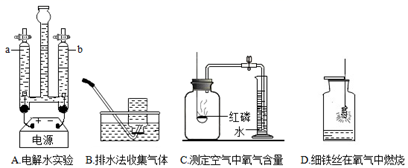
实验是进行科学探究的重要手段。请回答下列问题。
(1)实验 A 发生反应的化学方程式是_______,当电源接通一段时间后,a 管与 b 管中气体的体积比约为______。 (2)实验 B 集气瓶内装满水的目的是______. (3)实验 C 通过______现象,可得出氧气约占空气体积 1/5 的结论。 (4)实验 D 中水的作用是______。
|
|
| 22. | 详细信息 |
|
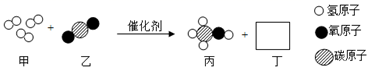
随着科学的发展,新能源的开发不断取得突破。清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下图(图中的微粒恰 好完全反应)所示。请根据微观示意图回答以下问题。
(1)丁的化学式为______,该反应的化学方程式为______。 (2)下列说法正确的是______(填写字母序号)。 A.反应前后原子数目发生改变 B.该反应属于复分解反应 C.甲是单质,乙、丙、丁均为化合物 D.该反应体现了无机物在一定条件下可以转化为有机物
|
|
| 23. | 详细信息 | |||||||||
|
小玲的爸爸是化学教授,她对爸爸的一项研究成果产生了兴趣:CO2 与 Na 在高温高压、催化剂的作用下,可以制得纳米级别的金刚石和一种白色固体。为了探究该白色固体的成分,小玲和同学一起来到爸爸的实验室,请你和她们一起完成如下探究: (提出问题)白色固体的成分是什么? (查阅资料)a.碳酸钠(Na2CO3)、氧化钠(Na2O)均为白色固体; b.氧化钠与水常温下反应生成氢氧化钠,Na2O+H2O=2NaOH。 (猜想与假设) 根据资料,小玲与两位同学提出以下猜想: 甲同学:“白色固体是氧化钠(Na2O)”; 乙同学:“白色固体是碳酸钠(Na2CO3)”; 小玲:_____ (实验与结论)①甲同学为验证猜想,取白色固体样品于试管中,加适量水,滴加无色酚酞溶液,通过酚 酞溶液变红就判断自己的猜想正确,但遭到其他同学反对,原因是:_____; ②为了验证自己的猜想,小玲设计了以下方案进行验证:
③通过上述实验可证明乙同学猜想正确,请写出Na与CO2反应的化学方程_____。
|
||||||||||
| 24. | 详细信息 |
|
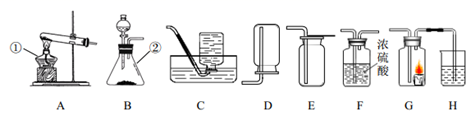
实验室制取气体时需要的一些装置如下图所示,请回答下列问题。
(1)写出标有序号的仪器名称:①___,②___。 (2)实验室制取氧气和二氧化碳的发生装置都可选用 B 装置的原因是____,装置中使用分液漏斗的优点是___。 (3)若要得到干燥的氧气,所选择装置的连接顺序为:B→____→___(填字母序号)。 (4)检验二氧化碳是否收集满的操作方法是__。 (5)某兴趣小组的同学连接 B、G、H装置进行实验。若实验时 G 装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则 B 装置中反应的化学方程式为___。 (6)(探究活动)探究二氧化碳能否与碱溶液反应
①分别振荡三个软质塑料瓶,观察到塑料瓶变瘪的程度由大到小的顺序为__。 ②对比A瓶与___瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应。
|
|
| 25. | 详细信息 |
|
已知氮化镁是一种微黄色的固体,可用于核废料的回收,极易与水反应,化学方程式为:Mg3N2+6H2O═3Mg(OH)2↓+2X↑.根据上述信息,计算下列问题: (1)氢氧化镁[Mg(OH)2]的相对分子质量___; (2)氮化镁中镁、氮元素的质量比___(最简整数比); (3)试确定X的化学式___.
|
|