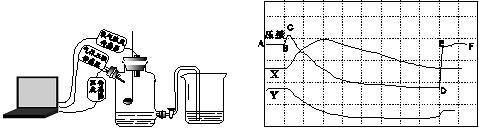2017北京九年级上学期人教版初中化学期末考试
| 1. | 详细信息 | ||||
|
下列化学家中,发现元素周期律并制出元素周期表的是
|
|||||
| 2. | 详细信息 | ||||
|
空气中体积分数约为78%的气体是
|
|||||
| 3. | 详细信息 |
|
下列物质在氧气中燃烧,火星四射并生成黑色固体的是 A.木炭 B.镁条 C.红磷 D.铁丝
|
|
| 4. | 详细信息 |
|
下列气体中,有毒的是 A.N2 B.O2 C.CO D.CO2
|
|
| 5. | 详细信息 | |||
|
右图为地壳中元素含量分布图,其中能代表氧元素的是 A.1 B.2 C.3 D.4
|
||||
| 6. | 详细信息 | ||||
|
铝的元素符号是
|
|||||
| 7. | 详细信息 | ||||
|
下列符号能表示2个氢原子的是
|
|||||
| 8. | 详细信息 |
|
下列物质中,不能溶于水形成溶液的是 A.食盐 B.蔗糖 C.花生油 D.酒精
|
|
| 9. | 详细信息 |
|
紫薯(右图)富含淀粉、蛋白质、维生素、钾、铁、钙、硒等,具有特殊的保健功能。其中的钾、铁、钙、硒指的是 A.单质 B.原子 C.分子 D.元素
|
|
| 10. | 详细信息 |
|
下列物质中,属于纯净物的是 A.石灰石 B.干冰 C.空气 D.糖水
|
|
| 11. | 详细信息 | |||||||
|
下列实验操作中,不正确的是
|
||||||||
| 12. | 详细信息 |
|
下列物质的化学式书写正确的是 A.硝酸银AgNO3 B.碳酸钾KCO3 C.氧化镁MgO2 D.氯化铁FeCl2
|
|
| 13. | 详细信息 |
|
化学变化前后发生改变的是 A.元素种类 B.原子个数 C.分子种类 D.原子质量
|
|
| 14. | 详细信息 |
|
已知一种氧原子,原子核内有8个质子和10个中子,则该氧原子中核外电子数为 A.2 B.8 C.10 D.18
|
|
| 15. | 详细信息 | ||||
|
下列物质的用途中,利用其物理性质的是
|
|||||
| 16. | 详细信息 |
|
盛放石灰水的试剂瓶内壁常附有一层白膜,除去该白膜选用的最佳试剂是 A.稀盐酸 B.蒸馏水 C.水 D.肥皂水
|
|
| 17. | 详细信息 | |||||||||||||||
|
下列实验操作一定能达到实验目的的是
|
||||||||||||||||
| 18. | 详细信息 | |||
|
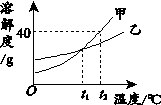
.甲、乙的溶解度曲线如右图所示。下列说法不正确的是 A.t1℃时,甲、乙两种饱和溶液中溶质的质量相等 B.t2℃时,甲的饱和溶液中溶质质量分数小于40% C.将t2℃时乙的饱和溶液降温到t1℃,溶剂质量不变 D.甲、乙的饱和溶液分别从t1℃升温到t2℃,两溶液中溶 质质量分数相等
|
||||
| 19. | 详细信息 |
|
氨基钠(NaNH2)是合成维生素A的原料。工业上将钠于97 ~ 100 ℃熔融,向反应容器中缓慢通入无水的液氨(NH3),再加热至350 ~ 360 ℃生成氨基钠和氢气。下列说法中,不正确的是 A.钠可能与水反应 B.钠的熔点比铁的熔点低 C.维生素A中一定含有钠元素 D.反应的化学方程式为:2Na + 2NH3
|
|
| 20. | 详细信息 |
|
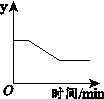
已知:Ca(HCO3)2
则y表示的是 A.Ca(HCO3)2的质量 B.固体中氧元素的质量 C.固体中钙元素的质量 D.固体中钙元素的质量分数
|
|
| 21. | 详细信息 |
|
空气和水是人类宝贵的自然资源。请回答21~22题。 空气是一种重要的资源。 (1)大气中二氧化碳含量过高会引起的环境问题是_______。 (2)人类时刻离不开空气,原因是空气中的氧气能 。 (3)举出一个氮气在生产生活中应用的实例: 。
|
|
| 22. | 详细信息 |
|
将碘溶解在酒精中制得碘的酒精溶液,即碘酒,可用于消毒。碘酒中的溶剂 是 。
|
|
| 23. | 详细信息 | ||||
|
请从24-A或24-B两题中任选1个作答,若两题均作答,按24-A计分。
|
|||||
| 24. | 详细信息 |
|
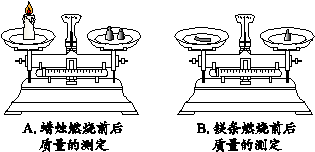
(1)木柴燃烧时,把木柴架空一些会燃烧更旺,原因是 。 (2)森林失火时,灭火队员通常要砍伐一些树木,开辟“防火隔离带”, 其主要目的是 。
方程式 。
|
|
| 25. | 详细信息 |
|
汽车方便了人们的出行。 (1)氢能源汽车备受人们关注,氢能源的优点有 (写出1条即可)。 (2)叠氮化钠(NaN3)被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发 NaN3迅速分解生成两种单质,写出该反应的化学方程式 。
|
|
| 26. | 详细信息 |
|
小明同学根据实践活动手册中的说明自制了豆腐。
(2)柠檬酸(C6H8O7)可用来点豆腐,下列说法不正确的是 。 A.柠檬酸中有21个原子 B.柠檬酸的相对分子质量为192g C.柠檬酸中碳、氢、氧元素的质量比为9:1:14 D.柠檬酸是由碳、氢、氧3种元素组成的混合物
|
|
| 27. | 详细信息 |
|
小红同学做了干冰跳入澄清石灰水的实验。 (1)小红观察到杯内云雾升腾,此现象说明干冰的性质是 。 (2)杯内的澄清石灰水变浑浊,发生反应的化学方程式为 。
|
|
| 28. | 详细信息 |
|
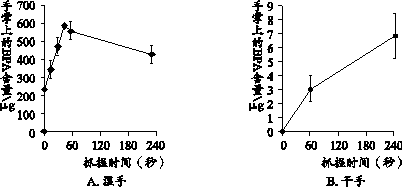
阅读下面科普短文。 购物小票你知多少 日常生活中,我们到超市购物结账时,都会拿到一张购物小票。网上曾流传“购物小票中含有毒的双酚A”的说法引发关注。 疑问1:小票中的双酚A是什么? 双酚A(Bisphenol A,简称BPA)其化学式为C15H16O2,通常状况下为白色结晶粉末,稍有酚味,不溶于水,能溶于碱溶液、乙醇、丙酮等。它是商业上使用量较大的化学品,可在热敏纸上充当显影剂和无色染料,这种热敏纸广泛用于飞机票、ATM机、加油机和收银机的凭据以及其他类型的小票。 疑问2:双酚A影响健康吗? 双酚A的确是一种有毒的化学物质,常温下稳定,高于100℃以上会释放,达到一定剂量会给身体带来健康隐患。专业机构检测结果显示,类似这种超市的购物小票中每100g约含有1 g的双酚A,人们在接触过程中的摩擦只会导致部分双酚A转移。也就是说即使是超市的收银员,按照每天接触200 g到300 g的热敏纸,折合下来也就是1 g到2 g双酚A的水平,它的量非常低。因而专家表示,即使是超市收银员的工作,也是比较安全的。虽然是在安全范围内,但还是要尽量通过一定的措施减少人体对其的接触和吸收。 疑问3:如何减少双酚A的吸收? 用手接触购物小票,小票中的双酚A会转移到手上,并能够经过皮肤被人体吸收。当使用含有皮肤渗透增强剂的消毒液后,转移量和吸收量还会大大增加。研究者们做了这样一个实验,先让被试者在刚使用完手部消毒液还未干透的情况下,用手掌握住购物小票;而在另一个实验中,被试者则用未使用过消毒液的干燥的手掌握住购物小票。随后研究者们用不含双酚A的湿巾擦拭被试者手掌表面,对残留的双酚A进行提取和分析。结果如下图所示:
虽然权威部门对低剂量双酚A的毒性尚未得出确切的结论,不过采取谨慎的态度,在日常生活中尽量减少对双酚A的接触还是有意义的。目前已有一些造纸企业采用了其他材料来代替双酚A。作为个人,通过养成一些良好的生活习惯,也可以帮助我们减少接触到双酚A,如日常生活中接触小票后,及时洗手可以较容易的冲洗掉。 依据文章内容回答下列问题。 (1)双酚A的物理性质有 (写出1条即可)。 (2)日常生活中接触购物小票,其中的双酚A不会对健康产生影响,其理由是 。 (3)通过文中图示,可获得的信息是 (写出1条即可)。 (4)下列说法不正确的是 。 A.双酚A是一种有机物 B.手上汗液较多时,尽量擦干后再接触小票 C.日常生活所接触的物品中,只有购物小票中含有双酚A D.图A中手掌上BPA含量先升高后降低,降低的原因是BPA释放了 (5)请你提出1条日常生活中减小接触到双酚A的建议 。
|
|
| 29. | 详细信息 |
|
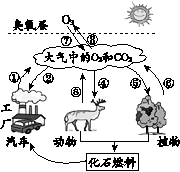
质循环,形成了自然界中物质的平衡。右图所示为氧气 和二氧化碳在自然界的主要循环途径。 (1)植物的光合作用过程中吸收的物质为 _______。 (2)图示大气中氧气的来源有 (填数字序号)。 (3)臭氧与氧气均是由氧元素组成,但其化学 性质不同,从微粒的角度解释其原因 。
|
|
| 30. | 详细信息 | ||
|
下列字母A~D所表示的物质,均由氢、碳、氧、氯、钙中的两种元素组成。 (1)上述元素中属于金属元素的是 (写元素符号)。 (2)A俗称生石灰。A的化学式为 。 (3)B为氧化物,将B通入到紫色石蕊溶液中,观察到溶液变红 。溶液变红的原因是 (用化学方程式表示)。 (4)C与B组成元素相同。写出C转化为B反应的化学方程式 。 (5)氢气不仅可以在氧气中燃烧,还可以在氯气(Cl2)中燃烧,发生化合反应生成D。若用“
|
|||
| 31. | 详细信息 |
|
下列是化学实验中常用的仪器。 (1)量取一定量的液体需要的仪器是________(填字母序号)。 (2)过滤操作除滤纸外,还需要的仪器有______(填字母序号)。 (3)举出1例说明玻璃棒在化学实验中的作用 。
|
|
| 32. | 详细信息 | |||
|
学完质量守恒定律后,为加深同学们的理解,老师又演示了如下实验。
(1)实验A中天平指针会 (填“左偏”、“不变”或“右偏”)。燃烧掉的石蜡的质量 (填“大于”、“小于”或“等于”)生成的二氧化碳和水蒸气的总质量。 (2)同学们预测实验B中最后指针会左偏,结果却右偏,其原因可能是 。
|
||||
| 33. | 详细信息 | |||||||||||
|
为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势 如图2所示。
图1 图2 (1)红磷燃烧的化学反应方程式为 。 (2)X曲线表示的是 (填“温度”或“氧气的浓度”)。 (3)结合X、Y两条曲线,解释图2中BC段气压变化的原因是 。 (4)实验中测得的数据如下:
根据实验数据计算:测得的空气中氧气的体积分数为 (列出计算式即可)。
|
||||||||||||
| 34. | 详细信息 |
|
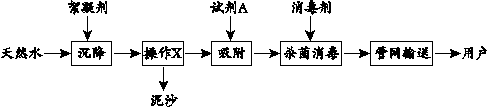
下列是自来水厂净化水的流程图。
(1)试剂A为 。 (2)高铁酸钾(K2FeO4)常用作絮凝剂和消毒剂,高铁酸钾中铁元素的化合价 为 。 (3)二氧化氯(ClO2)是新一代自来水消毒剂。它属于 (填字母序号)。 A.化合物 B.氧化物 C.混合物
|
|
| 35. | 详细信息 |
|
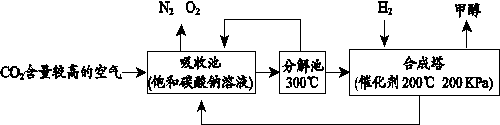
有人提出工业生产上回收利用空气中CO2的构想:把空气吹入饱和碳酸钠溶液中,溶液可吸收CO2生成碳酸氢钠(NaHCO3);加热碳酸氢钠分解放出CO2并生成碳酸钠;CO2在合成塔内与氢气反应生成甲醇。
(1)吸收池内参加反应的物质为 。 (2)合成塔中参加反应的氢气、二氧化碳与生成的甲醇和水的分子个数比为3:1:1:1, 则甲醇分子中碳、氢、氧原子的个数比为 。 (3)该流程中能循环利用的物质是 。
|
|
| 36. | 详细信息 |
|
实验室用高锰酸钾制取氧气,并验证氧气的化学性质。
实验1 实验2 (1)实验1中反应的化学方程式为 ;氧气可用排水法收集的原因是 。 (2)实验2中观察到的现象是 ,该反应的化学方程式为 。
|
|
| 37. | 详细信息 | ||||
|
利用右图装置可做多个实验。
是 。 (2)若将左管倾斜使其中的液体与右管中的固体接触,观察到有大 量气泡产生,气球鼓起,则左、右管中所加的药品可能为 。 (3)利用右图装置设计实验,证明可燃物燃烧条件之一为“温度达到物质的着火点”。 可供选择的其他实验用品:烧杯、、红磷、白磷、热水、冷水
|
|||||
| 38. | 详细信息 | |||||||||||||||||||||||||||||||||||||||||||
|
学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究。 【探究一】影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
(1)过氧化氢分解速率与温度的关系是 。 (2)能说明过氧化氢的分解速率与其质量分数有关的实验是 (填实验序号)。 【探究二】MnO2的聚集状态是否影响其催化效果? 将质量相同但聚集状态不同的MnO2分别加入到5mL5%的H2O2溶液中,测试结果 如下:
由上述实验得到的结论是 。 【探究三】其他金属氧化物能否起到类似MnO2的催化作用? 兴趣小组同学用天平称量0.2 g CuO,用量筒量取5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。
(1)小组同学通过上述实验得出结论:CuO可作过氧化氢分解的催化剂,支持该结论的实验证据是 。 (2)过氧化氢能被CuO催化分解放出氧气的化学反应方程式为 。 (3)欲比较不同催化剂CuO和MnO2对H2O2分解速率的影响,实验时需要控制的变量有 。
|
||||||||||||||||||||||||||||||||||||||||||||
| 39. | 详细信息 |
|
液氢和液氧是火箭发射的常用推进剂。已知卫星要被送达预定轨道,火箭至少要充分燃烧200 kg 的液氢才能产生足够能量。请依据相关反应的化学方程式计算:为满足这些液氢完全燃烧,至少应在火箭发动机中装入多少千克的液氧?
|
|