2019黑龙江高三上学期人教版(2019)高中化学期中考试
| 1. | 详细信息 |
|
下列反应中,在原理上可以设计成原电池的是( ) A. Ba(OH)2·8H2O与NH4Cl的反应 B. 氧化铝与硫酸的反应 C. 甲烷与氧气的反应 D. 石灰石的分解反应
|
|
| 2. | 详细信息 |
|
下列热化学方程式书写正确的是( ) A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=-1367.0kl B. NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kl/mol C. S(s)+O2(g)=SO2(g)△H=-296.8kl/mol D. 2NO2=O2+2NO △H=+116.2kl/mol
|
|
| 3. | 详细信息 |
|
下列说法正确的是 A. 强电解质溶液的导电能力一定比弱电解质溶液的强 B. 氨气是弱电解质,铜是强电解质 C. 氯化钠是强电解质,醋酸是弱电解质 D. 硫酸钠是强电解质,硫酸钡是弱电解质
|
|
| 4. | 详细信息 |
|
100 mL浓度为2 mol·L-1的盐酸跟锌片反应,以下操作对速率无影响的是( ) A. 升温 B. 加入5 mol·L-1的盐酸 C. 加入适量蒸馏水 D. 加入锌片
|
|
| 5. | 详细信息 |
|
在一定条件下,使NO和O2在一密闭容器中进行反应,下列说法中不正确的是( ) A. 反应开始时,正反应速率最大,逆反应速率为零 B. 随着反应的进行,正反应速率逐渐减小,最后为零 C. 随着反应的进行,逆反应速率逐渐增大,最后不变 D. 随着反应的进行,正反应速率逐渐减小,最后不变
|
|
| 6. | 详细信息 |
|
把a、b、c、d四块金属浸入稀H2SO4中,用导线两两相连可以组成各种原电池。若a、b相连时a溶解;c、d相连时c为负极;a、c相连时,c极上产生大量气泡;b、d相连时,b为正极,则四种金属活动性顺序由强到弱为( ) A. a>b>c>d B. a>c>d>b C. c>a>b>d D. b>d>c>a
|
|
| 7. | 详细信息 |
|
已知反应物的总能量高于产物的总能量,则反应是( ) A. 放热反应 B. 吸热反应 C. 有催化剂作用 D. 无法判断
|
|
| 8. | 详细信息 |
|
可逆反应2SO2(g)+O2(g) A. SO3、O2 B. SO2、SO3 C. SO2、O2、SO3 D. SO2、O2
|
|
| 9. | 详细信息 |
|
下列说法不正确的是( ) A. 体系有序性越高,熵值就越低 B. 自发过程可以导致体系的熵增大 C. 吸热反应不可以自发进行 D. 同种物质气态时熵值最大
|
|
| 10. | 详细信息 |
|
下列说法正确的是( ) A. HCl溶液中无OH- B. NaOH溶液中无H+ C. KCl溶液中既无H+也无OH- D. 常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14
|
|
| 11. | 详细信息 |
|
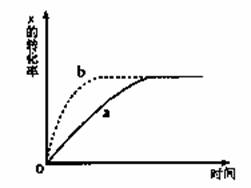
如图所示,a曲线表示一定条件下可逆反应:X(g)+Y(g)
A. 加入催化剂 B. 增大Y的浓度 C. 降低温度 D. 增大体系压强
|
|
| 12. | 详细信息 |
|
在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡: CH3COOH A. 加入水时,平衡向逆反应方向移动 B. 加入少量NaOH固体,平衡向正反应方向移动 C. 加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小 D. 加入少量CH3COONa固体,平衡向正反应方向移动
|
|
| 13. | 详细信息 |
|
.将纯水加热至较高温度,下列叙述正确的是( ) A. 水的离子积变大、pH变小、呈酸性 B. 水的离了积不变、pH不变、呈中性 C. 水的离子积变小、pH变大、呈碱性 D. 水的离子积变大、pH变小、呈中性
|
|
| 14. | 详细信息 |
|
在下列各溶液中,离子一定能大量共存的是( ) A. 强碱性溶液中:K+、Mg2+、Cl—、SO42— B. 室温下,pH=1的盐酸中:Na+、Fe3+、NO3—、SO42— C. 含有Ca2+的溶液中:Na+、K+、CO32—、Cl— D. 由水电离产生的c(H+)=1×10—3溶液中:Na+、K+、Cl—、SiO32—
|
|
| 15. | 详细信息 |
|
下列体系加压后,对化学反应速率没有影响的是 ( ) A. 2SO2+O2 C. CO2+H2O
|
|
| 16. | 详细信息 |
|
用pH试纸测定溶液pH的正确操作是( ) A. 将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照 B. 将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测点在试纸上,再与标准比色卡对照 C. 将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照 D. 将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
|
|
| 17. | 详细信息 |
|
下列微粒中不能破坏水的电离平衡的是( ) A. H+ B. OH- C. S2- D. Na+
|
|
| 18. | 详细信息 |
|
反应A(g)+3B(g) A. v(C)=0.04mol/(L·s) B. v(B)=0.06mol/(L·s) C. v(A)=0.03mol/(L·s) D. v(D)=0.01mol/(L·s)
|
|
| 19. | 详细信息 |
|
下列说法中,可以证明反应 N2+3H2 A. 一个N≡N键断裂的同时,有三个H-H键形成 B. 一个N≡N键断裂的同时,有三个H-H键断裂 C. 一个N≡N键断裂的同时,有两个N-H键断裂 D. 一个N≡N键断裂的同时,有六个N-H键形成
|
|
| 20. | 详细信息 |
|
在可逆反应中,平衡常数与反应进行的限度关系正确的是( ) A. K越大,反应程度越大 B. K越大,反应程度越小 C. K的大小与反应程度无关 D. 升高温度,K增大
|
|
| 21. | 详细信息 |
|
.已知下列热化学方程式:①H2(g)+1/2O2 (g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1 ,③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1,④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,回答下列问题: (1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为 ___________。(选数字) (2)燃烧1gH2生成液态水,放出的热量为_________________。 (3)液态水的稳定性_______气态水的稳定性(填“大于”、“小于”、“等于”)。 。
|
|
| 22. | 详细信息 |
|
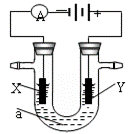
.电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: (1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则 ①电解池中X极上的电极反应式为______________________。 ②Y电极上的电极反应式为_________________________。 (2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是________________,电极反应式为_________________________。
|
|
| 23. | 详细信息 | ||||||||||||
|
在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g)
请回答下列问题: (1)该反应的化学平衡常数表达式为K =__________________。 (2)该反应为_________反应。(填“吸热”或“放热”) (3)若反应温度升高,CO2的转化率________(填“增大”“减小”或“不变”); (4)能判断该反应是否达到化学平衡状态的依据是______。 A.容器中压强不变 B.混合气体中 c(CO)不变 C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO) (5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____℃。
|
|||||||||||||
| 24. | 详细信息 |
|
.某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: (A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞; (B)用标准溶液润洗滴定管2-3次; (C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液; (D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm; (E)调节液面至0或0刻度以下,记下读数; (F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度。 完成以下填空: (1)正确操作的顺序是(用序号字母填写)______________________。 (2)实验中用左手控制_________(填仪器及部位),眼睛注视_______,直至滴定终点。判断到达终点的现象是___________。 (3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________________。 (4)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是____________。 (5)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是______。
|
|