2019й«ҳдёҖдёҠеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҹжң«иҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
зҺҜеўғжұЎжҹ“е·ІжҲҗдёәдәәзұ»зӨҫдјҡйқўдёҙзҡ„йҮҚеӨ§еЁҒиғҒпјҢдёӢеҲ—жұЎжҹ“зҺ°иұЎдёӯдё»иҰҒдёҺжҺ’ж”ҫSO2жңүе…ізҡ„жҳҜ пјҲВ В В В пјү A. иҮӯж°§з©әжҙһВ В В B. зҷҪиүІжұЎжҹ“В В В C. жё©е®Өж•Ҳеә”В В В D. й…ёйӣЁ
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢж“ҚдҪңй”ҷиҜҜзҡ„жҳҜпјҲВ В В В пјү A. еҲҶж¶ІжјҸж–—дҪҝз”ЁеүҚйңҖиҰҒе…ҲжЈҖжҹҘжҳҜеҗҰжјҸж¶І B. е®һйӘҢдёӯеү©дҪҷзҡ„й’ дёҚиғҪеҶҚж”ҫеӣһеҺҹиҜ•еүӮ瓶 C. еҒҡз„°иүІеҸҚеә”ж—¶пјҢй“Ӯдёқеә”з”Ёзӣҗй…ёжҙ—еҮҖ并зҒјзғ§иҮіж— иүІ D. и’ёйҰҸзғ§з“¶еҠ зғӯж—¶йңҖиҰҒеһ«зҹіжЈүзҪ‘
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдёҺеёёз”ЁеҚұйҷ©еҢ–еӯҰе“Ғзҡ„зұ»еҲ«дёҚеҜ№еә”зҡ„жҳҜпјҲВ В В В пјү A. ж°Ҝж°”дёҖжҳ“зҮғж°”дҪ“В В В B. жұҪжІ№вҖ”вҖ”жҳ“зҮғж¶ІдҪ“ C. жө“зЎ«й…ёвҖ”вҖ”и…җиҡҖе“ҒВ В В D. й«ҳй”°й…ёй’ҫвҖ”вҖ”ж°§еҢ–еүӮ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁNaCl еӣәдҪ“й…ҚеҲ¶0.1mo/L зҡ„NaCl жә¶ж¶І1000mLпјҢдёӢеҲ—ж“ҚдҪңжҲ–иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В В В пјү A. е°Ҷ5.85gNaCl еӣәдҪ“жә¶дәҺ1Lж°ҙдёӯеҸҜй…ҚжҲҗ0.1mol/Lзҡ„NaCl жә¶ж¶І B. з§°йҮҸж—¶пјҢе°ҶеӣәдҪ“NaCl зӣҙжҺҘж”ҫеңЁеӨ©е№іе·ҰзӣҳдёҠ C. еӣәдҪ“жә¶и§ЈеҗҺпјҢе°Ҷжә¶ж¶ІиҪ¬з§»еҲ°е®№йҮҸ瓶дёӯпјҢ然еҗҺеҗ‘е®№йҮҸ瓶дёӯзӣҙжҺҘеҠ ж°ҙзЁҖйҮҠеҲ°еҲ»еәҰзәҝ D. й…ҚеҲ¶жә¶ж¶Іж—¶е®№йҮҸ瓶дёӯеҺҹжқҘжңүе°‘йҮҸи’ёйҰҸж°ҙдёҚдјҡеҪұе“Қе®һйӘҢз»“жһң
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—ж°”дҪ“пјҢеҸҜд»Ҙз”ЁжҺ’ж°ҙ法收йӣҶзҡ„жҳҜпјҲВ В В В В В В пјү A. NOВ В В B. NH3В В В C. HClВ В В D. Cl2
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҜ№жҹҗдәӣй—®йўҳзҡ„и®ӨиҜҶжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В В В пјү A. жјӮзҷҪзІүе’ҢжҳҺзҹҫйғҪеёёз”ЁдәҺиҮӘжқҘж°ҙзҡ„еӨ„зҗҶпјҢдё”дәҢиҖ…зҡ„дҪңз”ЁеҺҹзҗҶзӣёеҗҢ B. Naзҡ„иҝҳеҺҹжҖ§жҜ”CuејәпјҢж•…еҸҜз”ЁNaдёҺCuSO4жә¶ж¶ІеҸҚеә”еҲ¶еҸ–Cu C. й“қеҲ¶йӨҗе…·дёҚе®ңз”ЁжқҘи’ёз…®жҲ–й•ҝж—¶й—ҙеӯҳж”ҫй…ёжҖ§гҖҒзўұжҖ§жҲ–е’ёзҡ„йЈҹзү© D. зҺ»з’ғгҖҒж°ҙжіҘгҖҒйҷ¶з“·гҖҒж°ҙжҷ¶йғҪжҳҜйҮҚиҰҒзҡ„зЎ…й…ёзӣҗжқҗж–ҷ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺж°Ҝж°”зҡ„еҸҷиҝ°дёӯпјҢй”ҷиҜҜзҡ„жҳҜпјҲВ В В В В В В пјү A. ж°Ҝж°”жҳҜдёҖз§Қй»„з»ҝиүІгҖҒжңүеҲәжҝҖжҖ§ж°”е‘ізҡ„жңүжҜ’ж°”дҪ“ B. й“ҒдёқеңЁж°Ҝж°”дёӯзҮғзғ§з”ҹжҲҗFeCl3 C. й“ңдёқеңЁж°Ҝж°”дёӯзҮғзғ§з”ҹжҲҗжЈ•й»„иүІзҡ„зғҹ D. ж°Ҝж°”дёҚе…·жңүжјӮзҷҪжҖ§пјҢдёҚиғҪдҪҝйІңиҠұиӨӘиүІ
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
|
жҸҗзәҜдёӢеҲ—зү©иҙЁпјҲжӢ¬еҸ·еҶ…зү©иҙЁдёәжқӮиҙЁпјүпјҢйҖүз”Ёзҡ„иҜ•еүӮе’Ңж–№жі•йғҪжӯЈзЎ®зҡ„жҳҜпјҲВ В В В пјү
A. AВ В В B. BВ В В C. CВ В В D. D
|
|||||||||||||||||||||
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗж–№зЁӢејҸд№ҰеҶҷжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В В В пјү A. й’ дёҺж°ҙпјҡ2Na+2H2O=2Na++2OH-+H2вҶ‘ B. CaCO3дёҺзЁҖзӣҗй…ёпјҡCO32-+2H+=CO2вҶ‘+H2O C. AlCl3жә¶ж¶ІдёӯеҠ е…Ҙи¶ійҮҸзҡ„ж°Ёж°ҙпјҡAl3++3OH-=Al(OH)3вҶ“ D. FeCl3жә¶ж¶ІдёҺFeеҸҚеә”пјҡFe3++Fe=2Fe2+
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁNAиЎЁзӨәйҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ пјү A. ж°Ёж°”зҡ„ж‘©е°”иҙЁйҮҸжҳҜ17g B. NAдёӘH2е’ҢNAдёӘO2зҡ„иҙЁйҮҸжҜ”дёә1вҲ¶16 C. ж ҮеҮҶзҠ¶еҶөдёӢпјҢ22.4 Lж°ҙдёӯеҗ«жңүзҡ„еҲҶеӯҗж•°зӣ®дёәNA D. 100 mL1mol/LMgCl2жә¶ж¶Ідёӯеҗ«жңү0.1mol Cl-
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
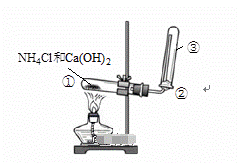
еёёз”ЁеҠ зғӯй“өзӣҗе’Ңзўұзҡ„ж··еҗҲзү©зҡ„ж–№жі•еҲ¶еҸ–гҖҒ收йӣҶж°ЁгҖӮдёӢеҲ—е®һйӘҢдёҚеҗҲзҗҶзҡ„жҳҜ
A. в‘ЎеӨ„з”Ёж№ҝж¶Ұзҡ„жЈүиҠұе өдҪҸиҜ•з®ЎеҸЈжҺ§еҲ¶NH3еӨ–йҖё B. в‘ЎеӨ„з”Ёж№ҝж¶Ұзҡ„зәўиүІзҹіи•ҠиҜ•зәёжЈҖйӘҢNH3жҳҜеҗҰйӣҶж»Ў C. дёҚ时移ејҖй…’зІҫзҒҜжҺ§еҲ¶в‘ еӨ„дә§з”ҹNH3зҡ„йҮҸ D. еҗ‘в‘ўдёӯеҠ е…Ҙй…ёеҢ–зҡ„AgNO3жә¶ж¶ІпјҢжЈҖйӘҢжҳҜеҗҰеҗ«ж°Ҝ
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
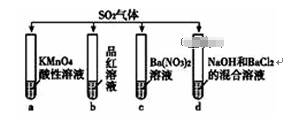
е°ҶSO2еҲҶеҲ«йҖҡе…ҘдёӢеҲ—4з§Қжә¶ж¶ІдёӯпјҢжңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ
A. иҜ•з®Ўaдёӯе®һйӘҢеҸҜд»ҘиҜҒжҳҺSO2е…·жңүжјӮзҷҪжҖ§ B. иҜ•з®Ўbдёӯжә¶ж¶ІиӨӘиүІпјҢиҜҙжҳҺSO2е…·жңүејәж°§еҢ–жҖ§ C. иҜ•з®ЎcдёӯиғҪдә§з”ҹзҷҪиүІжІүж·ҖпјҢиҜҘжІүж·Җзҡ„жҲҗеҲҶдёәBaSO3 D. иҜ•з®ЎdдёӯиғҪдә§з”ҹзҷҪиүІжІүж·ҖпјҢиҜҘжІүж·Җе®Ңе…Ёжә¶дәҺзЁҖзӣҗй…ё
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
жұҪиҪҰе®үе…Ёж°”еӣҠжҳҜеңЁеҸ‘з”ҹж’һиҪҰж—¶гҖҒдә§з”ҹдәҢж¬Ўзў°ж’һеүҚиғҪеӨҹиҮӘеҠЁиҶЁиғҖдҝқжҠӨд№ҳе‘ҳзҡ„иЈ…зҪ®пјҢзў°ж’һж—¶еҸ‘з”ҹеҸҚеә”дёәпјҡ10NaN3+2KNO3в•җK2O+5Na2O+16N2вҶ‘гҖӮдёӢеҲ—еҲӨж–ӯжӯЈзЎ®зҡ„жҳҜпјҲВ В В В В В В пјү A. N2ж—ўжҳҜж°§еҢ–еүӮеҸҲжҳҜиҝҳеҺҹеүӮ B. иҝҳеҺҹдә§зү©дёҺж°§еҢ–дә§зү©иҙЁйҮҸд№ӢжҜ”дёә1пјҡ15 C. жҜҸз”ҹжҲҗ16molN2иҪ¬з§»30moleп№Ј D. NaN3дёӯNе…ғзҙ иў«иҝҳеҺҹ
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдёӯпјҢдёҚеұһдәҺеҗҲйҮ‘зҡ„жҳҜпјҲВ В В В пјү A. йқ’й“ңВ В В B. дёҚй”Ҳй’ўВ В В C. зЎ¬й“қВ В В D. ж°ҙ银
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗжә¶ж¶Ідёӯж»ҙе…ҘBaCl2жә¶ж¶І,дә§з”ҹзҷҪиүІжІүж·Җ,еҶҚж»ҙе…ҘзЁҖзӣҗй…ё,жІүж·ҖдёҚжә¶и§Ј,еҲҷиҜҘжә¶ж¶Ідёӯ(В В ) A. дёҖе®ҡжңүSO42-В В В B. еҸҜиғҪжңүSO42-жҲ–Ag+В В В C. дёҖе®ҡж— Ag+В В В D. иҝҳеҸҜиғҪжңүCO32-
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
зЎ…еҸҠе…¶еҢ–еҗҲзү©еңЁжқҗж–ҷйўҶеҹҹдёӯеә”з”Ёе№ҝжіӣгҖӮдёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜпјҲВ В В В пјү A. жҷ¶дҪ“зЎ…еҸҜеҒҡе…үеҜјзәӨз»ҙВ В В B. SiO2еҸҜеҒҡи®Ўз®—жңәиҠҜзүҮ C. SiO2еҸҜдёҺж°ҙеҸҚеә”еҲ¶еӨҮзЎ…иғ¶В В В D. зҺ»з’ғгҖҒж°ҙжіҘгҖҒйҷ¶з“·йғҪжҳҜзЎ…й…ёзӣҗдә§е“Ғ
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
зҺ°жңүдёӢеҲ—еҚҒз§Қзү©иҙЁпјҡв‘ 0.1mol/LзЎ«й…ёгҖҒв‘Ўе°ҸиӢҸжү“гҖҒв‘ўзәҜзўұгҖҒв‘ЈдәҢж°§еҢ–зўігҖҒв‘Өи‘Ўиҗ„зі–гҖҒв‘Ҙ0.1mol/LNaOHжә¶ж¶ІгҖҒв‘Ұж°ўж°§еҢ–й“Ғиғ¶дҪ“гҖҒ⑧氨ж°ҙгҖҒв‘ЁAl2O3гҖҒв‘©жҳҺзҹҫ пјҲ1пјүдёҠиҝ°еҚҒз§Қзү©иҙЁдёӯпјҢеұһдәҺйқһз”өи§ЈиҙЁзҡ„жңү_____пјҲеЎ«еәҸеҸ·пјүгҖӮ пјҲ2пјүжңүдёӨз§Қзү©иҙЁеңЁж°ҙжә¶ж¶ІдёӯеҸҜеҸ‘з”ҹеҸҚеә”пјҢзҰ»еӯҗж–№зЁӢејҸдёәпјҡH++OH-=H2OпјҢиҝҷдёӨз§Қзү©иҙЁзҡ„еәҸеҸ·жҳҜ_________пјҲеЎ«еәҸеҸ·пјүгҖӮ пјҲ3пјүж—ўиғҪи·ҹзӣҗй…ёеҸҚеә”еҸҲиғҪи·ҹNaOHжә¶ж¶ІеҸҚеә”зҡ„жҳҜ__________пјҲеЎ«еәҸеҸ·пјүгҖӮ пјҲ4пјүж ҮеҮҶзҠ¶еҶөдёӢпјҢ_____Lв‘Јдёӯеҗ«жңү0.4molж°§еҺҹеӯҗгҖӮ пјҲ5пјүиғҪдә§з”ҹдёҒиҫҫе°”ж•Ҳеә”зҡ„жҳҜ__________пјҲеЎ«еәҸеҸ·пјүпјҢз”ҹжҙ»дёӯз”ЁжқҘеҮҖж°ҙзҡ„жҳҜ______пјҲеЎ«еәҸеҸ·пјү
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||||||
|
дёӢеӣҫжҳҜжҹҗе„ҝз«Ҙеҫ®йҮҸе…ғзҙ дҪ“жЈҖжҠҘе‘ҠеҚ•зҡ„йғЁеҲҶж•°жҚ®пјҡ еҢ»з–—жңәжһ„дёҙеәҠжЈҖйӘҢз»“жһңжҠҘе‘ҠеҚ•
ж №жҚ®дёҠиЎЁзҡ„ж•°жҚ®пјҢеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүиҜҘе„ҝз«Ҙ_____________е…ғзҙ еҗ«йҮҸеҒҸдҪҺгҖӮ пјҲ2пјүжҠҘе‘ҠеҚ•дёӯвҖңОјmol/LвҖқжҳҜ____________(еЎ«вҖңзү©иҙЁзҡ„йҮҸвҖқгҖҒвҖңдҪ“з§ҜвҖқжҲ–вҖңзү©иҙЁзҡ„йҮҸжө“еәҰвҖқпјүзҡ„еҚ•дҪҚгҖӮ пјҲ3пјүжңҚз”Ёз»ҙз”ҹзҙ CВ еҸҜдҪҝйЈҹзү©дёӯзҡ„Fe3+иҪ¬еҢ–дёәFe2+гҖӮеңЁиҝҷдёӘиҝҮзЁӢдёӯдҪ“зҺ°з»ҙз”ҹзҙ Cзҡ„____________пјҲеЎ«вҖңж°§еҢ–жҖ§вҖқжҲ–вҖңиҝҳеҺҹжҖ§вҖқпјүгҖӮ пјҲ4пјүзјәй“ҒжҖ§иҙ«иЎҖжӮЈиҖ…еә”иЎҘе……Fe2+гҖӮдёҖдәӣиЎҘй“ҒеүӮд»ҘзЎ«й…ёдәҡй“Ғдёәдё»иҰҒжҲҗеҲҶпјҢз”ЁзЎ«й…ёдәҡй“ҒеҲ¶жҲҗиҚҜзүҮж—¶еӨ–иЎЁеҢ…жңүдёҖеұӮзү№ж®Ҡзҡ„зі–иЎЈпјҢжҺЁжөӢзі–иЎЈзҡ„дҪңз”ЁжҳҜ________________________гҖӮ
|
||||||||||||||||||||||||||
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘй“ңе’Ңжө“зЎ«й…ёеҸҜд»ҘеңЁеҠ зғӯжқЎд»¶дёӢеҸ‘з”ҹеҰӮдёӢеҸҚеә”(еҸҚеә”ж–№зЁӢејҸе·Ій…Қе№і)пјҡCu+2H2SO4(жө“) (1)Aзү©иҙЁеҸҜд»ҘеҜјиҮҙй…ёйӣЁзҡ„еҪўжҲҗгҖӮеҲҷAеә”иҜҘеұһдәҺ______(з”Ёеӯ—жҜҚд»ЈеҸ·еЎ«еҶҷ) aпјҺй…ёВ В В В В bпјҺ зўұВ В В В В В cпјҺзӣҗВ В В В dпјҺй…ёжҖ§ж°§еҢ–зү©В В eпјҺзўұжҖ§ж°§еҢ–зү© (2)иҜҘеҸҚеә”дёӯиў«ж°§еҢ–зҡ„е…ғзҙ жҳҜ_________________пјҢеҸӮеҠ еҸҚеә”зҡ„ж°§еҢ–еүӮдёҺиҝҳеҺҹеүӮзҡ„зү©иҙЁзҡ„йҮҸд№ӢжҜ”дёә______гҖӮ (3)еҶҷеҮәиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ并用еҸҢзәҝжЎҘж ҮеҮәз”өеӯҗиҪ¬з§»зҡ„ж–№еҗ‘е’Ңж•°зӣ®пјҡ____________гҖӮ
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
.4.2gзҡ„зўій…ёж°ўй’ е’Ңзўій…ёй’ зҡ„ж··еҗҲзү©еҸ—зғӯеҲҶи§ЈеҗҺиҙЁйҮҸеҸҳдёә3.89gпјҢиҜ·й—®иҜҘж··еҗҲзү©дёӯзўій…ёй’ зҡ„иҙЁйҮҸеҲҶж•°дёәеӨҡе°‘пјҹ________________пјҲиҜ·еҶҷеҮәе…·дҪ“зҡ„и®Ўз®—жӯҘйӘӨпјү
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
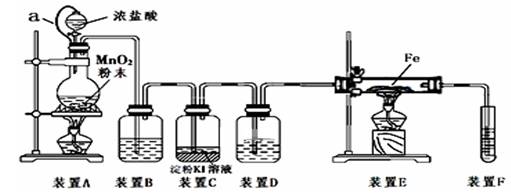
дёәдәҶжҺўз©¶е’ҢйӘҢиҜҒж°Ҝж°”зҡ„жҖ§иҙЁпјҢжҹҗз ”з©¶жҖ§еӯҰд№ е°Ҹз»„д»ҘMnO2е’Ңжө“зӣҗй…ёдёәдё»иҰҒеҺҹж–ҷпјҢи®ҫи®ЎдәҶеҰӮеӣҫжүҖзӨәиЈ…зҪ®(е…¶дёӯaжҳҜиҝһжңүжіЁе°„еҷЁй’ҲеӨҙзҡ„ж©Ўзҡ®з®ЎпјҢй’ҲеӨҙе·ІжҸ’е…Ҙ并з©ҝиҝҮж©Ўзҡ®еЎһ)иҝӣиЎҢдәҶз ”з©¶гҖӮ
пјҲиө„ж–ҷпјҡж°Ҝж°”дёҺй“ҒеҸҚеә”еҲ¶еҸ–ж°ҜеҢ–й“ҒиҰҒеңЁж— ж°ҙжқЎд»¶дёӢиҝӣиЎҢпјү иҜ•еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲlпјүиЈ…зҪ®AдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә_____________________гҖӮ пјҲ2пјүиЈ…зҪ®Bдёӯзҡ„иҜ•еүӮдёә_________пјҢиЈ…зҪ®DдҪңз”ЁжҳҜ________гҖӮ пјҲ3пјүиЈ…зҪ®CдёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә_____________________________гҖӮ пјҲ4пјүеҸҚеә”ејҖе§ӢеҗҺпјҢиЈ…зҪ®EеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә____________________________гҖӮ пјҲ5пјүиЈ…зҪ®FдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә________________________гҖӮ
|
|
- 2019-2020е№ҙй«ҳдёҖдёӢжңҹйҳ¶ж®өжҖ§иҖғиҜ•еҢ–еӯҰйўҳејҖеҚ·жңүзӣҠпјҲжұҹиӢҸзңҒиӢҸе·һйҷҶж…•й«ҳзә§дёӯеӯҰпјү
- е№ҝдёңзңҒжғ е·һеёӮжғ е·һдёӯеӯҰ2021еұҠй«ҳдёү12жңҲжңҲиҖғеҢ–еӯҰиҜ•еҚ·еңЁзәҝз»ғд№
- ж–°з–Ҷ2018е№ҙй«ҳдёҖеҢ–еӯҰдёҠеҚҠжңҹжңҹжң«иҖғиҜ•зҪ‘дёҠиҖғиҜ•з»ғд№
- 2018-2019е№ҙй«ҳдёҖдёҠеҚҠжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲпјҲеҢ—дә¬еёӮеёҲиҢғеӨ§еӯҰйҷ„еұһдёӯеӯҰпјү
- 2018е№ҙиҮі2019е№ҙй«ҳдәҢдёӢеӯҰжңҹ第дёҖж¬ЎжңҲиҖғеҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·пјҲжө·еҚ—зңҒе„Ӣе·һдёҖдёӯпјү
- 2019-2020е№ҙй«ҳдёҖдёҠжңҹжңҹдёӯиҒ”иҖғеҢ–еӯҰйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲжөҷжұҹзңҒжё©е·һеҚҒдә”ж ЎиҒ”еҗҲдҪ“пјү
- 2018е№ҙиҮі2019е№ҙй«ҳдәҢеҗҺеҚҠжңҹ第дёҖж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·е®Ңж•ҙзүҲпјҲж№–еҚ—зңҒж ӘжҙІеёӮж”ёеҺҝ第еӣӣдёӯеӯҰпјү
- ж·®еҢ—еёӮй«ҳдёҖеҢ–еӯҰдёӢеҶҢиҜҫж—¶з»ғд№ еҲ·йўҳи®ӯз»ғ