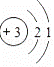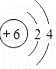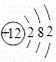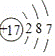2017江苏九年级下学期苏教版初中化学开学考试
| 1. | 详细信息 |
|
现代社会的生产和生活要消耗大量能量,下列活动中,通过化学反应提供能量的是( ) A. 发射航天飞机 B. 水力发电 C. 太阳能供热 D. 风力发电
|
|
| 2. | 详细信息 |
|
物质的结构决定物质的性质.下列关于物质结构与性质的说法不正确的是( ) A.生铁和钢的性能不同,主要是由于其含碳量不同 B.一氧化碳和二氧化碳的化学性质不同,是由于构成它们的分子不同 C.金刚石和石墨的物理性质不同,是由于构成它们的碳原子不同 D.金属钠和镁的化学性质不同,主要是由于钠原子和镁原子的最外层电子数不同
|
|
| 3. | 详细信息 |
|
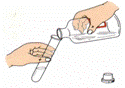
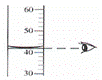
学习化学的一个重要途径是科学探究,实验是科学探究的重要手段,下列化学实验操作不正确的是( ) A. 液体的倾倒 B. 液体的量取 C. 点燃酒精灯 D. 滴加液体
|
|
| 4. | 详细信息 |
|
将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混和溶液中,充分反应后过滤,得到滤液M和滤渣N,下列有关说法中,不合理的是( ) A.滤液M中一定存在Fe2+ B.滤渣N的质量一定小于加入铁粉的质量 C.滤渣N中一定没有单质镁 D.滤液M中至少含有两种金属阳离子
|
|
| 5. | 详细信息 |
|
空气是人类宝贵的自然资源,下列有关空气的说法错误的是( ) A.液氮可用作制冷剂 B.氧气可用作火箭发射的燃料 C.氦气可用来填充探空气球 D.二氧化碳是植物进行光合作用必需的物质
|
|
| 6. | 详细信息 |
|
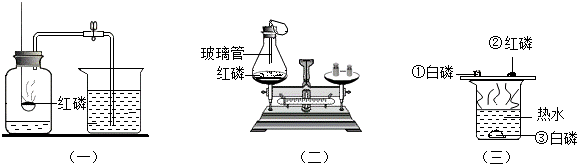
如图A、B、C是三个与磷燃烧有关的实验.下列说法正确的是( )
A.实验一的目的是探究空气中氧气的含量 B.实验二中,既可利用玻璃管引燃红磷,又可用气球缓冲瓶内压力 C.实验三中,采用了对比实验的研究方法,②③对比说明物质燃烧需要氧气 D.实验三中,采用了对比实验的研究方法,①②对比说明两物质的着火点不同
|
|
| 7. | 详细信息 |
|
下列事实的结论或解释中不正确的是( ) A.水烧开后易把壶盖冲起﹣﹣说明温度升高分子会变大 B.公园的桂花开放时满园飘香﹣﹣说明分子在不断运动 C.二氧化碳能用来灭火﹣﹣因为二氧化碳不能燃烧也不支持燃烧 D.铝制品有抗腐蚀性能﹣﹣实质是表面生成了致密氧化膜起保护作用
|
|
| 8. | 详细信息 |
|
逻辑推理是一种重要的化学思维方法,下列推理合理的是( ) A.金属遇酸有气体产生,则与酸反应产生气体的一定是金属 B.因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 C.因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 D.因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素
|
|
| 9. | 详细信息 | |||||||||||||||
|
除去下列物质中的杂质,所选用的方法不正确的是( )
A.A B.B C.C D.D
|
||||||||||||||||
| 10. | 详细信息 | ||||||||||||||||||
|
为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
下列判断正确的是( ) A.表中a的值为4.6 B.X可能是该反应的催化剂 C.X可能含有氢元素 D.X只含碳氧元素
|
|||||||||||||||||||
| 11. | 详细信息 | ||||||||||||||
|
以下是部分元素的原子结构示意图:
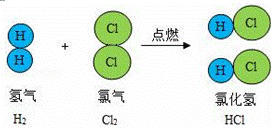
(1)该表中金属元素有 种. (2)氟元素的一个原子 个电子后,形成相对稳定结构的离子,符号为 . (3)从原子结构示意图可以判断,氯元素分布于元素周期表的第 个周期. (4)最外层电子数与元素的化学性质关系密切.锂元素的化学性质与 元素相似. (5)根据如图中蕴含知识回答:
①反应的化学方程式为 .②若有2n个氯气分子参加反应,则生成氯化氢分子的个数为 . ③生成物由 构成.
|
|||||||||||||||
| 12. | 详细信息 |
|
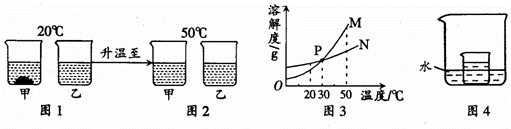
水和溶液在生命活动和生产、生活中起着十分重要的作用. (1)自来水生产过程中先用过滤的方法除去水中不溶性杂质,再进行消毒.X是一种常见的自来水消毒剂,工业上制取X的化学方程式为:Cl2+2NaClO2=2NaCl+2X,则X的化学式是 ,NaClO2中阴离子的化合价为 . (2)井水中通常含有较多的钙、镁离子,属于硬水.可用加入 的方法区别井水和蒸馏水.请写出生活中降低井水硬度的一种方法 . (3)下面是水与其他物质之间的转化关系(反应条件及部分反应物已省去).其中属于化合反应的化学方程式为 .CH4→H2O→Ca(OH)2→H2O (4)下列有关水的说法正确的是 . A.溶液中有水存在时水一定是溶剂 B.在水蒸发的过程中,水分子分解成氢原子和氧原子 C.水不可以用来鉴别硝酸铵、氢氧化钠、氯化钠、碳酸钙四种固体 D.水分子可以保持水的化学性质 (5)20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.请结合图示回答下列问题:
①图1中一定为饱和溶液的是 . ②图3中表示乙的溶解度曲线是 ;P点表示的含义是 . ③在图4所示的实验中,小烧杯内盛放的是20℃时甲物质的饱和溶液.某同学要使小烧杯内有固体析出时,他应向大烧杯的水中加入下列物质中的 (填字母). A.氧化钙 B.氯化钠 C.氢氧化钠 D.硝酸铵.
|
|
| 13. | 详细信息 |
|
过氧化钠(Na2O2)是一种供氧剂,与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.将质量为19.6g的不纯的Na2O2(只含有NaOH杂质)加入到87.6g水中,恰好完全反应后,所得溶液的质量为104g(水的挥发忽略不计).请计算: (1)生成氧气的质量为 g. (2)反应后所得溶液中溶质的质量 g. (3)将所得溶液稀释成溶质的质量分数为10%的溶液,需加水的质量 g.
|
|
| 14. | 详细信息 |
|
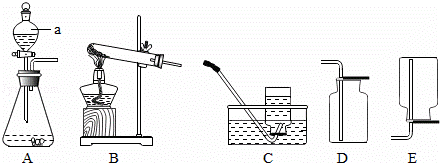
通过化学学习,我们已经掌握了实验室制取气体的一般规律.下面是实验室提供的一些实验装置:
请结合图中提供的仪器回答问题. (1)写出图中标号a的仪器名称 . (2)实验室可用高锰酸钾、双氧水来制备氧气,应选用的实验装置对应为 ,发生反应的化学方程式分别是 、 ,在以上选用的装置中有一种需作改进,改进的方法是 . (3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体. ①若用加热氯化铵和氢氧化钙的固体混合物制取氨气,则应选择的反应发生装置和收集装置对应为 . ②请写出氨气和氧化铜在加热条件下反应的化学方程式: .
|
|
| 15. | 详细信息 |
|
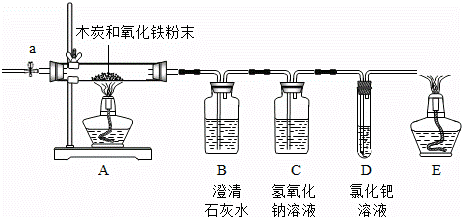
已知木炭粉(假设木炭粉中不含杂质)和氧化铁粉末在加热条件下能发生化学反应,某兴趣小组对该反应展开了如下的探究活动. 【查阅资料】将CO通入氯化钯溶液中,会出现黑色沉淀.氢氧化钠溶液能充分吸收二氧化碳.氧化铁能溶于盐酸中. 【实验过程】同学们设计了如下图所示装置(部分夹持仪器已略去).
(1)探究反应中产生气体的成分: 称取9.0g氧化铁和1.2g木炭粉,混合均匀后进行实验.打开止水夹a通一段时间的氮气后,关闭a.再对木炭粉和氧化铁粉末的混合物加热一段时间,观察到澄清石灰水变浑浊,氯化钯溶液中出现黑色固体.木炭与氧化铁粉末反应一定生成了 气体;E处酒精灯的作用是 ;B中发生反应的化学方程式为 ;加热前通一段时间氮气的原因是 . (2)探究反应后剩余固体的成分: 【提出猜想】 猜想1:只含有铁; 猜想2:含有铁和木炭;猜想3:含有 ; 猜想4:含有铁、木炭和氧化铁. 【实验验证】 该小组同学测得剩余固体质量后,将剩余固体置于烧杯中,向其中加入足量的稀盐酸,固体全部 溶解且有大量气泡出现,猜想不成立的是 .若剩余固体质量为6.6g,则剩余固体中含有的物质为 、剩余固体成分的质量是 .
|
|