天津市蓟县擂鼓台中学2020-2021学年高二上学期化学第一次月考试卷
天津市蓟县擂鼓台中学2020-2021学年高二上学期化学第一次月考试卷
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
室温下,向圆底烧瓶中加入1molC2H5OH和含1molHBr的氢溴酸,溶液中发生反应;C2H5OH+HBr
 C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是( ) C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是( )
A . 加入NaOH,可增大乙醇的物质的量
B . 增大HBr浓度,有利于生成C2H5Br
C . 若反应物增大至2 mol,则两种反应物平衡转化率之比不变
D . 若起始温度提高至60℃,可缩短反应达到平衡的时间
|
|
| 2. 单选题 | |
|
下列说法错误的是( )
A . 需要加热才能发生的反应不一定是吸热反应
B . 任何放热反应在常温条件下一定能发生
C . 反应物和生成物所具有的总能量的相对大小决定了反应是放热还是吸热
D . 吸热反应在一定条件下(如常温、加热等)也能发生
|
|
| 3. 单选题 | |
|
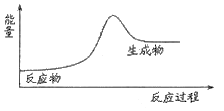
下列反应中的能量变化关系符合如图所示的是( )
A . 盐酸与烧碱反应
B . 天然气燃烧
C . 三氧化硫与水反应
D . 煅烧石灰石
|
|
| 4. 单选题 | |
|
列依据热化学方程式得出的结论正确的是( )
A . 已知2SO2(g)+O2(g)
 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 已知2SO2(g)+O2(g) 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 已知2SO2(g)+O2(g)  2SO3(g)为放热反应,达到平衡后,再加入SO2反应的ΔH减小
C . 已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 , 则任何酸碱中和反应的热效应均为57.3 kJ
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1<ΔH2 2SO3(g)为放热反应,达到平衡后,再加入SO2反应的ΔH减小
C . 已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 , 则任何酸碱中和反应的热效应均为57.3 kJ
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1<ΔH2
|
|
| 5. 单选题 | |
|
下列说法正确的是( )
A . 升高温度反应速率增大,主要原因是反应物分子中活化分子百分数增大
B . 有气体参加的反应,增大压强,活化分子百分数增大,所以速率加快
C . 增大反应物浓度,增大单位体积内活化分子百分数,有效碰撞次数增大
D . 催化剂不影响活化能,但能增大单位体积内活化分子百分数
|
|
| 6. 单选题 | |
|
一定量的FeCl3溶液与KSCN溶液反应达到平衡状态,下列条件不能使化学平衡移动的是( )
A . 加少量KCl固体
B . 加少量铁粉
C . 增大 FeCl3溶液的浓度
D . 升高温度
|
|
| 7. 单选题 | |
|
反应N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol表示的意义为( ) 2NH3(g) △H=-92.4kJ/mol表示的意义为( )
A . 1 mol N2 和3 mol H2 充入密闭容器中反应放出92.4kJ热量
B . 1 mol N2 和3 mol H2 充入密闭容器中反应吸收92.4kJ热量
C . 每生成2 mol NH3 放出92.4 kJ热量
D . 每生成2 mol NH3 吸收92.4 kJ热量
|
|
| 8. 单选题 | |
|
在一定温度下,恒容密闭容器中,充入一定量的NO和O2 , 发生2NO(g)+ O2(g)
 2NO2(g),反应达到平衡的标志是 ( ) 2NO2(g),反应达到平衡的标志是 ( ) ① NO、O2、NO2分子数目比是2:1:2 ② 反应混合物中各组分物质的浓度相等 ③ 混合气体的颜色不再改变 ④ 混合气体的密度不再改变 ⑤ 混合气体的平均相对分子质量不再变化 ⑥2υ正(O2) = υ逆(NO2)
A . ③④⑤
B . ①②
C . ②③④
D . ③⑤⑥
|
|
| 9. 单选题 | |
|
反应C(s)+H2O(g)
 CO(g)+ H2(g)在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( ) CO(g)+ H2(g)在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( )
A . 增加H2O(g)的物质的量
B . 将容器的体积缩小一半
C . 保持体积不变,充入N2使体系压强增大
D . 保持压强不变,充入N2使容器体积变大
|
|
| 10. 单选题 | |
|
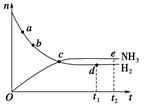
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)
 2NH3(g)(正反应为放热反应),673 K,30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( ) 2NH3(g)(正反应为放热反应),673 K,30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
A . c点处正反应速率和逆反应速率相等
B . a点处正反应速率比b点处的大
C . d点(t1时刻)和e点(t2时刻)处n(N2)不同
D . t2点时刻,正反应速率大于逆反应速率
|
|
最近更新