江苏省南通市海门区2021-2022学年高三12月第二次诊断测试化学试题
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
工业上通过Al2O3+N2+3C
 2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( ) 2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
A . N2的电子式为:
|
|
| 2. 单选题 | |
|
T、W、X、Y、Z是原子序数依次增大的五种短周期主族元素且分布于三个周期,W元素可形成硬度最大的单质,X是地壳中含量最多的元素,Y与X同主族。下列说法不正确的是( )
A . 原子半径:r(Z)>r(Y)>r(X)>r(W)>r(T)
B . Y、Z的最高价氧化物对应水化物的酸性:Y<Z
C . 第一电离能:W<X
D . W、X可分别与T形成含有非极性键的极性分子
|
|
| 3. 单选题 | |
|
阅读下列材料,回答问题:
FeCl3是棕红色固体,易潮解,在300℃以上可升华成含二聚三氯化铁( 方法①:氯化法。以废铁屑和氯气为原料,在立式反应炉里反应,生成的氯化铁蒸气和尾气由炉的顶部排出,进入捕集器冷凝为固体结晶。 方法②:熔融法。将铁屑和干燥氯气在低共熔混合物(如30%KCl与70%FeCl3混合)内进行反应生成氯化铁,升华后收集在冷凝室中,该法制得的氯化铁纯度高。 方法③:复分解法。用氧化铁与盐酸反应后得到氯化铁溶液。 方法④:氯化亚铁合成法。将铁屑溶于盐酸中,然后向其中通入氯气得到氯化铁。
|
|
| 4. 单选题 | |
|
阅读下列材料,回答问题:
含硫矿物如黄铁矿(FeS2)、黄铜矿、芒硝在工业上有着重要的用途。收集黄铜矿炼铜过程中产生的SO2制备SO3 , 其反应为2SO2(g)+O2(g)
|
|
| 5. 单选题 | |
|
工业上以碳酸镐矿(主要成分为MnCO3 , 另含FeO、Fe2O3 , CaO等杂质)为主要原料生产镒酸锂(LiMn2O4)的工艺流程如下
下列有关说法不正确的是( )
A . 可以采用搅拌的方法提高“酸浸”时碳酸镒矿的浸出速率
B . 氧化过程的离子方程式:8H++
 +5Fe2+=Mn2++5Fe3++4H2O
C . “过滤”后的溶液中大量存在的离子有:K+、Mn2+、 +5Fe2+=Mn2++5Fe3++4H2O
C . “过滤”后的溶液中大量存在的离子有:K+、Mn2+、  D . “气体1”是含CO2的两种混合气体,另一种可能是CO
D . “气体1”是含CO2的两种混合气体,另一种可能是CO
|
|
| 6. 单选题 | |
|
一种抗血栓药物新抗凝的结构如右图所示,以下说法不正确的是( )
A . 该物质存在顺反异构体
B . 1mol新抗凝最多可与3molNaOH发生反应
C . 该物质能与金属—钠发生置换反应A
D . 新抗凝和足量H2加成后的产物中有5个手性碳原子工
|
|
| 7. 单选题 | |
|
室温下:
 、 、 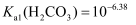 、 、  、 、  实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下 实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下 下列所得结论正确的是( )
A . 实验1溶液中存在:
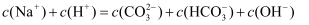 B . 由实验2可得
B . 由实验2可得  C . 实验3反应的离子方程式:CO2+H2O+2
C . 实验3反应的离子方程式:CO2+H2O+2 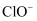 = =  +2HClO
D . 实验4所得上层清液中的 +2HClO
D . 实验4所得上层清液中的 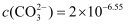 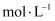
|
|
| 8. 单选题 | |
|
甲醛中木材加工、医药等方面有重要用途。甲醇利用脱氢法可制备甲醛,主要反应为:CH3OH(g)
 HCHO(g)+H2(g) HCHO(g)+H2(g)  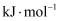 。Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下: 。Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下: 历程ⅰ: 历程ⅱ: 历程ⅲ: 历程ⅳ: 如图所示为在体积2L的恒容容器中,投入1molCH3OH,在碳酸钠催化剂作用下,经过 5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的CH3OH中生成HCHO的百分比),下列有关说法正确的是( )
A . 600℃时,前5min内生成甲醛的平均速率v(HCHO)=0.055
 B . 700℃时,反应历程ⅱ的速率小于反应历程ⅲ的速率
C . 脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D . 反应历程ⅰ的活化能大于CH3OH(g)
B . 700℃时,反应历程ⅱ的速率小于反应历程ⅲ的速率
C . 脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D . 反应历程ⅰ的活化能大于CH3OH(g)  HCHO(g)+H2(g)的活化能 HCHO(g)+H2(g)的活化能
|
|
| 9. 综合题 | |
|
钒广泛应用于钢铁工业,钒的氧化物在化学工业常用作催化剂。某沉钒废水(含Al3+、Fe2+、VO2+)钒含量约为2%。从该沉钒废水中分离出铁元素并制备V2O5的流程如下所示:
已知:①钒元素的存在形态较多,部分四价钒和五价钒物种的分布分数与pH的关系如图-1所示。 ②Fe(OH)2完全沉淀的pH为8.4;VO(OH)2完全溶解的pH约为11 ③吉布斯自由能(
|
|
| 10. 综合题 | |
|
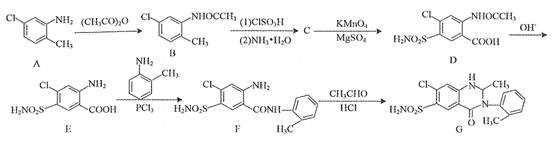
美托拉宗临床上用于利尿降压。其一种合成路线为:
已知:①
|
|



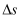 >0
>0
 的空间构型为平面三角形
的空间构型为平面三角形




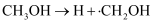
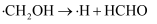
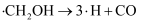


 G)可以用来判断反应进行的方向。一个反应的
G)可以用来判断反应进行的方向。一个反应的 
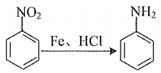 ②
② 



