2016年江西省新余市分宜县高考化学五模试卷
2016年江西省新余市分宜县高考化学五模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
关于0.1 mol/L H2SO4溶液的叙述错误的是( )
A . 1 L该溶液中含有H2SO4的质量为9.8 g
B . 0.5 L该溶液中氢离子的物质的量浓度为0.2 mol/L
C . 从1 L该溶液中取出100 mL,则取出溶液中H2SO4的物质的量浓度为0.01 mol/L
D . 取该溶液10 mL,加水稀释至100 mL后H2SO4的物质的量浓度为0.01 mol/L
|
|
| 2. 单选题 | |
|
已知化学反应C(s)+O2(g)
 CO2(g)、2CO(g)+O2(g) CO2(g)、2CO(g)+O2(g)  2CO2(g)都是放热反应,据此判断,下列说法错误的是( ) 2CO2(g)都是放热反应,据此判断,下列说法错误的是( )
A . 12gC所具有的能量一定高于28gCO所具有的能量
B . 56gCO和32gO2所具有的总能量大于44gCO2所具有的总能量
C . 12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D . 将一定质量的碳燃烧,生成CO2比生成CO时放出的热量多
|
|
| 3. 单选题 | |
|
下列离子方程式正确的是( )
A . 用醋酸除水垢:CaCO3+2H+═Ca2++H2O+CO2↑
B . 用小苏打治疗胃酸过多:HCO3﹣+H+═CO2↑+H2O
C . 向溴化亚铁溶液中通入足量氯气:2Br﹣+Cl2═Br2+2Cl﹣
D . 向澄清石灰水中通入过量二氧化碳:Ca2++2OH﹣+CO2═CaCO3↓+H2O
|
|
| 4. 单选题 | |
|
氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下列说法正确的是( )
A . 一个16O原子的质量为16g
B . 17O的相对原子质量约为17
C . 氧元素的相对原子质量为
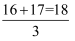 D . 氧元素的相对原子质量为(16a%+17b%+18c%)
D . 氧元素的相对原子质量为(16a%+17b%+18c%)
|
|
| 5. 单选题 | |
|
2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行.能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是( )
A . 点燃,能燃烧的是矿物油
B . 测定沸点,有固定沸点的是矿物油
C . 加入水中,浮在水面上的是地沟油
D . 加入足量氢氧化钠溶液共热,不分层的是地沟油
|
|
| 6. 推断题 | |
|
某固体混合物可能含Al、(NH4)2SO4、MgCl2、AlCl3、FeCl3中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如下图(气体体积已换算成标准状况下的体积).下列叙述不正确的是( )
A . 该实验的整个过程共涉及6个化学反应
B . 该实验的整个过程只涉及1个氧化还原反应
C . 混合物中一定有Al、(NH4)2SO4、MgCl2 , 一定没有AlCl3、FeCl3
D . 混合物中一定有Al、(NH4)2SO4、MgCl2、AlCl3 , 一定没有FeCl3
|
|
| 7. 单选题 | |
|
已知某反应aA(g)+bB(g)⇌cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )

A . T1<T2 , P1<P2 , a+b>c,Q>0
B . T1>T2 , P1<P2 , a+b<c,Q>0
C . T1<T2 , P1>P2 , a+b<c,Q>0
D . T1<T2 , P1>P2 , a+b>c,Q<0
|
|
| 8. 单选题 | |
|
将反应Cu(s)+2Ag+(aq)⇌Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是( )

A . KNO3盐桥中的K+移向Cu(NO3)2溶液
B . 当电流计指针指向0时,该反应达平衡,平衡常数K=0
C . 若向硝酸银溶液中加入NaCl固体,随着NaCl量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
D . 向硝酸铜溶液中加入NaOH固体,随着NaOH量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
|
|
| 9. 实验探究题 | |
|
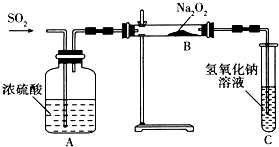
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.请回答下列问题:
|
|
| 10. 推断题 | |
|
有X、Y、Z三种元素,已知:
①X2﹣、Y﹣均与Y的气态氢化物分子具有相同的电子数; ②Z与Y可组成化合物ZY3 , ZY3溶液遇苯酚呈紫色. 请回答:
|
|
高中化学 试卷推荐
- 湖南省长沙市宁乡市2022年高中学业水平模拟(5月)化学试题
- 北京市东城区2022届高三一模考试化学试题
- 黑龙江省肇东市第四中学校2020-2021学年高三上学期化学期中考试试卷
- 四川省射洪市2021年高考化学模拟试卷
- 重庆市2022届高三模拟调研卷(三)化学试题
- 四川省绵阳市2020-2021学年高一下学期期末考试化学试题
- 湖南省岳阳市平江县2022届高三下学期教学质量监测(三)化学试题
- 山西省运城市高中联合体2021-2022学年高一下学期期中联考化学试题
- 江苏省淮安市高中校协作体2020-2021学年高二上学期化学期中考试试卷
- 广西南宁市2020-2021学年高一上学期期末联考化学试题
- 广东省汕头市2022届普通高中毕业班第二次模拟试化学试题
- 河北省石家庄市2020-2021学年高二下学期化学期末考试试卷
最近更新

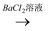 白色沉淀
白色沉淀 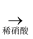 仍有部分白色沉淀不溶解,证明有Na2SO4生成
仍有部分白色沉淀不溶解,证明有Na2SO4生成


