内蒙古鄂尔多斯市乌审旗高级中学2021-2022学年高三上学期10月第一次月考理科综合化学试题
内蒙古鄂尔多斯市乌审旗高级中学2021-2022学年高三上学期10月第一次月考理科综合化学试题
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学与生活、社会发展息息相关,下列有关说法错误的是( )
A . 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
B . 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
C . “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D . 制造新版人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
|
|
| 2. 单选题 | |
|
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 27gAl与NaOH完全反应,转移的电子数为0.1NA
B . 1L0.1mol/LNaHCO3溶液中,HCO3-的数量为0.1NA
C . 标准状况下,11.2L乙烷中含有的共用电子对数目为3NA
D . 0.1mol18O中含有的中子数为1NA
|
|
| 3. 单选题 | |
|
下列化学反应的离子方程式正确的是( )
A . 在
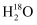 中投入Na2O2固体:2 中投入Na2O2固体:2 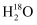 + 2Na2O2= 4Na+ + 4OH -+ 18O2↑
B . 向AlCl3溶液中加入过量的浓氨水: Al3++4NH3·H2O= + 2Na2O2= 4Na+ + 4OH -+ 18O2↑
B . 向AlCl3溶液中加入过量的浓氨水: Al3++4NH3·H2O=  +4 +4  +2H2O
C . 漂白粉溶液在空气中失效: ClO-+CO2+H2O=HClO+HCO3-
D . Fe3O4溶于稀硝酸的反应:3Fe3O4+28H++ +2H2O
C . 漂白粉溶液在空气中失效: ClO-+CO2+H2O=HClO+HCO3-
D . Fe3O4溶于稀硝酸的反应:3Fe3O4+28H++  =9Fe3+ +NO↑+ 14H2O =9Fe3+ +NO↑+ 14H2O
|
|
| 4. 单选题 | |
|
已知硫酸酸化的K2Cr2O7溶液能与KI反应:aH2SO4+bK2Cr2O7+cKI=mK2SO4+nI2+pCr2(SO4)3+qH2O,下列说法错误的是( )
A . a=7
B . K2Cr2O7也可用盐酸酸化
C . 每生成1molCr2(SO4)3 , 转移6mole-
D . 由上述反应可知,I-的还原性强于Cr3+的还原性
|
|
| 5. 单选题 | |||||||||
|
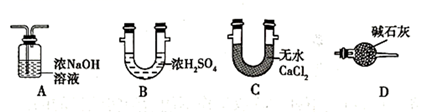
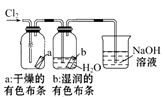
有关下列装置或操作说法错误的是( )
A . 图1中:将胶头滴管中的水滴入到金属钠中,能看到U形管右侧红墨水升高
B . 图2中:观察到湿润的有色布条能褪色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成
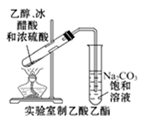
C . 图3可用于制备、收集乙酸乙酯
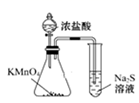
D . 图4可以比较KMnO4、Cl2和S氧化性的相对强弱
|
|||||||||
| 6. 单选题 | |
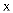 、 、 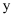 、 、 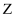 、 、 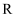 、 、 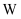 为原子序数依次增大的短周期元素, 为原子序数依次增大的短周期元素, 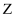 、 、 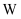 为同族元素, 为同族元素, 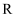 的原子半径是同周期主族元素中最大的。其中, 的原子半径是同周期主族元素中最大的。其中, 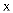 、 、 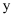 、 、 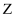 、 、 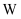 形成的化合物可表示为 形成的化合物可表示为  。下列说法正确的是( ) 。下列说法正确的是( )
A . 原子半径:W>Z>Y
B . 简单氢化物的沸点:W>Z
C .
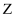 与 与 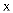 、 、 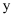 、 、 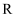 、 、 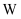 均可形成多种化合物
D . 均可形成多种化合物
D . 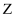 、 、 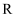 、 、 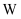 三种元素形成的化合物的水溶液呈中性 三种元素形成的化合物的水溶液呈中性
|
|
| 7. 单选题 | ||||||||||||||||||||||||||
|
下表各组物质中,可以实现X
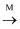 Y Y 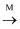 Z(每步只发生一个反应)所示转化的是( ) Z(每步只发生一个反应)所示转化的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||||||||||||
| 8. 综合题 | |
|
解答下列问题
|
|
| 9. 实验探究题 | |
|
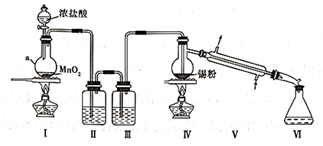
SnCl4可用于染色时的媒染剂、润滑油添加剂、玻璃表面处理剂等。实验室可通过如下图装置制备少量SnCl4(夹持装置略)
已知:①锡的熔点232℃、沸点2260℃;②SnCl2的熔点246.8℃、沸点623℃;③SnCl4的熔点-33℃、沸点114℃,SnCl4极易水解。通常将SnCl4晶体加入浓盐酸中,以配制无色的SnCl4溶液。回答以下问题
|
|
| 10. 综合题 | |
|
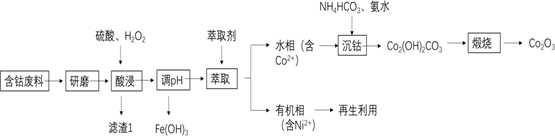
三氧化二钴(Co2O3)常用作制滤光眼镜的添加剂、催化剂和氧化剂。以含钴废料(主要成分CoO、Co2O3 , 含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下:
|
|
高中化学 试卷推荐
- 陕西省榆林市2020年高考理综-化学3月线上模拟试卷
- 2015-2016学年河南省开封市兰考二中高二上学期期末化学试卷
- 2017年高考化学备考复习专题二:化学常用计量
- 2016-2017学年湖北省天门市渔薪高中高一上学期期中化学试卷
- 高中化学人教版(2019)选择性必修1第三章第四节沉淀溶解平衡
- 2015-2016学年河北省秦皇岛市卢龙县高二上学期期末化学试卷
- 专题31:有机综合
- 上海市嘉定区大交附中2019-2020学年高二上学期化学开学考试试卷
- 安徽省濉溪中学2018-2019学年高三化学 电解与电池 单元测试卷
- 广东省惠州市2016-2017学年高一上学期化学期末考试试卷
- 2015-2016学年山东省枣庄市滕州三中高三上学期期末化学模拟试卷(二)
- 2016年云南省弥勒市高考化学模拟试卷(1)
最近更新
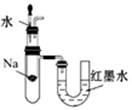

 O2(g)=H2O(l)ΔH1=-akJ·mol-1
O2(g)=H2O(l)ΔH1=-akJ·mol-1 O2(g)=8CO2(g)+9H2O(l)ΔH2=-bkJ·mol-1
O2(g)=8CO2(g)+9H2O(l)ΔH2=-bkJ·mol-1