备考2018年高考化学一轮基础复习:专题32 定量实验和化学实验的设计与评价
备考2018年高考化学一轮基础复习:专题32 定量实验和化学实验的设计与评价
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | |
|
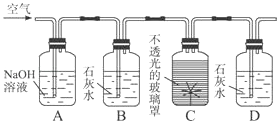
图是测定植物的某一生命活动过程的实验装置.A瓶中NaOH溶液的作用是,B瓶中的石灰水的作用是,D瓶中出现的现象是.此实验说明植物具有性质.
|
|
| 2. 实验探究题 | |
|
某强酸性溶液X,可能含有Al3+、Ba2+、NH
 、Fe2+、Fe3+、CO 、Fe2+、Fe3+、CO  、SO 、SO  、SiO 、SiO  、NO 、NO  中的一种或几种离子,取该溶液进行实验,其现象及转化如图.反应过程中有一种气体是红棕色. 中的一种或几种离子,取该溶液进行实验,其现象及转化如图.反应过程中有一种气体是红棕色.
请回答下列问题:
|
|
| 3. 单选题 | |
|
中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液进行实验,下列说法不正确的是( )
A . 改用25mL 0.50mol/L盐酸跟25mL 0.55 mol/L NaOH溶液进行反应,求出的中和热数值和原来相同
B . 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
C . 装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热减少热量损失
D . 实验中应记录测量出的最高温度
|
|
| 4. 填空题 | |
|
①用50mL0.50mol/L盐酸与50mL一定浓度的NaOH溶液在如图所示的装置中进行中和反应.
通过测定反应过程中所放出的热量可计算中和热.该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称,另一处错误是. ②实验室提供了0.50mol/L和0.55mol/L两种浓度的NaOH溶液,应该选择mol•L﹣1的溶液进行实验.大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”). ③如果用相同浓度和体积的醋酸(CH3COOH)代替HCl溶液进行上述实验,测得的中和热的数值会;(填“偏大、偏小、无影响”) 如果用60mL0.50mol/L盐酸与50mL0.55mol/L的NaOH溶液所求中和热(填“相等、不相等”). |
|
| 5. 单选题 | |
|
侯氏制碱法的原理为:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl,2NaHCO3
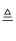 Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( ) Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( )
A .
 制备氨气
B . 制备氨气
B . 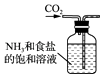 制取NaHCO3
C . 制取NaHCO3
C .  分离NaHCO3
D . 分离NaHCO3
D .  灼烧NaHCO3 灼烧NaHCO3
|
|
| 6. 单选题 | ||||||||||||||||
|
下列实验“操作和现象”与“结论”对应且正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 7. 单选题 | |
|
某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如图装置(含试剂)进行实验.
下列说法不正确的是( )
A . 必须在②③间添加吸收HCl的装置
B . ④的作用是防止空气中的气体影响实验的精确度
C . 通入空气的作用是保证②中产生的气体完全转移到③中
D . 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
|
|
| 8. 单选题 | |
|
海带提碘实验中,不会用到的装置是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 9. 单选题 | |
|
下列实验操作能达到实验目的是( )
A . 用排水法收集铜粉与浓硝酸反应产生的NO2
B . 用氨水鉴别NaCl、MgCl2、AlCl3、NH4Cl四种溶液
C . 用酸性KMnO4溶液验证草酸的还原性
D . 用饱和NaHCO3溶液除去Cl2中混有的HCl
|
|
| 10. 单选题 | |
|
用标准浓度的NaOH溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗 ②锥形瓶中盛有少量蒸馏水,再加待测液 ③酸式滴定管用蒸馏水洗净后,未用盐酸润洗 ④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失 ⑤滴定后观察碱式滴定管读数时,俯视刻度线.
A . ①④
B . ①③
C . ②③
D . ④⑤
|
|
高中化学 试卷推荐
- 陕西省榆林市第二中学2018-2019学年高二下学期化学期中考试试卷
- 2018年高考理综化学真题试卷(全国Ⅲ卷)
- 天津市红桥区2017-2018学年高一上学期化学期末考试试卷
- 专题18:化学反应与能量变化
- 人教版化学高二选修4第四章第二节化学电源同步练习
- 安徽省江南十校2017-2018学年高一上学期化学期中考试试卷
- 江苏省启东市2019-2020学年高一下学期化学期末考试试卷
- 北京市昌平区2016-2017学年高一上学期化学期末考试试卷
- 广东省东莞高级中学2019-2020学年高一下学期化学期中考试试卷
- 高中化学人教版(2019)选择性必修1第二章第一节化学反应速率
- 浙江省衢州市2017-2018学年高一上学期化学期中考试试卷
- 山东省烟台市2018-2019学年高三上学期化学期末考试试卷
最近更新